Lyme-Borreliose
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
Loslegennach der US-amerikanischen Ortschaft Lyme
Synonyme: Lyme-Krankheit, Lyme-Erkrankung
Englisch: Lyme disease, Lyme borreliosis
Definition
Die Lyme-Borreliose ist die häufigste durch Vektoren übertragene Erkrankung weltweit. Sie wird durch das Bakterium Borrelia burgdorferi oder verwandte Arten aus der Gruppe der Spirochäten hervorgerufen.
ICD-10-Code
- A69.2 Lyme-Krankheit inkl. Erythema chronicum migrans durch B. burgdorferi
- M01.1 Arthritis bei Lyme-Krankheit
- G05.0 Enzephalitis, Myelitis und Enzephalomyelitis bei anderenorts klassifizerten Krankheiten
Ätiologie
Während die Borreliose in den USA fast ausschließlich durch Borrelia burgdorferi sensu stricto (Borrelia burgdorferi "im engeren Sinn") und Borrelia mayonii hervorgerufen wird, sind in Europa neben Borrelia burgdorferi vier weitere Genospezies zu berücksichtigen:
- Borrelia garinii (auch häufig in Asien)
- Borrelia afzelii
- Borrelia bavariensis
- Borrelia spielmanii
Diese sechs der über zwanzig beschriebenen Spezies sind gesichert humanpathogen und werden unter dem Begriff Bbsl-Komplex (Borrelia burgdorferi sensu lato) zusammengefasst.
Borrelia burgdorferi ist ein empfindliches, mikroaerophiles, aktiv bewegliches, gramnegatives, schraubenförmiges Bakterium mit einem linearen Chromosom und überdurchschnittlich vielen Lipoproteinsequenzen. Es ist in der Lage, die Lipoproteine auf der Zelloberfläche von Generation zu Generation zu verändern. Auf die Weise können Borrelien von spezifischen Antikörpern schlecht erkannt werden (Immunevasion) und im Körper überdauern.
Epidemiologie
Die Genospezies des Bbsl-Komplex leben enzootisch. Übertragen wird die Lyme-Borreliose durch Zeckenarten des Ixodes-ricinus-Komplex. Eine Übertragung durch blutsaugende Insekten wurde bisher nicht sicher dokumentiert. Eine Ansteckung von Mensch zu Mensch ist nicht möglich.
Zum Ixodes-ricinus-Komplex gehören:
- Ixodes ricinus: Hauptvektor in Europa bis Russland, überträgt außerdem das FSME-Virus
- Ixodes scapularis ist der wichtigste Vektor im Nordosten sowie mittleren Westen der USA; überträgt außerdem die Babesiose (Babesia microti), humane Anaplasmose (Anaplasma phagocytophilum) sowie seltener Borrelia miyamotoi, Theileria microti und das Powassan-Virus.
- Ixodes pacificus: Vektor an der Westküste der U.S.A.
- Ixodes persulcatus: Im asiatischen Teil Russlands, in China und Japan; überträgt außerdem das FSME-Virus
Die Zecken durchlaufen erst ein Larven- und ein Nymphenstadium, bevor sie ausgewachsen sind. In jedem dieser Stadien nehmen sie eine Blutmahlzeit zu sich. Das Infektionsrisiko für den Menschen ist abhängig von der Häufigkeit des Auftretens der Zecken, deren Nahrungsgewohnheiten und ihrer tierischen Wirte. Beispielsweise sind Weißfußmäuse und andere Nagetierarten der bevorzugte Wirt für die Larven und Nymphen der Ixodes scapularis-Zecken. Die Borrelien werden im Frühsommer von infizierten Nymphen auf die Mäuse und im Spätsommer über die infizierten Mäuse auf die Larven übertragen, die sich wieder zu Nymphen entwickeln. Als weiteres Erregerreservoir gelten Vögel, Reptilien, Igel, Füchse oder Kaninchen. Die Infektion des Menschens ist eine Sackgasse für die Spirochäte.
In Europa liegt die Inzidenz der gemeldeten Fälle bei ungefähr 30.000 pro Jahr, vermutet werden jedoch eher 150.000 pro Jahr. Höhere Fallzahlen finden sich in Mitteleuropa und Skandinavien. Jedoch ist die genaue Häufigkeit in Deutschland nicht bekannt. Die Meldeinzidenz schwankt zwischen 60.000 bis über 200.000 Erkrankungen pro Jahr mit deutlichen geografischen Unterschieden. Von einer Infektionsgefährdung ist in allen Teilen Deutschlands auszugehen. Die Durchseuchungsrate der Zecken liegt gebietsabhängig zwischen 5 und 35 %. Neuere Daten legen nahe, dass die Inzidenz in Europa weiterhin steigt, u. a. im Kontext der Klimaveränderungen und erweiterten Zeckengebiete.
Das Infektionsrisiko ist stark von den Witterungsbedingungen abhängig. Ixodes ricinus ist ab einer Temperatur von 6 °C aktiv. Erkrankungen treten gehäuft zwischen Juli und August auf. Davon ausgenommen sind Manifestationen mit langer Latenzzeit (Lyme-Arthritis, späte Neuroborreliose), die weitestgehend unabhängig von der Saisonalität auftreten können.
Pathophysiologie
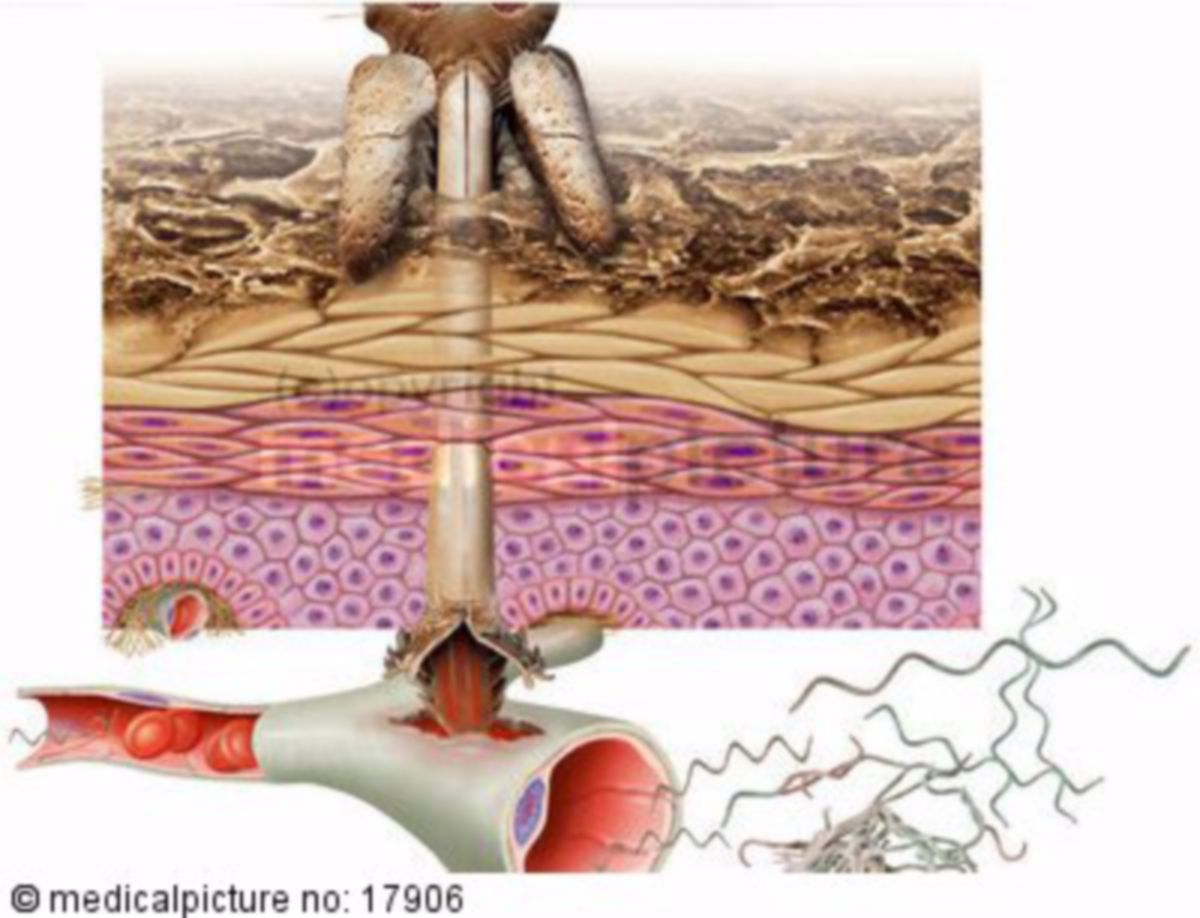
In der nüchternen Zecke befinden sich die Borrelien im Darm. Nach Beginn des Saugaktes wandern sie in die Speicheldrüsen, von wo sie auf den Menschen übertragen werden. Daher muss die Zecke zumindest mehrere Stunden, meist mindestens 24 Stunden, am Wirt verbleiben, damit sie Borrelien übertragen kann. Eine zuverlässige zeitliche Untergrenze, ab welcher mit einer Infektion zu rechnen ist, lässt sich jedoch nicht ableiten. Nach dem Eindringen in die Haut breiten sich die Borrelien zentrifugal aus und können hämatogen oder lymphogen andere Organe befallen.
Zusätzlich zur klassischen Systemausbreitung ist eine Neuroinvasion möglich: Über den Blut-Liquor-Schranke-Weg oder entlang peripherer Nervenfasern können Borrelien das Nervensystem erreichen.
Symptomatik
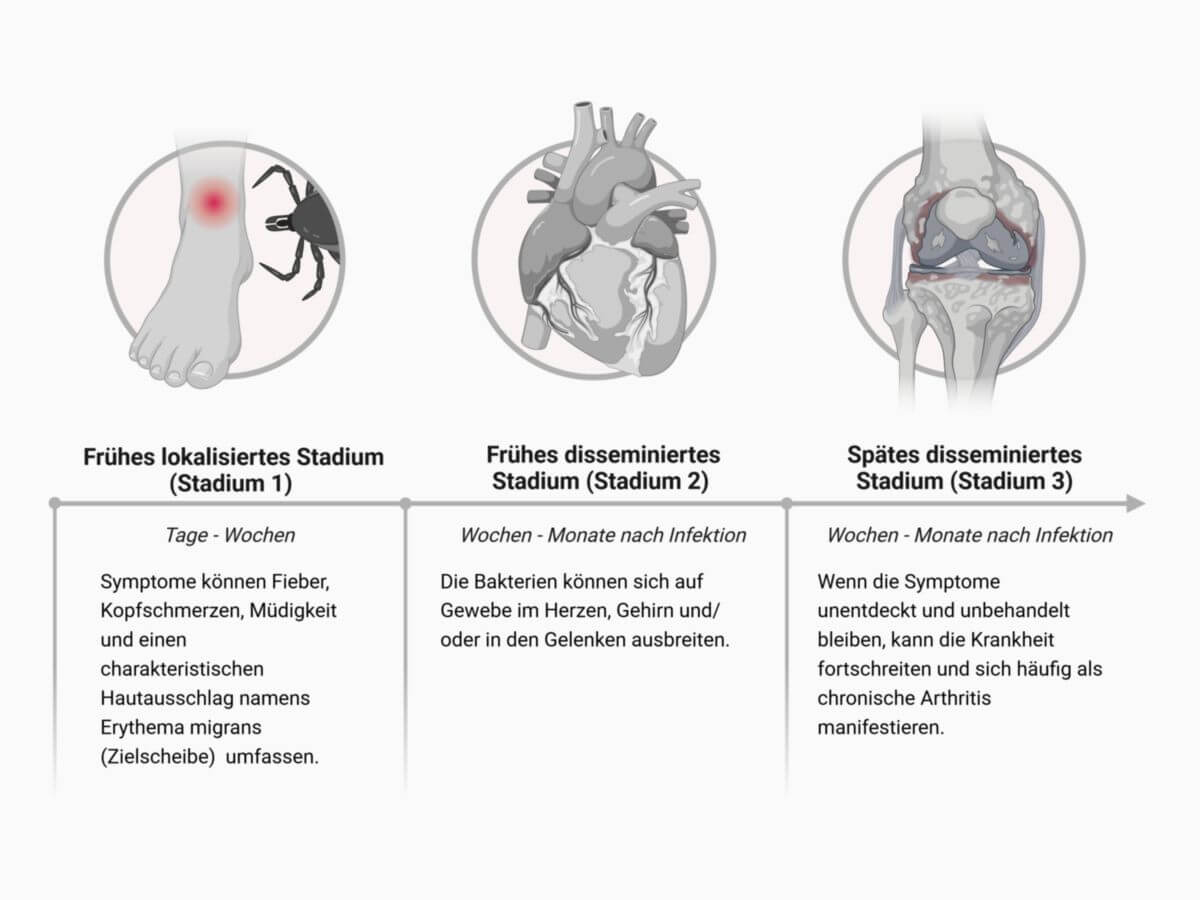
Die meisten Infektionen führen nicht zu Symptomen. Der Verlauf der multisystemischen Lyme-Borreliose wird meist in drei Stadien eingeteilt. Diese Einteilung beinhaltet einen Übergang von einem anfangs eher lokalen Geschehen zu einer mehr systemischen Beteiligung, stellt jedoch einen "idealisierten" Verlauf dar.
Während alle Borrelien ein Erythema migrans aulösen können, zeigen B. garinii und B. bavariensis eine Assoziation mit neurologischen Manifestationen, B. afzelii mit der Entwicklung einer Acrodermatitis chronica atropicans und B. burgdorferi sensu stricto ist assoziiert mit der Lyme-Arthritis.
Frühes lokalisiertes Stadium (Stadium 1)
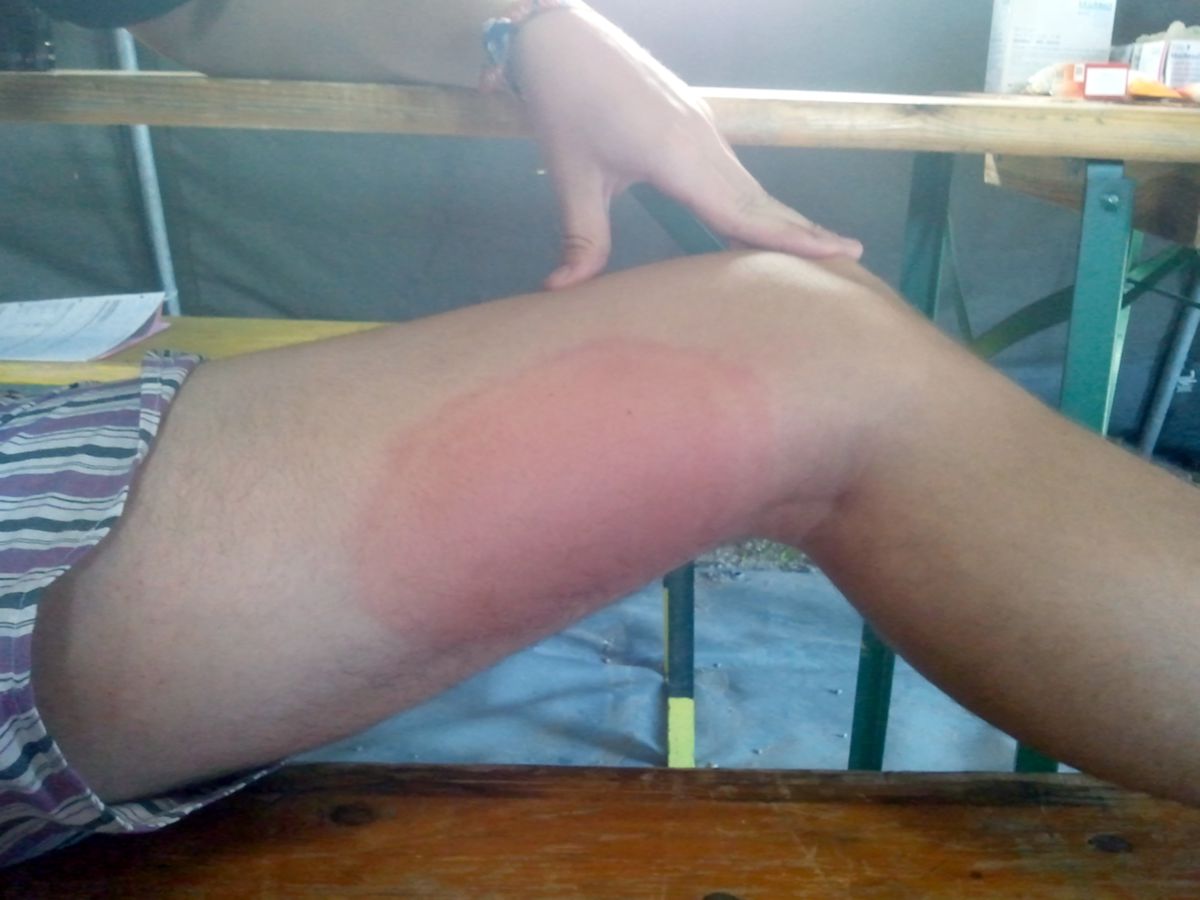
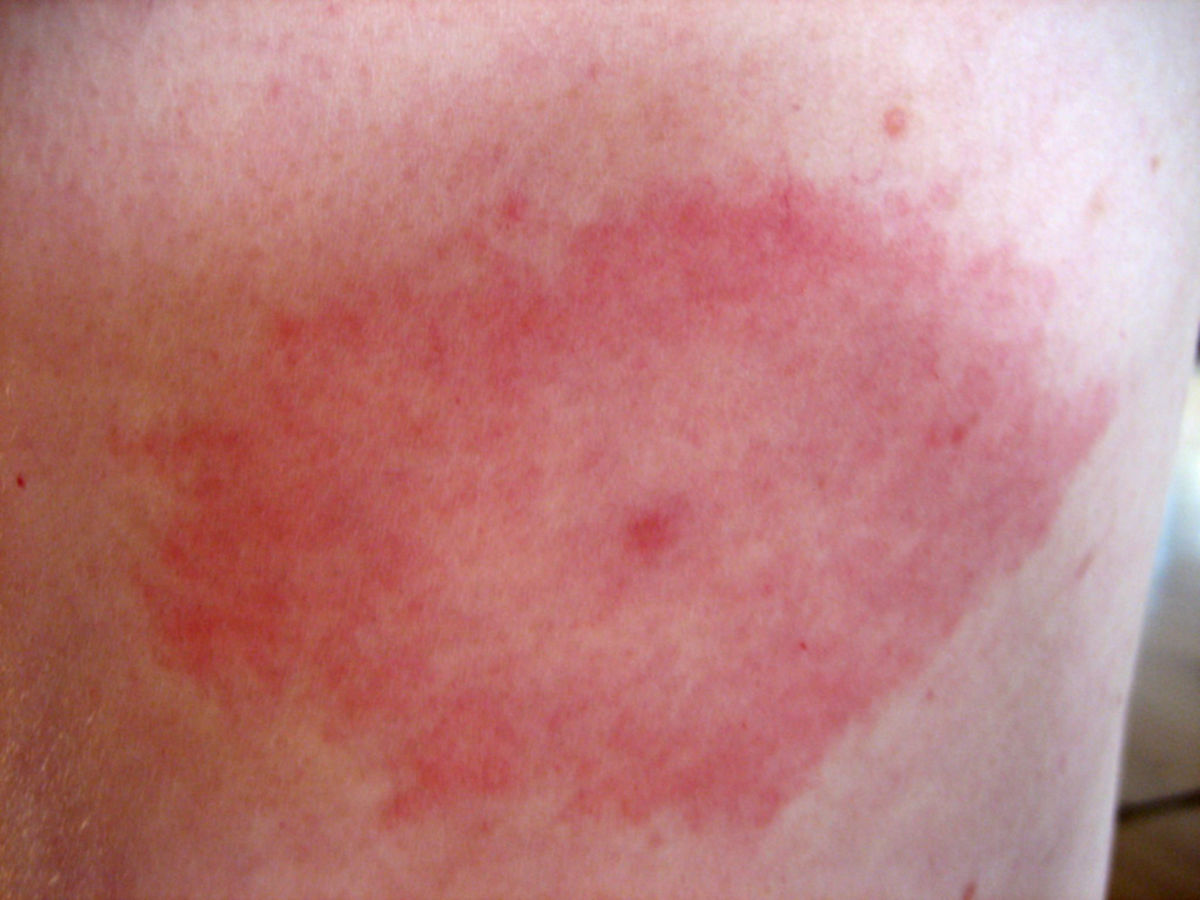
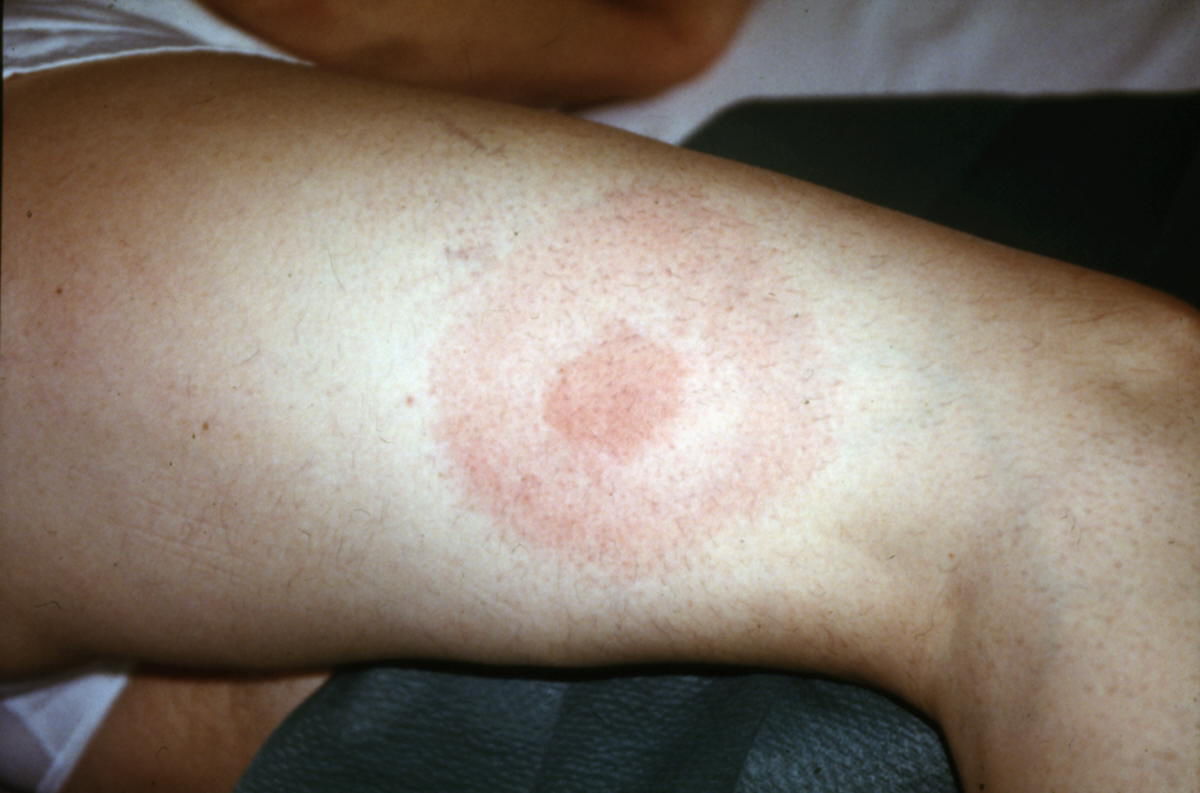
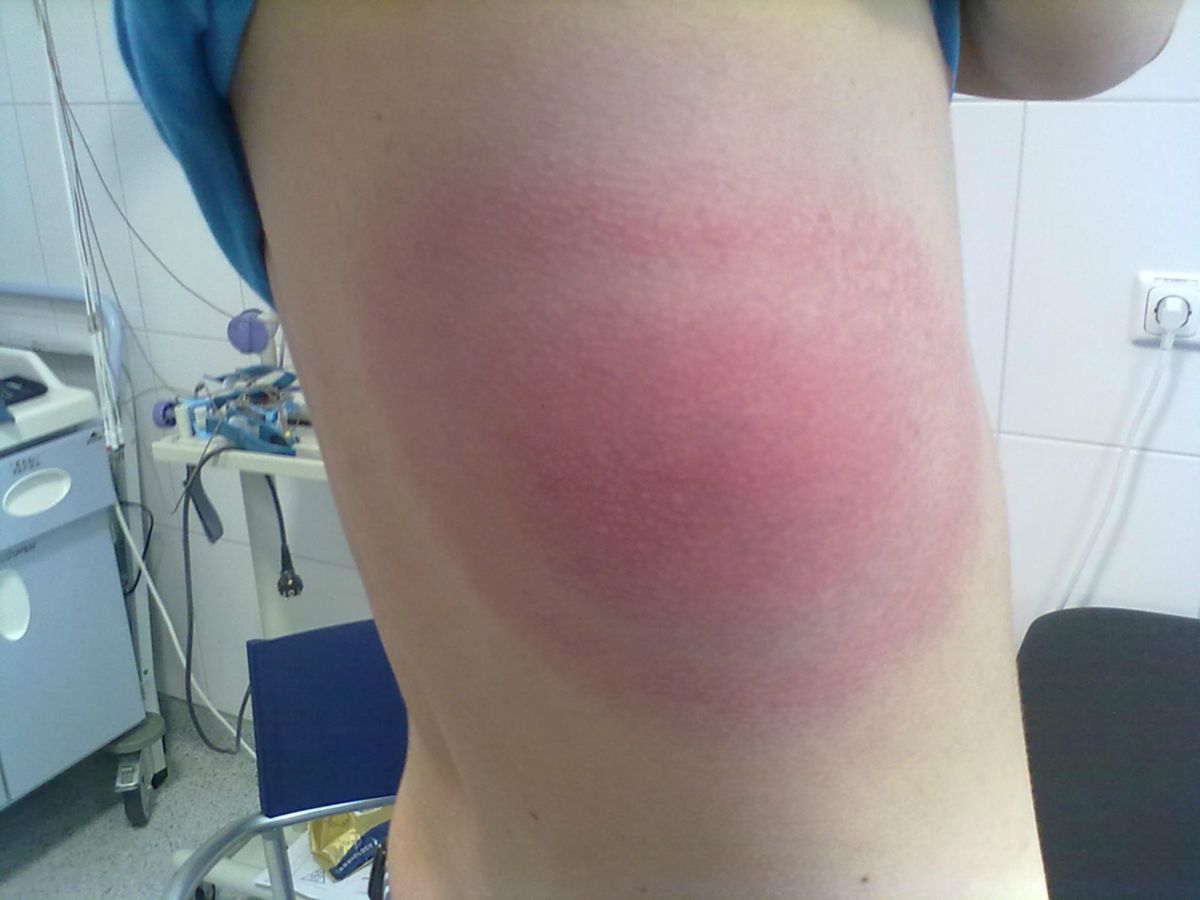
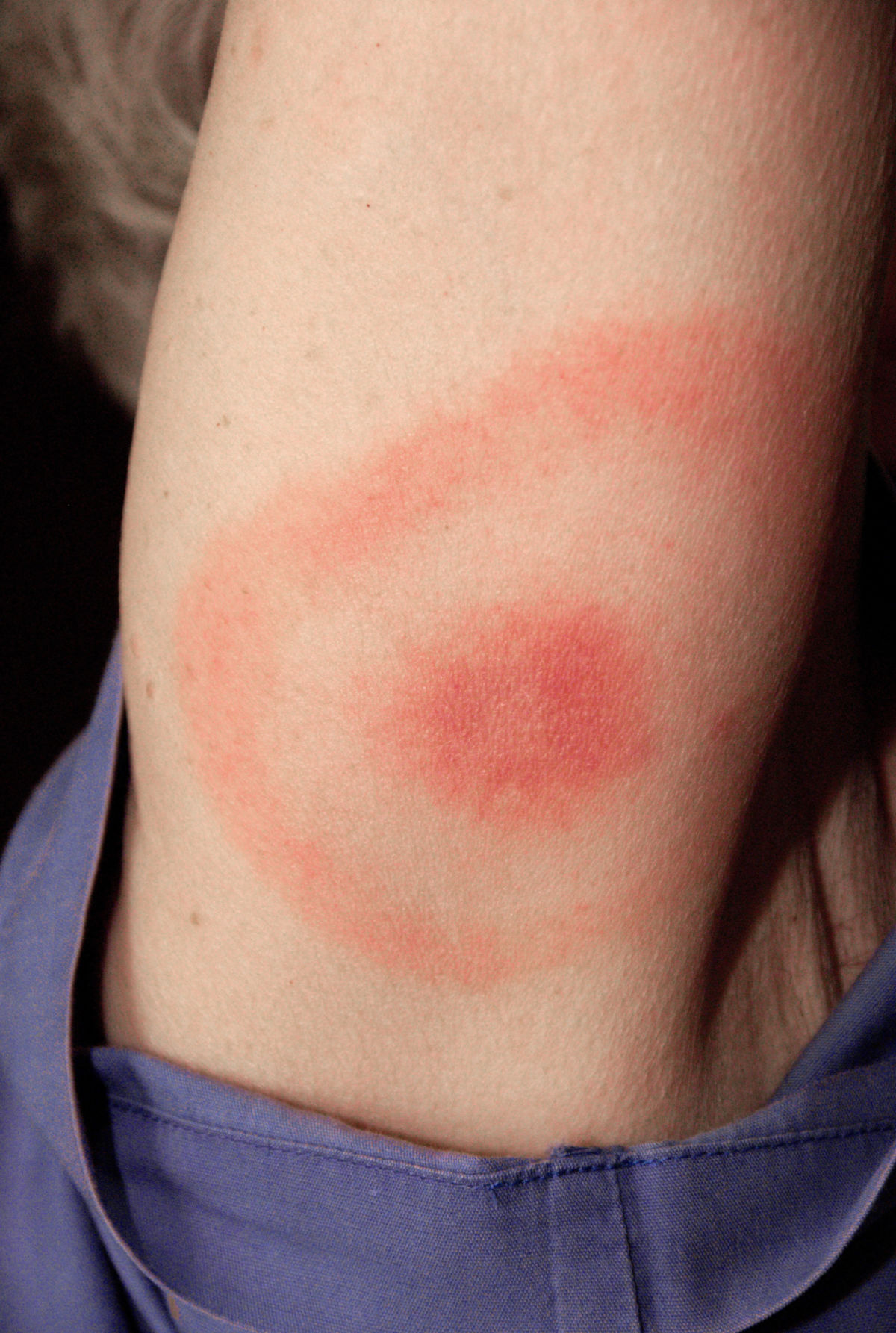
Bei über 90 % der Patienten kommt es nach einer Inkubationszeit von 3 bis 32 Tagen (Median 8 Tage) an der Einstichstelle zur Ausbildung eines Erythema migrans. Dieses Erythem beginnt meist als rötliche Makula oder Papel, die sich langsam zentrifugal zu einem großen Ring ausweitet; meist mit hellrotem Rand und zentraler Aufhellung. Das Zentrum kann manchmal auch gerötet und induriert erscheinen. Selten kommt es zur Blasenbildung oder Nekrose. Die Hautveränderung ist oft leicht erwärmt aber nur selten schmerzhaft. In einigen Fällen finden sich eine gleichmäßige, intensive Rotfärbung oder mehrere Ringe um ein bläuliches Zentrum. Das Erythema migrans kann am ganzen Körper lokalisiert sein, meist an den Oberschenkeln, in den Leisten und in den Achselhöhlen. Besteht das Erythema migrans über Wochen oder Monate, wird es als Erythema chronicum migrans bezeichnet.
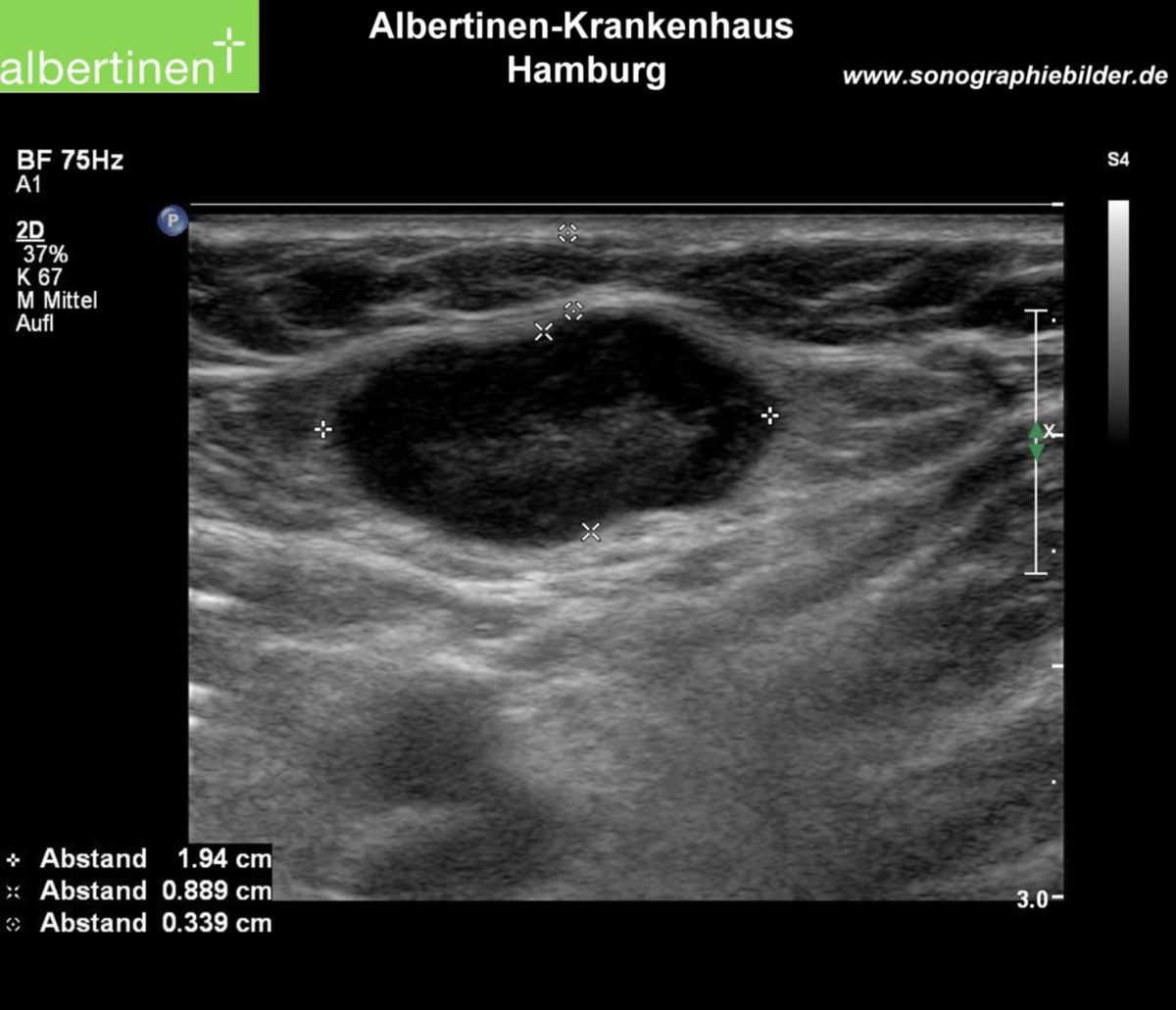
Selten und bevorzugt bei Kindern kann es zu einem meist solitären, livid-roten subkutanen Knoten oder Plaque kommen, der histologisch aus einem lymphozytären Infiltrat besteht. Dieses Borrelien-Lymphozytom ist ein Pseudolymphom und wird auch als Lymphadenosis cutis benigna bezeichnet. Es findet sich bevorzugt an den Ohrläppchen, Mamillen oder im Genitalbereich.
Frühes disseminiertes Stadium (Stadium 2)
Innerhalb von Tagen bis Wochen nach Auftreten des Erythema migrans kann eine hämatogene Streuung in verschiedene Organe erfolgen. Sekundäre ringförmige Hautveränderungen, die dem initialen Erythema migrans ähneln, werden als multiple Erythema migrantia bezeichnet. Begleitend können Kopfschmerzen, leichte Nackensteifigkeit, subfebrile Temperaturen bis hin zu Fieber, Myalgien, Unwohlsein und Müdigkeit auftreten. Seltener kommt es zur generalisierten Lymphadenopathie, Splenomegalie, Hepatitis, Pharyngitis, unproduktivem Husten, Konjunktivitis, Iritis und Hodenschwellung. Bis auf die Müdigkeit und Abgeschlagenheit treten die Symptome oft intermittierend auf.
Auch bei unbehandelten Patienten kommt es in der Regel zu einer Besserung. Bei etwa 15 % der unbehandelten Patienten entsteht wenige Wochen bis einige Monate nach dem Zeckenstich eine frühe Neuroborreliose: Die häufigste Manifestationsform bei Erwachsenen in Europa ist das Garin-Bujadoux-Bannwarth-Syndrom (Meningoradikuloneuritis). Die Radikulitis äußert sich durch nachts betonte, initial segmentale Schmerzen wechselnder Lokalisation. Sie haben einen brennenden, bohrenden, beißenden oder reißenden Charakter und sprechen nur gering auf Analgetika an. Das Maximum erreichen die Schmerzen innerhalb weniger Stunden oder Tage. Bei ungefähr 75 % der Betroffenen entwickeln sich nach 1 bis 4 Wochen neurologische Ausfälle:
- Paresen, seltener Sensibilitätsstörungen
- Alle Hirnnerven (außer dem Nervus olfactorius) können beteiligt sein, am häufigsten der Nervus facialis, dabei meist als bilaterale Fazialisparese mit/ohne Geschmacksstörung. Eine vollständige Rückbildung wird in den meisten Fällen innerhalb von 1 bis 2 Monaten beobachtet.
Bei Kindern sind die häufigsten Manifestationen einer Neuroborreliose eine lymphozytäre Meningitis und eine Fazialisparese. Die Symptome der Meningitis sind meist nur diskret. Weiterhin können neben dem Nervus facialis insbesondere die Nerven der äußeren Augenmuskeln betroffen sein. Eine radikuläre Symptomatik ist selten.
Bei bis zu 8 % der Patienten kann es innerhalb einiger Wochen nach Erkrankungsbeginn zur kardialen Beteiligung kommen (Lyme-Karditis), meist mit diffuser Symptomatik wie bei einer akuten Myoperikarditis. Diese Symptome klingen meist nach ein paar Wochen ab, können aber rezidivieren. Fälle einer chronischen Kardiomyopathie sind beschrieben.
In diesem Stadium kommt es außerdem häufig zu Myalgien und Arthralgien (frühe/flüchtige Lyme-Arthritis), die wandernd in den Gelenken, Sehnen, Bursen, Muskeln oder Knochen und in der Regel ohne Schwellung auftreten. Meist hält der Schmerz Stunden oder Tage an.
Spätes disseminiertes Stadium (Stadium 3)
In den USA entwickelt sich bei ungefähr 60 % der unbehandelten Patienten Monate nach Erkrankungsbeginn eine (chronische) Lyme-Arthritis. In Deutschland sind die Genospezies B. fazelii und B. garinii deutlich seltener mit einer Arthritis assoziiert (ungefähr 5 % der Patienten). Die Lyme-Arthritis ist eine Mon- oder Oligoarthritis der großen Gelenke, insbesondere des Kniegelenks, die Wochen bis Monate anhalten kann. Kleine Gelenke sind wenn überhaupt nur in der Frühphase betroffen. Bei einem kleinen Prozentsatz der Patienten kommt es zur Schädigung des Knorpel- und Knochengewebes. Trotz adäquater Therapie sind Fälle einer antibiotikarefraktären Arthritis beschrieben, wobei von einer autoimmunologischen Reaktion bei genetisch Prädisponierten ausgegangen wird. Sie ist assoziiert mit HLA-DRB1*0401 oder HLA-DRB1*0101 und dem Polymorphismus 1805GG des Toll-like Rezeptors 1.
Seltener kann eine neurologische Symptomatik erst Monate oder Jahre nach Infektion auftreten ("späte Neuroborreliose"), meist in Form einer schleichenden Enzephalopathie. Mögliche Symptome sind Paresen, Sprach- und Sprechstörungen, Koordinationsstörungen, gelegentliche epileptische Anfälle, selten ein organisches Psychosyndrom oder Halluzinationen. Weiterhin können sich eine Myelitis mit querschnittförmig verteilten Sensibilitätsstörungen, zentrale und periphere Paresen sowie Blasenentleerungsstörungen manifestieren. Eine borrelieninduzierte Vaskulitis zeigt sich hauptsächlich in Form eines ischämischen Insult. Extrem selten manifestiert sich eine späte Neuroborreliose mit einer Myositis. Eine periphere (axonale) Polyneuropathie zeigt sich meist nur in Kombination mit einer Acrodermatitis chronica atrophicans.
Diese späte Hautmanifestation der Borreliose ist überwiegend mit B. afzelii assoziiert. Sie betrifft hauptsächlich ältere Frauen und ungefähr einen Prozent der Infizierten. Die Hautläsionen sind vor allem akral an Armen und Beinen lokalisiert. Im initial ödematös-infiltrativen Stadium findet sich ein hellrotes retikuläres, zunehmend livides, ödematöses Erythem. Im Verlauf kommt es zur zunehmenden Atrophie aller Hautschichten und Hautanhangsgebilde (atrophes Stadium). Gelegentlich sieht man auch juxtaartikuläre, derbe, fibroide Knoten sowie bandförmige Streifen.
Post-Lyme-Syndrom
Monate oder Jahre nach Beseitigung der objektiven Befunde der Infektion leiden einige Patienten noch unter Schmerzen, neurokognitiven Manifestationen oder Erschöpfungssyndromen. Dieses chronische Beschwerdebild ist nicht allgemeingültig definiert und kein einheitlich akzeptiertes Syndrom. Das Post-Lyme-Syndrom wird in der Literatur uneinheitlich auch als Post-Treatment Lyme Disease Syndrome (PTLDS) oder Post-Lyme-Enzephalopathie bezeichnet. Die Symptome können sich innerhalb von Monaten zurückbilden oder über Jahre bestehen bleiben und einer Fibromyalgie ähneln. Oft bestehen Angst und Depression als Komorbidität. Insgesamt spricht die aktuelle (2022) Evidenzlage weder für eine chronische Borrelieninfektion noch für einen Autoimmunprozess.
Diagnostik
Die Lyme-Borreliose ist eine primär klinische Diagnose, die durch serologische und ggf. molekularbiologische Untersuchungen gestützt wird. Bei dem klassischen Bild eines Erythema migrans kann unter Umständen auf eine serologische Diagnostik verzichtet werden.
Frischer Zeckenstich
Anamnestisch wird ein Zeckenstich von bis zu 50 % der Borreliose-Patienten verneint, daher schließt dies eine Lyme-Borreliosee nicht aus. Eine Untersuchung der Zecke auf Borrelien mittels PCR ist möglich, jedoch nicht sinnvoll, da ein negatives Ergebnis die Infektiosität nicht völlig ausschließt. Daher sollte die Stichstelle lediglich für 4 bis 6 Wochen beobachtet werden.
Serologische Diagnostik
Material
Für die Untersuchung wird 1 ml Serum benötigt.
Methoden
Da es keinen optimalen Einzeltest gibt, wird in der Regel zweistufig vorgegangen:
- Stufe 1: ELISA als Suchtest
- Stufe 2: Immunoblot als Bestätigungstest
Referenzbereiche ELISA
| Test | Ergebnis | Bewertung |
|---|---|---|
| IgG IgM |
< 3 U/ml | negativ |
| 3–5 U/ml | schwach positiv | |
| > 5 U/ml | positiv |
Interpretation
Die IgM-Antikörper sind erst ab der 3. Woche positiv. Aufgrund dieser diagnostischen Lücke erfolgt gegebenenfalls eine Wiederholung der Untersuchung nach 3 bis 4 Wochen. Der IgG-Antikörperanstieg beginnt ab der 6. Woche. Durch den Einsatz des VlsE- bzw. C6-Peptids als Testantigen lassen sich IgG-Antikörper mittlerweile früher nachweisen. Bei den Spätmanifestationen finden sich in der Regel nur hohe IgG-Antikörperkonzentrationen.
In der frühen Immunantwort sind relevante Antigene Flagellenprotein (p41), OspC, und VlsE, bei der späten Immunantwort p83/100, p58, p43, p39, p30, p21, DbpA (Osp 17), p14 sowie VlsE.
Die serologische Diagnostik kann nicht sicher zwischen einer akuten oder einer vergangenen Infektion unterscheiden, da die Antikörper-Titer über Jahre persistieren. Waldarbeiter in deutschen Risikogebieten sind geschätzt zu 20 % seropositiv. In der Altersgruppe der 14- bis 17-Jährigen liegt die Antikörper-Prävalenz bei 7 %. In der Gruppe der 70 bis 79-Jährigen zwischen 16 und 25 %.[1] Entsprechend ist eine serologische Untersuchung nicht zum Screening geeignet und sollte nur bei ausreichendem klinischen Verdacht erfolgen.
Weiterhin ergeben sich falsch-positive Reaktionen bei Autoimmunerkrankungen, Syphilis oder EBV-Infektionen. Ein negativer Antikörpernachweis bei längerer Krankheitsdauer schließt bei einem immungesunden Patienten eine Lyme-Borreliose weitestgehend aus. Bei immunsupprimierten Patienten (z.B. unter Rituximab) kann die Antikörperbildung abgeschwächt sein. Ein isolierter IgM-Nachweis spricht gegen eine Spätmanifestation.
Direkter Erregernachweis
Die kulturelle Anzucht von Borrelien gestaltet sich schwierig und wird nur in Ausnahmefällen mittels Barbour-Stoenner-Kelly-Medium durchgeführt. In frühen Stadien gelingt sie nur in einigen Fällen aus Hautbiopsien und seltener aus Blutplasma oder Liquor.
Bei fortgeschrittener Infektion ist die PCR für den Nachweis von Borrelien aus der Gelenkflüssigkeit der kulturellen Anzucht überlegen. Da die DNA von Borrelien aber auch noch Wochen nach einer Therapie persistieren kann, ist der DNA-Nachweis kein Test auf eine aktive Gelenkinfektion. Die Sensitivität der PCR im Liquor ist deutlich geringer als in der Gelenkflüssigkeit.
Liquordiagnostik
Material
Für die Untersuchung werden 2 ml Liquor und 1 ml Serum benötigt.
Befunde
Für die Diagnose einer Neuroborreliose ist eine Liquoruntersuchung notwendig. Typischerweise sind entzündliche Veränderungen zu erwarten:
- Lymphozytäre Pleozytose mit Plasmazellen und Lymphozyten
- Zellzahl meist zwischen 170 bis 220/µl
- Erhöhung des Gesamteiweiß bzw. des Albuminquotienten (Schrankenstörung)
- In der Frühphase intrathekale IgM-Synthese und meist IgG-Synthese, in 70 bis 80 % der Fälle Nachweis von oligoklonalen IgG-Banden
- Bei der späten Neuroborreliose häufiger und höhere intrathekale IgG- und IgA-Syntheseraten
- Laktat nur gering erhöht
- Glukose normal oder leicht erniedrigt
Borrelienspezifischer Antikörperindex
Zur Bestimmung des borrelienspezifischen Antikörper-Index (AI) wird analog zur Reibermethode berechnet.
Als Cut-off für einen positiven AI wird ein Wert ab 1,5 empfohlen. Die spezifische intrathekale Antikörperproduktion beginnt ab der zweiten Krankheitswoche und ist nach 6 bis 8 Wochen bei den meisten Patienten nachweisbar.
Zusätzliche Liquordiagnostik
Der Nachweis des Chemokins CXCL13 im Liquor korreliert mit dem Auftreten von Symptomen der frühen Neuroborreliose und kann die Diagnose in unklaren Fällen unterstützen. Meist steigt die Konzentration noch bevor eine spezifische Antikörperantwort generiert wird. Jedoch ist der Wert nicht spezifisch für die Neuroborreliose, sondern findet sich auch bei Neurolues, tuberkulöser Meningitis und ZNS-Lymphomen. Die Bestimmung wurde bislang (2025) nicht allgemein standardisiert.
Routinelabor
Bei Patienten mit Borreliose finden sich meist normale oder leicht erhöhte Werte für BSG, CRP, Leukozyten und Transaminasen. Das Routinelabor dient der Differenzialdiagnostik.
Bildgebung
Die MRT ist notwendig bei Verdacht auf eine borrelieninduzierte Vaskulitis. Weiterhin zeigen sich durch eine Kontrastmittelaufnahme entzündliche Läsionen im Rahmen einer Enzephalomyelitis. Bei der frühen Neuroborreliose sind unauffällige Befunde zu erwarten, sodass die MRT differenzialdiagnostisch bedeutsam ist.
Weitere Diagnostik
- Neuropsychologische Tests: bei späten Neuroborreliose
- Elektromyografie: bei Polyneuropathie
- EKG: bei Lyme-Karditis finden sich typischerweise ein wechselnder AV-Block sowie EKG-Veränderungen wie bei einer akuten Myoperikarditis
- Gelenkpunktion: bei Lyme-Arthritis kann die Gelenkflüssigkeit analysiert werden; die Zellzahl liegt meist bei ungefähr 25.000/µl, mit einem überwiegenden Anteil von Granulozyten. Rheumafaktoren und antinukleäre Antikörper sind meist negativ. In einer Synovialbiopsie erkennt man Fibrinanreicherungen, zottige Hypertrophien, vaskuläre Proliferationen, mikroangiopathische Läsionen sowie eine ausgeprägte Infiltration mit Lymphozyten und Plasmazellen.
- Beim Post-Lyme-Syndrom zeigen sich weder Zeichen einer Gelenkentzündung noch objektivierbare neurologische Befunde.
Nicht empfohlene Diagnostik
Derzeit (2025) nicht empfohlene Methoden aufgrund nicht ausreichender Validierung:
- Lymphozytenaktivierungs- oder –transformationstest (LTT, MELISA, ELISPOT)
- Direktnachweis von Borrelien mittels lichtmikroskopischer Technik
- PCR oder Antigennachweis aus Urin oder Blut
- Antikörpernachweis aus Immunkomplexen
- Visual Contrast Sensitivity Test (VCS)
- Nachweis einer erniedrigten CD57-positiven Lymphozytensubpopulation.
Differenzialdiagnostik
Wenn sich das initiale Erythem nur wenig ausbreitet, kann es auch für eine unspezifische Reaktion eines nicht infizierten Zeckenstiches gehalten werden. Hierbei zeigt sich ab dem zweiten Tag eine Abnahme des Erythems (Decrescendo-Reaktion). Bei rascher Ausbreitung kann es als Erysipel oder allergische Lokalreaktion fehlgedeutet werden. Weitere Differenzialdiagnosen sind ein fixes Arzneimittelexanthem, eine initiale Morphea und ein Granuloma anulare.
Bei multiplen Erythema migrata muss an ein Erythema exsudativum multiforme gedacht werden, wobei es bei der Borreliose weder zur Blasenbildung an Schleimhäuten noch zur kutanen palmoplantaren Beteiligung kommt. Weitere Differenzialdiagnosen sind ein Erythema anulare centrifugum und eine Parvovirus B19-Infektion (Ringelröteln).
Bei einem Borrelien-Lymphozytom muss man an ein solitäres Mastozytom und an ein solitäres B- bzw. T-Zell-Lymphom denken.
Die Acrodermatitis chronica atrophicans erinnert an kutane Manifestationen des Lupus erythematodes, an ein kutanes Lymphom, zirkumskripte Sklerodermie, an eine Altersatrophie der Haut oder an eine chronisch venöse Insuffizienz.
Eine Fazialisparese ist oft mit einem Erythema migrans assoziiert. Selten kann bei Borreliose jedoch auch eine isolierte Fazialisparese auftreten. Generell muss die Neuroborreliose von einer FSME, Plexusneuritis, Spondyloarthritis, Polymalgia rheumatica, Guillain-Barré-Syndrom, multiplen Sklerose und einem Bandscheibenvorfall abgegrenzt werden.
Die Lyme-Arthritis ähnelt insbesondere einer reaktiven Arthritis bei Erwachsenen und einer juvenilen idiopathischen Arthritis bei Kindern. Weitere Differenzialdiagnosen sind eine Psoriasis-Arthritis, enteropathische Arthritis, rheumatische Arthritis und das Löfgren-Syndrom
Weiterhin ist zu beachten, dass verschiedene Zeckenarten auch eine Babesiose, humane Anaplasmose, ein Rückfallfieber, die FSME sowie die Powassan-Enzephalitis übertragen können. Obwohl Infektionen mit Babesien und Anaplasmen meist asymptomatisch verlaufen, können Patienten auch unspezifische Symptome zeigen. Eine Babesiose verursacht oft eine Thrombopenie und in schweren Fällen eine hämolytische Anämie, die humane Anaplasmose eine Leukopenie und Thrombopenie. Anaplasmen können eine positive IgM-Antwort auf B. burgdorferi hervorrufen. In Endemiegebieten zeigen ungefähr 4 % der Patienten Zeichen einer Koinfektion.
Therapie
Grundsätzlich kann jede Manifestation mit Doxycyclin (2 x 100 mg/d p.o.) behandelt werden. Mögliche Alternativen sind:
- Ceftriaxon 1 x 2 g i.v.
- Cefotaxim 3 x 2 g i.v.
- Penicillin G 4 x 5 Millionen IE i.v.
Bei isoliertem Erythema migrans kann insbesondere bei Kindern auch Amoxicillin verwendet werden: 50 mg/kgKG/d bzw. 3 x 500 mg/d. Doxycyclin ist bei Schwangeren kontraindiziert.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Bei ungefähr 15 % der Patienten kommt es in den ersten 24 Stunden nach Therapiebeginn zu einer Jarisch-Herxheimer-ähnlichen Reaktion. Die antibiotische Therapie sollte fortgesetzt werden; falls benötigt können symptomatisch NSAR helfen.
Bezüglich der Therapiedauer finden sich in der Literatur unterschiedliche Empfehlungen. In Deutschland wird grundsätzlich eine Therapiedauer von 14 Tagen, bei einer späten Neuroborreliose von 14 bis 21 Tagen empfohlen. Bei einer Lyme-Arthritis, Acrodermatitis chronica atrophicans oder kardialer Beteiligung empfehlen einige Autoren eine Dauer von 30 Tagen. Ein Schrittmacher ist in der Regel nicht notwendig.
Die Borrelienserologie sowie der borrelienspezifische Antikörperindex im Liquor sollten nicht zur Therapiekontrolle eingesetzt werden. Eine antibiotische Kombinationstherapie oder die Verwendung von Chloroquin, Carbapenem oder Metronidazol wird nicht empfohlen. Bei persistierender Entzündung ohne Erregernachweis können NSAR, DMARDs und als Ultima Ratio eine Synovektomie erfolgsversprechend sein. Bei anhaltenden Symptomen trotz adäquater Behandlung (Post-Lyme-Syndrom) ist eine Antibiotikagabe nicht indiziert. Stattdessen sollten die Patienten symptomatisch behandelt werden.
Therapiehinweise
Eine frühe Antibiotikatherapie kann Titerbewegungen, wie z.B. die Ausbildung von IgM-Antikörpern, inhibieren. Auch nach einer erfolgreichen Therapie fallen die Titer nur sehr langsam ab, daher sind serologische Kontrollen frühestens 2 Monate nach der Therapie ratsam. Des Weiteren persistieren die IgM-Titer trotz ausreichender Therapie oft über mehrere Jahre.
Prophylaxe
Protektion
Protektive Maßnahmen zur Verhinderung der Borreliose sind Vermeidung von Zeckenstichen (Expositionsreduktion) durch hautbedeckende Kleidung, hoch schließende Schuhe, Anwendung von Repellents und tägliches Absuchen des Körpers. Die Kleidung sollte ausgeklopft werden.
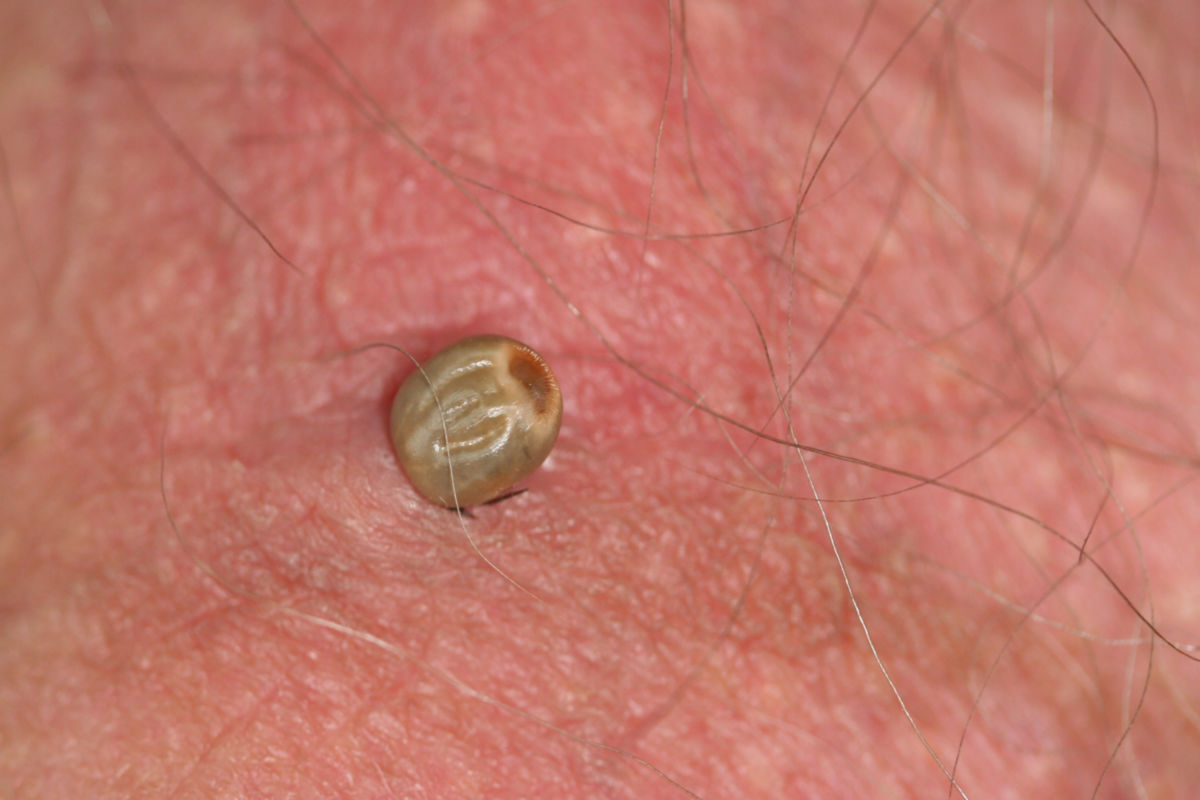
Zeckenentfernung
Die frühzeitige Entfernung (innerhalb von 12–24 Stunden) der Zecken schützt in der Regel vor einer Infektion. Das Risiko einer Infektion nach einem Zeckenstich ist jedoch gering, sodass keine Indikation für eine routinemäßige prophylaktische Antibiotikatherapie vorliegt. Bei der Zeckenentfernung greift man diese mit einer Pinzette nahe der Hautoberfläche und zieht sie zügig gerade aus der Haut. Anschließend sollte die Stichstelle desinfiziert und etwa sechs Wochen beobachtet werden. Wenn keine Pinzette vorhanden ist, sollte die Zecke trotzdem sofort entfernt werden. Bleiben Teile des Stechapparates in der Haut, können diese nachträglich mit einer Nadel oder Kürettage entfernt werden.
Antibiotikaprophylaxe
Bei Hochrisikostichen (endemisches Gebiet, Zecke saß mindestens 36 h am Körper) empfiehlt die Infectious Diseases Society of America (IDSA) für alle Altersgruppen eine Einzeldosis von oralem Doxycyclin innerhalb von 72 Stunden nach der Zeckenentfernung. Dabei erhalten Erwachsene einmalig 200 mg und Kinder 4,4 mg/kg (bis zu einer Höchstdosis von 200 mg).[2]
Impfung
Zur Zeit (2025) befinden sich mehrere Impfstoffe in der Entwicklung:
- I9ISP ist ein Impfstoffkandidat auf mRNA-Basis. Es handelt sich dabei um eine Mischung von mRNAs, die für 19 Speichelproteine (19ISP) der Zecke I. scapularis kodieren. Die Vakzine richtet sich also nicht gegen B. burgdorferi selbst, sondern gegen Bestandteile des Zeckenspeichels.
- VLA15 ist ein multivalenter Proteinimpfstoff, der als Antigen rekombinant hergestellte Antikörper gegen das äußere Oberflächenprotein A (OspA) von den sechs in Europa und den Vereinigten Staaten verbreiteten Borrelia-Serotypen enthält. Sticht eine Zecke eine geimpfte Person, nimmt sie Blut mit OspA-Antikörpern auf. Die Antikörper lassen die Borrelien absterben, bevor sie in den Wirt gelangen. Der Impfstoff soll 2025 zugelassen werden.
- mRNA-1982 und mRNA-1975 sind experimentelle Vakzinen, die den Körper anregen sollen, Antikörper herzustellen, die spezifisch für B. burgdorferi sind.
Meldepflicht
Es besteht keine einheitliche Meldepflicht laut IfSG.
- Arztmeldepflicht:
- namentlich bei Erkrankungs- und Todesfällen: Berlin, Brandenburg, Sachsen, Thüringen
- nicht namentlich bei Erkrankungs- und Todesfällen: Mecklenburg-Vorpommern
- nicht namentlich bei Erythema migrans, akuter Neuroborreliose oder akuten Lyme-Arthritis: Bayern, Rheinland-Pfalz, Saarland
- Labormeldepflicht:
- namentlich bei Erregernachweis: Berlin, Brandenburg, Sachsen
- nicht namentlich bei Erregernachweis: Mecklenburg-Vorpommern
- nicht namentlich bei Erregernachweis, falls Hinweise auf akute Infektion vorliegen: Sachsen-Anhalt
Prognose
Insgesamt kann bei der Mehrzahl der Patienten eine Heilung mit allenfalls geringen Residuen erzielt werden. Selbst eine spätere Therapie hat noch eine gute Prognose, wobei sich der Heilungsprozess verzögern kann. Bei einer Neuroborreliose kommt es in 75 % der Fällen zur kompletten Remission.
Eine erneute Infektion mit B. burgdorferi sensu lato kann auftreten. Bei Patienten, die wegen eines Erythema migrans behandelt wurden, reicht die Immunantwort nicht aus, um vor einer erneuten Infektion zu schützen. Bei Patienten zum Beispiel mit einer Lyme-Arthritis scheinen über Jahre vor erneuten Infektionen geschützt zu sein.
Literatur
- Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF): S3-Leitlinie Neuroborreliose, abgerufen am 15.07.2019
- Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) S2k-Leitlinie „Kutane Lyme-Borreliose“. 2016, abgerufen am 15.07.2019
- Deutsche Borreliose-Gesellschaft e.V. Diagnostik und Therapie der Lyme-Borreliose. 2011, abgerufen am 15.07.2019
- RKI Ratgeber April 2019, abgerufen am 15.07.2019
- Steiner F, Suttorp N. 210 Lyme-Borreliose. In: Suttorp N, Möckel M, Siegmund B et al., Hrsg. Harrisons Innere Medizin. 19. Auflage. Berlin: ABW Wissenschaftsverlag; 2016.
- Klinische Leitlinie Neuroborreliose, Rauer S, Kastenbauer S, Fingerle V, Hunfeld KP, Huppertz HI, Dersch R: Dtsch Arztebl Int 2018; 115: 751–6, abgerufen 31.5.2019
- Laborlexikon: Borreliendiagnostik
- Nau, R. et al.: Lyme-Borreliose – aktueller Kenntnisstand (Dtsch Arztebl Int 2009; 106(5): 72-81; DOI: 10.3238/arztebl.2009.0072)
- Pfister, H.-W.: Diagnostik und Behandlung der Neuroborreliose. Was nötig ist und was Sie sich sparen können. MMW Fortschr. Med. 2010; 152(25-27): 31-35.
- Schuster, N.: Auf die Zecken, fertig, los, DocCheck News, 22.6.2023
Quiz
Bildquelle
- Bildquelle für Flexikon-Quiz: © Erik Karits / Unsplash
Quellen
- ↑ Wilking et al., Antibodies against Borrelia burgdorferi sensu lato among adults, Germany, 2008-2001, Emerging Infectious Diseases, 2015
- ↑ Lantos et al., 2020 Guidelines for the Prevention, Diagnosis and Treatment of Lyme Disease, Clinical Infectious Diseases, 2021,