Magen
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonyme: Ventriculus, Gaster
Englisch: stomach
Definition
Anatomie
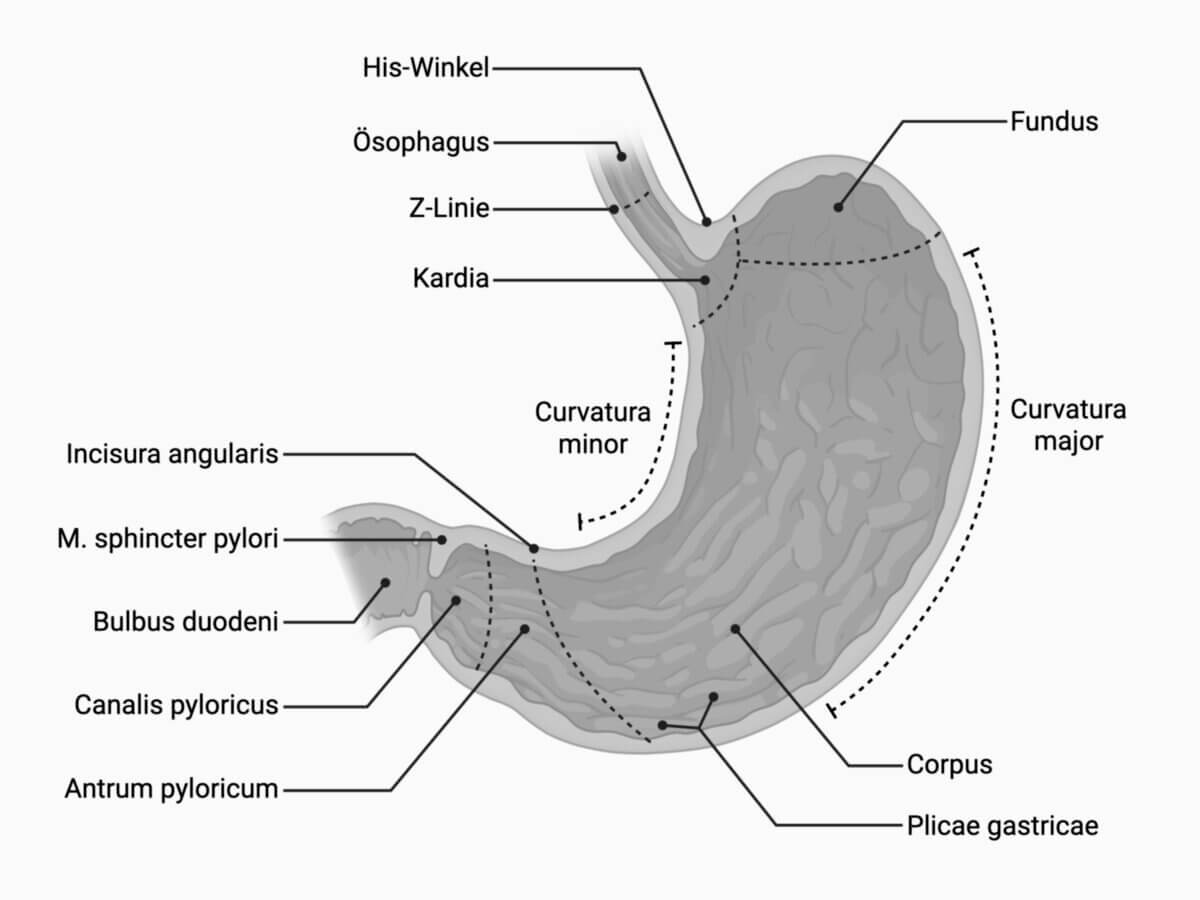
Form
Der Magen ist ein schlauch- bis sackförmiges Hohlorgan, das sich im linken oberen Quadranten des Abdomens kurz unterhalb des Diaphragma befindet. Beim Mensch liegt er als einhöhliger Magen vor. Der Magen besitzt eine Vorderwand (Pars anterior) und eine Hinterwand (Pars posterior). Durch seine gebogene Form weist er eine konvexe, nach links gerichtete, und eine konkave, nach rechts und kranial weisende Magenkurvatur auf:
- Curvatura gastrica major (größere Magenkurvatur)
- Curvatura gastrica minor (kleinere Magenkurvatur)
Einteilung
Die Einteilung des Magens erfolgt in vier Abschnitte, die eine unterschiedliche Histologie und Funktion aufweisen. Man unterscheidet:
- Pars cardiaca ventriculi oder Kardia: der kurze, nach oral hin gelegene Abschnitt mit der Einmündung des Ösophagus in den Magen (Ostium cardiacum)
- Fundus ventriculi oder Fundus: der links neben der Kardia gelegene und nach oben gewölbte Abschnitt. Die Kuppel des Fundus wird als Fornix gastricus bezeichnet. Hier sammelt sich Luft in Form der Magenblase.
- Corpus ventriculi oder Korpus: der zentral gelegene Magenkörper, der den Hauptteil des Organs ausmacht
- Pars pylorica ventriculi: das Endteil des Magens mit dem Antrum pyloricum, dem Canalis pyloricus ("Pars praepylorica") und dem Pylorus. Letzterer steht über das Ostium pyloricum mit der Pars superior duodeni in Verbindung.
An der kleinen Kurvatur ist der Beginn der Pars pylorica durch die Incisura angularis gastris markiert.
Topographie
Der Magen liegt intraperitoneal, als entwicklungsgeschichtliches Relikt weist er zwei Mesogastrien (Mesenterien) auf, die sich als Omentum majus bzw. minus sowie als Verbindungszüge zwischen Magen und benachbarten Organen weiterentwickeln und die Bursa omentalis einschliessen.
Die Kardia liegt auf Höhe des 10.-12. Brustwirbels, der Pylorus auf Höhe des 1. und 2. Lendenwirbels.
Der Magen wird vorne z.T. vom linken Leberlappen überlagert. Zwischen dem Leberrand und dem linken Rippenbogen liegt der Magen vorne der Bauchwand direkt an (Magenfeld). Die Hinterwand des Magens grenzt an die Bursa omentalis und gleitet z.T. auf der Vorderfläche des Pankreas und dem Mesocolon transversum.
Peritonealbezüge des Magens
Im Omentum majus befinden sich verstärkte Faserzüge, die den Magen mit anderen Strukturen verbinden:
- Ligamentum gastrosplenicum: stellt die peritoneale Verbindung zwischen Curvatura gastrica major und dem Milzhilus dar. Begrenzt nach links die Bursa omentalis.
- Ligamentum gastrophrenicum: Verbindung zwischen Magen und Diaphragma. Teil des Omentum majus.
- Ligamentum gastrocolicum: Verbindung zwischen Curvatura gastrica major und Taenia omentalis des Colon transversum. Begrenzt nach ventral die Bursa omentalis.
Das Ligamentum hepatogastricum ist ein kranialer Teil des Omentum minus zwischen Curvatura gastrica minor und der Leberpforte.
Magenlumen
Die Magenschleimhaut ist makroskopisch in Falten aufgeworfen. Diese Plicae gastricae verlaufen im Bereich der kleinen Kurvatur fast parallel zur Längsrichtung des Korpus und bilden hier die sog. Waldeyer-Magenstraße. Im Bereich der großen Kurvatur verlaufen die Falten unregelmäßig.
Der Querschnitt des leeren Magens ist im kontrahierten Zustand rund, im erschlafften Zustand liegen Vorder- und Hinterwand aufeinander. Das maximale Fassungsvermögen ist individuell verschieden und beträgt beim Erwachsenen ca. 1,5 l.
Arterielle Versorgung
Die arterielle Versorgung des Magens erfolgt über mehrere Blutgefäße, die alle aus dem Truncus coeliacus entspringen, untereinander anastomosieren und so Gefäßarkaden entlang der kleinen und der großen Kurvatur bilden.
Die Gefäßarkade an der kleinen Kurvatur wird gebildet von:
- Arteria gastrica sinistra: entspringt direkt aus dem Truncus coeliacus, zieht in der Plica gastropancreactica zum Magen und gelangt in der Nähe der Kardia an die kleine Kurvatur. Sie gibt aufsteigende Rami oesophagei und Äste für die Hinter- und Vorderwand des Magens ab und verbindet sich mit der rechten Arteria gastrica.
- Arteria gastrica dextra: entspringt i.d.R. aus der Arteria hepatica propria, in ungefähr einem Drittel der Fälle aus der Arteria hepatica communis.
Die Gefäßarkade an der großen Kurvatur wird gebildet von:
- Arteria gastroomentalis sinistra: entspringt aus dem distalen Teil der Arteria splenica, verläuft im Ligamentum gastrocolicum zur großen Kurvatur. Sie gibt Rami gastrici an die Vorder- und Hinterfläche des Magens sowie Rami omentales zum Omentum majus ab und verbindet sich dann mit der rechten Arteria gastroomentalis.
- Arteria gastroomentalis dextra: entstammt der Arteria gastroduodenalis, gelangt im Ligamentum gastrocolicum an die große Kurvatur und gibt Rami gastrici und Rami omentales ab.
- Arteriae gastricae breves: entspringen der Arteria splenica am Milzhilus, verläufen durch das Ligamentum gastrosplenicum zum Fundus und versorgen die Hinterwand.
- Arteria gastrica posterior: inkonstantes Gefäß aus der Arteria splenica. Versorgt die Rückwand des Magens.
Die Arterien durchbrechen nach Abgabe feiner Äste an einen Plexus subserosus die Muskelschicht und verzweigen sich in der Submukosa zu einem dichten Plexus submucosus.
Venöse Drainage
Das venöse Blut der Magenwand sammelt sich in den gleichnamigen Venen, die mit den Arterien verlaufen:
- Vena gastrica dextra und sinistra entlang der kleinen Kurvatur
- Vena gastroomentalis dextra und Vena gastroomentalis sinistra entlang der großen Kurvatur
Der durch die Venae gastricae dextra et sinistra und durch eine Vena praepylorica gebildete Gefäßbogen entlang der kleinen Kurvatur wird auch als Vena coronaria ventriculi ("Kranzvene") bezeichnet.
Die Magenvenen verlaufen z.T. direkt, teils über die Vena splenica und Vena mesenterica superior in die Vena portae. Am Übergang von Ösophagus und Magen sind einige Venen mit den Venae oesophageales verbunden, die zur Vena azygos bzw. Vena hemiazygos ziehen. Durch diese Venen sind das portale und das kavale Kreislaufgebiet verbunden (portokavale Anastomose).
Lymphgefäße
Im Magen unterscheidet man drei Lymphabflussgebiete, deren Grenzen sich jedoch überlappen:
- Die Lymphe der Kardia und eines Großteils der Vorder- und Hinterwand im Bereich der kleinen Kurvatur wird über Lymphknoten geleitet, die entlang der kleinen Kurvatur an der Kardia liegen. Die drainierenden Lymphgefäße verlaufen entlang der Arteria gastrica sinistra zu den Nodi lymphatici coeliaci und anschließend in den Truncus intestinalis oder den Truncus lumbalis.
- Die Lymphe aus den linken Teilen des Fundus und angrenzenden Abschnitten des Korpus gelangt über Nodi lymphatici splenici am Milzhilus und über Lymphknoten entlang der Arteria splenica ebenfalls zu den Nodi lymphatici coeliaci.
- Die Lymphe der unteren zwei Drittel der großen Kurvatur und des Pylorus sammelt sich in Nodi lymphatici pylorici und Knoten entlang der großen Kurvatur. Die Knoten am Pylorus werden über Bahnen entlang der Arteria hepatica communis (Nodi lymphatici hepatici) zu den Nodi lymphatici coeliaci abgeleitet. Ein Teil der Knoten entlang der großen Kurvatur kann auch über Verbindungen entlang der Vena gastroomentalis dextra zu kaudal vom Pankreas liegenden Lymphknoten ziehen, die zur Gruppe der Nodi lymphatici mesenterici gezählt werden.
Innervation
Wie andere Teile des Verdauungstrakts, besitzt auch der Magen ein autonom funktionierendes Nervensystem (enterisches Nervensystem). Die selbstständige Tätigkeit des Magens wird durch vegetative Nervenfasern moduliert:
Parasympathische Fasern
Die parasympathischen Fasern für den Magen stammen aus dem Truncus vagalis anterior und Truncus vagalis posterior. Die Trunci gehen an der Vorder- bzw. Hinterseite des Ösophagus aus dem Plexus oesophageus des Nervus vagus hervor. Der Truncus vagalis anterior erhält v.a. Fasern aus dem linken, der Truncus vagalis posterior aus dem rechten Nervus vagus. In den parasympathischen Nerven verlaufen auch viszeroafferente Fasern.
Häufig verlassen schon direkt nach dem Durchtritt durch das Zwerchfell (Hiatus oesophageus) einige kleinere Äste (Rami pylorici) die Trunci vagales, um zum Pylorus zu ziehen. Auf dem Weg dorthin verlaufen sie zunächst mit den Rami hepatici in Richtung der Leberpforte, um dann im Omentum minus nach kaudal laufend den Pylorus zu erreichen.
Wird der Parasympathikus aktiviert, führt dies zu einer Steigerung der Magenmotorik (Peristaltik) und -sekretion sowie zu einer Erweiterung der Gefäße (Vasodilatation).
Sympathische Innervation
Die sympathischen Nerven stammen aus dem Plexus coeliacus und verlaufen entlang der gastralen Blutgefäße. Die Perikaryen der präganglionären Fasern liegen im Seitenhorn der Rückenmarkssegmente Th5 bis Th9. Über den Grenzstrang gelangen die Fasern in die Nervi splanchnici und werden im Ganglion coeliacum auf postganglionäre Neurone umgeschaltet.
Eine Sympathikusaktivierung führt zu einer Hemmung der Magenmotorik und verringert die Magensekretion. Zusätzlich bewirkt sie eine Vasokonstriktion. In den sympathischen Nerven verlaufen auch afferente Fasern, v.a. Schmerzfasern. Ihre Perikaryen liegen in den Spinalganglien der Segmente Th5 bis Th9.
Sensible Innervation
Die sensible Innervation des Magens erfolgt über den linken Nervus phrenicus.
Präparat
Histologie
Der Magen weist schematisch denselben Wandaufbau auf wie alle Abschnitte des Gastrointestinaltraktes. Man unterscheidet zwischen:
- Tunica mucosa: Magenschleimhaut
- Tela submucosa: submuköse Bindegewebeschicht
- Tunica muscularis: dreilagige, gewunden verlaufende Muskelschicht
- Tela subserosa
- Tunica serosa
Tunica mucosa
Die Magenschleimhaut ist ca. 1-2 mm dick, enthält tubulöse Magendrüsen (Glandulae gastricae) und besteht aus:
Die Plicae gastricae der Magenschleimhaut entstehen durch Ausstülpungen der darunterliegenden Tela submucosa. Dabei handelt es sich um fixe Strukturen unabhängig von Füllungszustand und Peristaltik. Lichtmikroskopisch erkennt man eine Felderung der Schleimhautoberfläche. Die einzelnen Felder (Areae gastricae) besitzen einen Duchmesser von ca. 1-2 cm. Die Einziehungen an den Grenzen der Areae entstehen duch Züge glatter Muskulatur, die senkrecht zur Lamina muscularis mucosae verlaufen. Auf den Areae gastricae münden die Magengrübchen (Foveolae gastricae).
Oberflächenepithel
Die Lamina epithelialis ist ein einfaches Säulenepithel und kleidet auch die Foveolae gastricae aus. Der apikale Bereich der Zellen enthält Schleimgranula, die fucosereiche Muzine (v.a. MUC5AC) enthalten und mittels PAS-Reaktion darstellbar sind. Die Fucosereste der sezernierten Muzine verleihen dem Schleim Blutgruppeneigenschaften (AB0-System) und erhöhen den Viskositätsgrad des Schleims durch hydrophobe Wechselwirkungen. Gleichzeitig sezernieren die Zellen Proteine, welche die Muzine miteinander quervernetzen und so die Muzinschicht stabilisieren (z.B. TFF1). Die Epithelzellen bilden durch die Sekretion der Muzine die tiefe Schicht der 0,02 bis 0,2 mm dicken Schleimschicht, die die Tunica mucosa vor Andauung durch den Magensaft schützt. Die oberflächliche Lage der Schleimschicht besteht v.a. aus MUC6 aus den Nebenzellen der Hauptdrüsen (siehe unten).
Weiterhin sezernieren die Epithelzellen Bikarbonationen und puffern somit Protonen an der Epitheloberfläche ab. Außerdem bilden sie Phospholipide, die eine hydrophobe oberflächliche Lage auf der Schleimschicht bilden (Barrierefunktion). Die Sekretion von Muzinen und Bikarbonat wird durch Prostaglandin E2 stimuliert, das von Epithelzellen selbst (autokrin) und von Stromazellen der Lamina propria gebildet wird.
Verstreut im Epithel der Oberfläche und Foveolae befinden sich Bürstenzellen mit langen, steifen Mikrovilli, die in den Magenschleim ragen. Sie besitzen Chemorezeptorfunktion, enthalten α-Gustducin sowie Enzyme, die Stickoxid (NO) produzieren. NO stiuliert u.a. die Muzin- und Bikarbonatsekretion des Oberflächenepithels.
Magendrüsen
Vom Grund der Fovaeolae gastricae gehen die langen, verzweigten, tubulösen Magendrüsen aus. Man unterscheidet:
- Kardiadrüsen (Glandulae cardiacae): am Obergang zum Ösophagus besitzt die Kardia einen schmalen Streifen mit tubulösen, z.T. zystisch aufgetriebenen, mukösen Drüsen, die Schleim und Lysozym sezernieren.
- Hauptdrüsen (Glandulae gastricae propriae): Fundusdrüsen und Drüsen im Corpus ventriculi
- Pylorusdrüsen (Glandulae pyloricae): muköse Drüsen. Die Zellen entsprechen denen der Kardiadrüsen und den Nebenzellen der Hauptdrüsen. Sie produzieren einen schwach sauren Schleim. In der Lamina propria und Submukosa des Pylorus kommen Lymphfollikel vor.
Die Hauptdrüsen sind 1,5 mm lange, mäßig verzweigte tubulöse Drüsen, die bis zur Lamina muscularis mucosae reichen. Man unterscheidet drei Abschnitte:
- Isthmus: Übergang zwischen Foveola und Drüsenschlauch; enthält multipotente Stammzellen
- Halsteil (Cervix)
- Hauptteil (Pars principalis): endet im Drüsengrund (Fundus)
In den Hauptdrüsen findet man drei verschiedene Zelltypen, die durch dichte Zonulae occludentes sowie Desmosomen und Nexus verbunden sind:
- Nebenzellen: produzieren Muzine und sind v.a. im Isthmus und Cervix lokalisiert.
- Hauptzellen: bilden Pepsinogen und befinden sich v.a. im Hauptteil
- Parietalzellen (auch Belegzellen genannt): produzieren Salzsäure und kommen in allen Abschnitten vor (v.a. im Halsteil)
| Merkhilfe |
|---|
| "Die Belegschaft ist sauer, weil die Nebenschaft schleimt und die Hauptschaft Pepsi trinkt." (Belegzellen → Salzsäure, Nebenzellen → Schleim, Hauptzellen → Pepsinogen) |
Nebenzellen
Die Nebenzellen sind meist zwischen benachbarten Parietalzellen dreieckig eingekeilt und besitzen große Sekretgranula mit Muzinen (v.a. MUC6). Die enthaltenden sulfatierten N-Acetylglucosamin-Moleküle bewirken eine schwache bis mäßige Basophilie der Zellen. Weiterhin sind sie über eine mäßig positive PAS-Reaktion darstellbar.
Außer MUC6 sezernieren Nebenzellen auch Lysozym und TFF2.
Parietalzellen
Die großen, pyramidenförmigen Parietalzellen buckeln sich in die Lamina propria vor. Meist ist der schmale luminale Zellpol nicht angeschnitten, sodass sie wie von außen aufgelegt erscheinen. Sie enthalten viele Mitochondrien und sind daher azidophil anfärbbar. Ihre apikale Oberfläche ist über Mikrovilli und tiefe Einstülpungen (sekretorische Canaliculi) vergrößert.
Parietalzellen besitzen eine Protonen-Kalium-Pumpe, die unter ATP-Verbrauch Kaliumionen gegen Protonen in das Drüsenlumen transportiert. Für die abgegebenen Protonen bleiben Hydroxid-Ionen in der Zelle zurück, die sich mit Kohlendioxid zu Bikarbonationen vereinigen (membranständige Carboanhydrase). Die Bikarbonationen verlassen die Zelle über die basolaterale Membran mittels Bikarbonat-Chlorid-Antiporter (Anionen-Austauscher 2). Die in die Zellen transportierten Chloridionen gehen mit Hilfe eines Chlorid-Kanals passiv in den Magensaft über, sodass zusammen mit den Protonen Salzsäure entsteht.
Die Parietalzellen sind in der Lage, die Protonen-Kalium-Pumpen durch Verlagerung in intrazelluläre Vesikel zu speichern und durch Stimuli wieder in die Zellmembran einzubauen. Trigger sind Acetylcholin aus cholinergen Fasern des mukösen Nervenplexus sowie Histamin aus ECL-Zellen der Drüsen und aus Mastzellen. Gastrin aus G-Zellen (v.a. im Pylorus und Duodenum) gelangt über die Blutbahn in die Magenschleimhaut und stimuliert die Freisetzung von Histamin aus ECL-Zellen.
Neben Salzsäure sezernieren Parietalzellen noch den Intrinsischen Faktor, der für die Resorption von Cobalamin (Vitamin B12) im Ileum benötigt wird.
Hauptzellen
Die säulenförmigen Hauptzellen bilden:
- Pepsinogene
- Gastricin: im Säuglingsalter für die Verdauung von Milcheiweiß
- Magenlipase: spaltet 10-30 % der aufgenommenen Neutralfette
Die Pepsinogene werden in großen, apikalen Sekretgranula verpackt. Je nach Fixierung ist der Inhalt basophil bzw. elektronendicht oder ausgewaschen. Die basale Basophilie beruht auf dem ausgeprägten rauen endoplasmatischen Retikulum. Die Sekretion von Pepsinogen wird v.a. durch Acetylcholin und Gastrin ausgelöst. Weiterhin stimulieren Protonen im Lumen die Sekretion. Pepsinogene werden in die aktiven Pepsine gespalten. Diese Reaktion wird durch Pepsin selbst bei einem pH-Wert von unter 5 katalysiert.
Endokrine Zellen
Im Antrum und Pylorus kommen endokrine Zellen häufig vor, insbesondere im basalen Drittel der Drüsen. Hier dominieren:
- G-Zellen: bilden Gastrin
- D-Zellen: sezernieren Somatostatin
- EC-Zellen: sezernieren Serotonin
In der Fundus- und Korpusregion sind endokrine Zellen gleichmäßig im Epithel der Hauptdrüsen verteilt. Der häufigste Zelltyp ist die Histamin-sezernierende ECL-Zelle. Außerdem kommen auch hier D-Zellen vor.
Tunica muscularis
Die Tunica muscularis des Magens enthält ein außen gelegenes Stratum longitudinale, das die Fortsetzung der Längsmuskelschicht des Ösophagus bildet. Die Muskelbündel verlaufen in Längsrichtung und sind v.a. im Bereich der Kurvaturen kräftig ausgebildet.
Die nach innen folgende Ringmuskelschicht (Stratum circulare) ist in allen Bereichen des Magens gut entwickelt und am Pylorus zu einem Schließmuskel (Musculus sphincter pylori) verdickt.
Angrenzend an die Tela submucosa kommen schräg verlaufende Muskelzüge vor (Fibrae obliquae), die kranial das Ostium cardiacum umschlingen und bei der Ausbildung der Incisura cardiaca (His-Winkel) eine Rolle spielen. Von dort verlaufen sie schräg nach aboral und lassen dabei die kleine Kurvatur frei. Im unteren Korpusbereich biegen sie zur großen Kurvatur um und strahlen in die Ringmuskulatur ein.
Embryologie
Die Entwicklung des Magens beginnt etwa ab der 5. Embryonalwoche mit einer kleinen spindelförmigen Erweiterung des Vorderdarms, der sich zuvor aus dem primitiven Darmkanal entwickelt hat. Durch stärkeres Wachstum der dorsalen Anteile kommt es zu einer Krümmung der Magenanlage mit Ausbildung einer kleinen und großen Kurvatur. Die anschließende Drehung des Magens um 90 Grad im Uhrzeigersinn verlagert die große Kurvatur nach links.
siehe Hauptartikel: Embryonale Magenentwicklung
Physiologie
Der Magen erfüllt im Wesentlichen folgende Aufgaben:
- Zwischenspeicher der Nahrung mit portionsweiser Abgabe durch den Pylorus in das Duodenum
- Ausbereitung der Nahrung durch Denaturierung, Zerkleinerung und partieller Verdauung von Proteinen und Fetten
- Abtötung von Krankheitserregern durch die Salzsäure
- Bildung des intrinsischen Faktors für die Resorption von Cobalamin
Magenmotorik
Bezüglich der Magenmotorik kann man den Magen in zwei Abschnitte einteilen:
- oraler Abschnitt: Kardia, Fundus, obere zwei Drittel des Korpus
- aboraler Abschnitt: unterer Korpusdrittel, Pars pylorica
Die Muskulatur der Kardia befindet sich in einem Dauertonus, der einen Verschluss gegen den Ösophagus ermöglicht. Eine Öffnung des Ostium cardiacum wird v.a. durch die Peristaltik des Ösophagus ermöglicht. Der restliche orale Abschnitt unterliegt einem Ruhetonus unterschiedlicher Stärke, je nach Füllungszustand des Magens. Die tonische Umschließung des Magens wird als Peristole bezeichnet.
Der aborale Abschnitt besitzt eine phasische Aktivität, die peristaltische Wellen erzeugt. Diese gehen vom unteren Korpus aus und berlaufen über das Antrum zum Pylorus. Tief einschneidende Kontraktionsringe wandern pyloruswärts und schieben den Mageninhalt (Chymus) vor sich her. Jede Kontraktionswelle dauert bis zu 20 Sekunden, die maximale Fequenz beträgt drei Kontraktionen pro Minute. Abhängig vom aufgebauten intraluminalen Druck und vom Tonus des Pylorus wird somit der Chymus durch das Ostium pyloricum in das Duodenum befördert (Propulsion). Ein Großteil des Mageninhalts schwappt dabei zurück (Retropulsion), sodass der Speisebrei durchmischt und mechanisch zerkleinert wird. Die Durchmischung des Chymus bewirkt eine Emulgierung der in der Nahrung erhaltenen Fette und optimiert die weitere Fettverdauung.
Nach Durchlass einer Portion des Chymus wird der Pylorus verschlossen, bis der in den Darm gelangte saure Mageninhalt neutralisiert ist.
Die Peristaltik steuern Schrittmacherpotenziale der Muskulatur im mittleren Korpusbereich. An deren Generierung sind interstitielle Cajalzellen (ICC) beteiligt. Die Amplitude und Frequenz der Potenziale werden vom Nevus vagus vermindert; die Frequenz durch Gastrin erhöht. Weiterhin wird die Motorik durch Dehnungsrezeptoren gesteuert. Die sog. Intramuscular Arrays (IMA) bestehen aus gebündelten afferenten Vagusterminalen, die in Kontakt mit Muskelzellen und ICCs stehen. Andere Dehnungsrezeptoren werden durch Neuronen des Plexus myentericus gebildet.
Vorverdauung
Der Magen übernimmt einen wichtigen Teil der Verdauung von Proteinen und Fetten und unterliegt dabei in seiner sekretorischen und mechanischen Funktion einer komplexen endokrinen Regulation. Über eine Ansäuerung des Speisebreis mit Magensäure und eine Versetzung mit Pepsin und Kathepsin wird eine erste Aufschließung der Proteine vorgenommen. Sie führt zu einer Denaturierung bzw. Quellung der Eiweiße und ihrer Aufspaltung in kleinere Polypeptid-Fragmente.
Enzymatisch wird die Fettverdaung durch die im sauren Bereich aktive Magenlipase unterstützt. Die Kohlenhydratverdauung hingegen sistiert im Magen, da die Aktivität der Alpha-Amylase durch den sauren Magen-pH gestoppt wird.
Magensaft
Der Magensaft besteht aus dem Sekret der Parietalzellen (Salzsäure) und aus anderen Zellen des Magens (Muzine, Pepsinogene, Lipase). Es handelt sich um eine leicht trübe, schleimige, fast farblose Flüssigkeit, die meist durch Gallenrückfluss grünlich verfärbt ist. Täglich werden 2-3 Liter sezerniert. Der mittlere pH-Wert beträgt 2 bis 2,5. Die Sekretion der Parietalzellen kann um das 10fache gesteigert werden.
In Erwartung einer Mahlzeit (Riechen, Vorstellung) wird die Sekretion der Magendrüsen zentralnervös über den Nervus vagus stimuliert (kephale Phase). Seine viszeroefferenten Fasern stimulieren die Parietalzellen und Hauptzellen der Hauptdrüsen sowie indirekt die G-Zellen im Pylorus über intramurale Neurone, die Gastrin Releasing Peptide (GRP) freisetzen.
In der anschließenden gastralen Phase bewirkt der Eintritt der Speisen in den Magen eine Dehnung der Wand sowie eine pH-Erhöhung. Die Magendehnung führt zur Aktivierung von Mechanorezeptoren und zur Stimulation von vagalen und intramuralen Reflexen. Neben der Gastrinausschüttung werden auch ECL-Zellen der Hauptdrüsen zur Histaminsekretion angeregt. Die Stimulation der ECL-Zellen erfolgt über Gastrin (CCK2-Rezeptor) sowie indirekt durch cholinerge Hemmung der D-Zellen. D-Zellen hemmen Parietalzellen und ECL-Zellen durch Freisetzung von Somatostatin. Histamin stimuliert Parietalzellen zur Salzsäureproduktion (H2-Rezeptor) und hemmt D-Zellen (H3-Rezeptor). Weiterhin wird Gastrin als Reaktion auf Peptide und bestimmte Aminosäuren, alkoholische Getränke und Kaffee freigesetzt. Außerdem stimuliert Gastrin die Sekretion des Intrinsischen Faktors und des Pepsinogens. Es bewirkt auch eine Hyperplasie der Parietalzellen. Somatostatin wird v.a. durch luminale pH-Erniedrigung freigesetzt.
Sobald der saure Mageninhalt in das Duodenum gelangt, beginnt die intestinale Phase. Verschiedene Mechanismen führen dann zur Hemmung der Säuresekretion:
Die Ausschüttung von Sekretin aus S-Zellen des Duodenums stimuliert die Bikarbonatsekretion des Pankreas und bewirkt so eine schnelle Neutralisation des sauren Magenbreis. Die Sekretion von Cholecystokinin aus I-Zellen des Duodenums aktiviert inhibitorische Neuronen des Plexus myentericus des Magens, sodass die Magenperistaltik abnimmt.
Klinik
Der Magen fällt in den Arbeitsbereich der Gastroenterologie. Häufige Magenerkrankungen sind u.a.:
Als wichtigste Untersuchungsmethode hat sich die Gastroskopie mit flexiblen Endoskopen etabliert, bei der im gleichen Untersuchungsgang als Ösophagogastroduodenoskopie (ÖGD) auch der Ösophagus und das Duodenum mit untersucht werden. Sie ermöglicht die direkte Beurteilung der Magenschleimhaut und das Aufspüren von malignen Veränderungen mit anschließender Entnahme einer Biopsie. Durch funktionsdiagnostische Verfahren wie die pH-Metrie lassen sich Sekretionsstörungen des Magens nachweisen.
Podcast

Trivia
Magenknurren entsteht, wenn sich bei leerem Magen der Inhalt mit Luft vermischt und durch die Peristaltik in Schwingung gebracht wird.
Literatur
- Anderhuber et al., Waldeyer - Anatomie des Menschen: Lehrbuch und Atlas in einem Band (19. aktualisierte Auflage), De Gruyter, 2012
- Fritsch et al., Taschenatlas der Anatomie, Band 2: Innere Organe: Mit Online-Zugang (12. aktualisierte Auflage), Thieme Verlag, 2018
- Aumüller et al., Duale Reihe Anatomie: Mit Online-Zugang (5. aktualisierte Auflage), Thieme Verlag, 2020
Bildquelle
- Bildquelle Podcast: ©Dan Burton / Unsplash
- Präparat freundlicherweise zur Verfügung gestellt durch die Anatomie der Uni Köln