Mammakarzinom
Synonym: Brustkrebs
Englisch: breast cancer, carcinoma of the breast
Definition
Das Mammakarzinom ist eine maligne Neoplasie, die von den Epithelzellen der Brustdrüse ausgeht. Es ist die häufigste Krebserkrankung der Frau und tritt selten auch beim Mann auf.
- ICD10-Code: C50.- Bösartige Neubildung der Brustdrüse
Epidemiologie
Frauen
Das Mammakarzinom ist die häufigste maligne Tumorerkrankung der Frau in Deutschland. Die altersstandardisierte Inzidenz des Mammakarzinoms bei Frauen in Deutschland liegt bei etwa 150 Neuerkrankungen pro 100 000 Frauen pro Jahr. Jährlich werden rund 74.000–75.000 Neuerkrankungen diagnostiziert. Das Lebenszeitrisiko für eine Frau, im Laufe ihres Lebens an einem Mammakarzinom zu erkranken, beträgt etwa 12–13 %, entsprechend etwa 1 von 8 Frauen. Das mittlere Erkrankungsalter liegt bei etwa 64–65 Jahren. Mammakarzinome treten am häufigsten zwischen der 6. und 7. Lebensdekade auf. Erkrankungen vor dem 35. Lebensjahr sind selten.
Männer
Auch Männer können an einem Mammakarzinom erkranken, jedoch deutlich seltener als Frauen. Das Verhältnis der Neuerkrankungen (Männer : Frauen) beträgt etwa 1:100. In Deutschland werden pro Jahr etwa 700–800 Neuerkrankungen bei Männern diagnostiziert. Die altersstandardisierte Inzidenz liegt bei etwa 1,7–1,8 Neuerkrankungen pro 100.000 Männer pro Jahr. Das Lebenszeitrisiko für Männer, im Laufe ihres Lebens an einem Mammakarzinom zu erkranken, liegt bei etwa 0,1 %. Das Erkrankungsalter liegt im Mittel etwas höher als bei Frauen.
Risikofaktoren
Die Risikofaktoren für die Entstehung von Brustkrebs sind bisher (2026) noch nicht vollständig geklärt. Es gibt jedoch eine Reihe von Faktoren, die hinsichtlich ihrer Mitwirkung gut untersucht und epidemiologisch gesichert sind. Das Alter ist der wichtigste Risikofaktor. Mit zunehmendem Lebensalter steigt das Risiko kontinuierlich an. Ein deutlicher Inzidenzanstieg zeigt sich ab dem mittleren Erwachsenenalter. Frauen, bei denen die Menarche vor dem 12. Lebensjahr oder die Menopause nach dem 55. Lebensjahr auftritt, haben ein erhöhtes Risiko. Ebenso ist eine späte erste Schwangerschaft oder Nulliparität mit einem erhöhten Risiko assoziiert. Frauen, die vor ihrem 20. Lebensjahr gebären, haben gegenüber später gebärenden oder nicht gebärenden Frauen ein erniedrigtes Brustkrebsrisiko. Ein erhöhtes Risiko besteht außerdem bei:
- vorherigem Mammakarzinom der kontralateralen Brust
- vorherigem Carcinoma in situ (DCIS oder LCIS)
- Brustkrebs bei Verwandten ersten Grades, insbesondere bei Erkrankung in jungem Alter
Ergänzend ist eine hohe mammographische Brustdichte als unabhängiger Risikofaktor etabliert.
Genetische Faktoren
Etwa 5–10 % der Mammakarzinome sind auf pathogene Keimbahnmutationen zurückzuführen, überwiegend in hochpenetranten Genen. Am häufigsten liegen Keimbahnmutationen in den Genen BRCA1 auf Chromosom 17 oder BRCA2 auf Chromosom 13 vor. Die kodierten Proteine spielen zusammen mit Rad51 eine zentrale Rolle in der homologen DNA-Reparatur. Ein Funktionsverlust führt zu einer verminderten Reparatur von DNA-Doppelstrangbrüchen und erhöht damit die Wahrscheinlichkeit einer Tumorentstehung. Trägerinnen pathogener BRCA1- oder BRCA2-Mutationen haben ein kumulatives Lebenszeitrisiko von etwa 60–75 %, bis zum 80. Lebensjahr an einem Mammakarzinom zu erkranken. Bei sporadischen Mammakarzinomen können ebenfalls Störungen des BRCA-vermittelten DNA-Reparatursystems vorliegen. Diese beruhen jedoch in der Regel nicht auf Keimbahnmutationen, sondern auf somatischen genetischen oder epigenetischen Veränderungen. Eine allgemeine Rolle als individueller Risikofaktor ist hieraus nicht ableitbar.
Neben BRCA1 und BRCA2 gibt es weitere, seltene Gene, deren Mutation (Protein-truncating variants) mit einem signifikant erhöhten Mammakarzinomrisiko einhergeht. Sie kodieren für:[1]
- Serin-Proteinkinase ATM (ATM)
- Checkpoint-Kinase 2 (CHEK2)
- Partner and Localizer of BRCA2 (PALB2)
- TP53
- RAD51C
- RAD51D
- BARD1
- PTEN
Diese Gene kodieren überwiegend für Proteine der DNA-Reparatur und Zellzykluskontrolle.
Familiäres Mammakarzinom
Eine genetische Beratung und ggf. molekulargenetische Testung sollte angeboten werden, wenn die Wahrscheinlichkeit für das Vorliegen einer pathogenen Keimbahnmutation ≥ 10 % beträgt. Die Risikobewertung erfolgt anhand etablierter Kriterien.[2] Hinweise auf eine solche Risikokonstellation sind unter anderem:
- mindestens 3 Frauen mit Mammakarzinom in einer Familienlinie
- mindestens 2 Mammakarzinome, davon eines vor dem 51. Lebensjahr
- mindestens 2 Ovarialkarzinome in einer Linie
- Kombination von Mammakarzinom und Ovarialkarzinom in einer Linie
- Mammakarzinom vor dem 36. Lebensjahr
- bilaterales Mammakarzinom vor dem 51. Lebensjahr
- Mammakarzinom beim Mann
- triple-negatives Mammakarzinom vor dem 50. Lebensjahr
- Ovarialkarzinom vor dem 80. Lebensjahr
Hormonelle Faktoren
Eine verlängerte endogene Östrogenexposition ist ein gesicherter Risikofaktor für die Entstehung eines Mammakarzinoms. Das Risiko steigt mit der kumulativen Dauer der hormonellen Stimulation des Brustdrüsenepithels. Hierzu zählen insbesondere:
- frühe Menarche (vor dem 12. Lebensjahr),
- späte Menopause (nach dem 55. Lebensjahr),
- Nulliparität,
- und erste Geburt in höherem Lebensalter.
Frauen, die vor dem 20. Lebensjahr ein Kind geboren haben, weisen im Vergleich zu später oder nicht gebärenden Frauen ein signifikant reduziertes Risiko auf. Langfristig wirkt jede ausgetragene Schwangerschaft protektiv, insbesondere bei früher Erstgeburt. Eine kombinierte postmenopausale Hormonersatztherapie (Östrogen plus Gestagen) erhöht das Mammakarzinomrisiko. Das Risiko steigt mit der Anwendungsdauer. Eine alleinige Östrogentherapie zeigt ein differenzierteres und insgesamt geringeres Risikoprofil.
Die Einnahme oraler Kontrazeptiva ist mit einem leicht erhöhten relativen Risiko assoziiert. Dieses ist dosis- und anwendungsdauerabhängig und normalisiert sich in der Regel innerhalb von etwa zehn Jahren nach Absetzen.
Geographische Faktoren
Die Inzidenz des Mammakarzinoms variiert weltweit erheblich. Höhere Erkrankungsraten finden sich insbesondere in Nordamerika, Nordeuropa und Australien, während sie in vielen ostasiatischen und Teilen mediterraner Regionen niedriger sind. Migrationsstudien zeigen, dass sich das Erkrankungsrisiko von Frauen aus Niedriginzidenzregionen innerhalb einer oder zweier Generationen dem Niveau des Ziellandes annähert. Dies spricht gegen eine primär genetische Ursache der Unterschiede und für einen maßgeblichen Einfluss von Lebensstil- und Umweltfaktoren. Als relevante Einflussgrößen gelten unter anderem Ernährungsgewohnheiten, Körpergewicht, Alkoholkonsum, körperliche Aktivität sowie reproduktive Faktoren (z.B. Anzahl und Zeitpunkt von Schwangerschaften).
Ionisierende Strahlen
Ionisierende Strahlen wirken mutagen und können durch die Induktion von DNA-Doppelstrangbrüchen zur Karzinogenese beitragen. Das Mammakarzinomrisiko ist dabei sowohl von der kumulativen Strahlendosis als auch vom Alter zum Zeitpunkt der Exposition abhängig. Eine besonders relevante Risikokonstellation besteht bei thorakaler Bestrahlung im jungen Lebensalter, insbesondere vor dem 30. Lebensjahr (z.B. bei Hodgkin-Lymphom). In dieser Gruppe ist das spätere Mammakarzinomrisiko deutlich erhöht und kann – abhängig von Dosis und Alter bei Exposition – erheblich über dem Bevölkerungsdurchschnitt liegen. Mit zunehmendem Alter bei Strahlenexposition nimmt das zusätzliche Risiko deutlich ab, ist jedoch nicht vollständig ausgeschlossen. Die im Rahmen des qualitätsgesicherten Mammographie-Screenings eingesetzte Röntgenstrahlung ist mit einer sehr niedrigen Einzeldosis verbunden. Nach derzeitigem Kenntnisstand überwiegt der Nutzen der Früherkennung das theoretische strahlenbedingte Zusatzrisiko deutlich.
Weitere Risikofaktoren
Adipositas ist insbesondere nach der Menopause ein gesicherter Risikofaktor. Ursache ist unter anderem die vermehrte periphere Östrogenbildung im Fettgewebe durch Aromatisierung von Androgenen. Regelmäßiger Alkoholkonsum erhöht das Mammakarzinomrisiko dosisabhängig. Bereits geringe Mengen Alkohol sind mit einem leicht erhöhten relativen Risiko assoziiert. Körperliche Inaktivität ist ebenfalls mit einem erhöhten Erkrankungsrisiko verbunden, während regelmäßige körperliche Aktivität protektiv wirkt. Für eine fettreiche Ernährung besteht keine konsistente unabhängige Evidenz als spezifischer Risikofaktor. Auch für Nikotinkonsum ist die Datenlage hinsichtlich eines eigenständigen Brustkrebsrisikos uneinheitlich, wenngleich Rauchen zahlreiche andere onkologische Erkrankungen begünstigt.
Einteilung
...nach Invasivität
Mammakarzinome werden in Abhängigkeit vom Durchbruch der Basalmembran unterteilt in nicht-invasive Carcinomata in situ und invasive Karzinome.
...nach histopathologischem Typ
Gemäß der WHO-Klassifikation (5. Auflage) unterscheidet man folgende Typen:
- nicht-invasive Karzinome (Carcinomata in situ):
- duktales Carcinoma in situ (DCIS)
- lobuläres Carcinoma in situ (LCIS): wird heute als nicht-obligate Präkanzerose bzw. Risikoläsion eingeordnet.
- invasive Karzinome:
- Invasives Karzinom ohne speziellen Typ (NST) (ca. 70–80 %)
- Invasives lobuläres Karzinom (ca. 10–15 %)
- Invasive Karzinome mit speziellem Typ: u.a. tubulär, muzinös, kribriform, neuroendokrin, metaplastisch
Aufgrund der Heterogenität der Tumorzellen kann die histologische und molekulare Charakterisierung zwischen Primärtumor und Metastasen variieren.[3] Bei Rezidiv oder Metastasierung wird daher eine erneute Biopsie empfohlen.
...nach histologischem Grading
Die histologische Differenzierung invasiver Mammakarzinome erfolgt in der Regel nach dem modifizierten Bloom-Richardson-System (Nottingham-Grading, Elston-Ellis-Score). Das Grading ist ein unabhängiger prognostischer Faktor. Bewertet werden drei morphologische Kriterien:
- Tubulus- bzw. Drüsenbildung (Grad der strukturellen Differenzierung)
- Kernpleomorphie (Größe, Form und Variabilität der Zellkerne)
- Mitoserate (Proliferationsaktivität)
Jedes Kriterium wird mit 1 bis 3 Punkten bewertet. Die Summe (3–9 Punkte) ergibt den histologischen Gesamtgrad:
- G1 (3–5 Punkte): gut differenziert
- G2 (6–7 Punkte): mäßig differenziert
- G3 (8–9 Punkte): schlecht differenziert
Ein höherer Grad ist mit einer ungünstigeren Prognose assoziiert. Das Grading wird ausschließlich bei invasiven Karzinomen angewendet. Beim DCIS erfolgt eine separate nukleäre Graduierung.
...nach molekularem Subtyp
Neben der histologischen Typisierung erfolgt die klinisch relevante Einteilung invasiver Mammakarzinome anhand immunhistochemisch bestimmter Biomarker. Entscheidend sind der Östrogenrezeptor (ER), der Progesteronrezeptor (PR), der HER2-Status sowie die Proliferationsrate (Ki-67). Auf Grundlage dieser Parameter werden therapeutisch und prognostisch relevante Subtypen unterschieden:
- Hormonrezeptor-positiv (HR+)/HER2-negativ: Tumoren mit Expression von ER und/oder PR ohne HER2-Überexpression oder -Amplifikation. Innerhalb dieser Gruppe werden häufig unterschieden:
- Luminal A-like: niedrig proliferierend, günstige Prognose
- Luminal B-like: höher proliferierend und/oder PR-niedrig, ungünstigere Prognose
- HER2-positiv: Tumoren mit HER2-Überexpression oder -Genamplifikation, unabhängig vom Hormonrezeptorstatus. Diese Subgruppe ist gezielt therapeutisch adressierbar.
- Triple-negativ: Keine Expression von ER und PR sowie kein HER2-Nachweis. Diese Tumoren weisen häufig eine höhere Proliferationsrate auf und sind prognostisch ungünstiger. Molekular entsprechen sie häufig dem sogenannten "basal-like"-Subtyp.
Die molekulare Subtypisierung hat entscheidende Bedeutung für Therapieplanung, Prognoseabschätzung und Auswahl systemischer Behandlungsstrategien.
...nach klinischem Stadium
- Frühes Mammakarzinom (Early Breast Cancer, EBC)
- Lokal fortgeschrittenes Mammakarzinom
- Metastasiertes Mammakarzinom (Metastatic Breast Cancer, MBC)
Die Stadieneinteilung erfolgt nach der TNM-Klassifikation (s.u.)
Sonderformen
- Morbus Paget der Mamille: meist mit einem zugrunde liegenden DCIS oder invasiven Karzinom assoziiert; keine eigenständige histologische Kategorie
- Inflammatorisches Mammakarzinom: klinisch definierte Sonderform
Pathogenese
Das Mammakarzinom entsteht durch die schrittweise Akkumulation genetischer und epigenetischer Veränderungen in Epithelzellen der terminalen duktulolobulären Einheit (TDLU). Diese Veränderungen betreffen zentrale Signalwege der Zellproliferation, DNA-Reparatur, Apoptose und Differenzierung.
Genetische und molekulare Veränderungen
Die Tumorentstehung beruht auf einem Ungleichgewicht zwischen onkogenen Aktivierungen und dem Verlust tumorsuppressiver Funktionen. Häufige molekulare Alterationen betreffen unter anderem:
- PI3K/AKT/mTOR-Signalweg (z.B. PIK3CA-Mutationen)
- TP53 (insbesondere bei triple-negativen Tumoren)
- HER2 (ERBB2)-Amplifikation
- Störungen der homologen DNA-Reparatur (z.B. bei BRCA1/2-Defizienz)
Bei einem Teil der Tumoren liegt eine Defizienz der homologen Rekombination (homologous recombination deficiency, HRD) vor, die zu genomischer Instabilität führt.
Hormonabhängige Karzinogenese
Ein wesentlicher pathogenetischer Faktor ist die hormonelle Stimulation durch Östrogene. Östrogenrezeptor-vermittelte Signalwege fördern die Proliferation und das Überleben von Epithelzellen. Eine verlängerte oder verstärkte hormonelle Exposition erhöht die Wahrscheinlichkeit von Replikationsfehlern und klonaler Expansion transformierter Zellen.
Hormonrezeptor-positive Karzinome entstehen typischerweise über hormonabhängige Wachstumsmechanismen, während triple-negative Karzinome häufiger durch Defekte in DNA-Reparatur- oder Zellzyklusregulationssystemen charakterisiert sind.
Genomische Instabilität und Tumorprogression
Im Verlauf der Tumorentwicklung kommt es zu zunehmender genomischer Instabilität, klonaler Selektion und intratumoraler Heterogenität. Diese Heterogenität kann zu unterschiedlichen biologischen Eigenschaften innerhalb desselben Tumors führen und beeinflusst Therapieansprechen sowie Resistenzentwicklung. Der Übergang vom Carcinoma in situ zum invasiven Karzinom ist durch den Verlust der Basalmembranintegrität und Veränderungen der Zelladhäsion (z.B. E-Cadherin-Verlust beim lobulären Karzinom) gekennzeichnet.
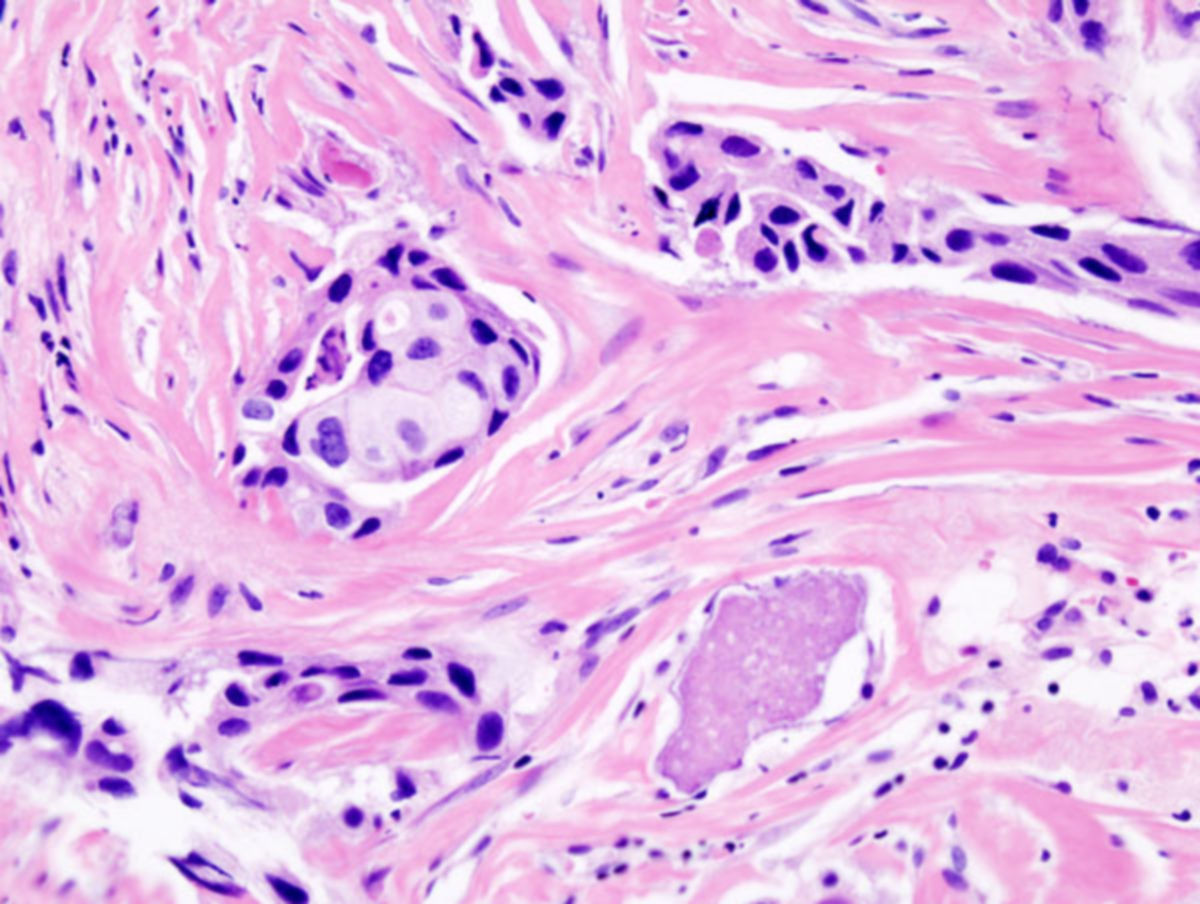
Histopathologie
Klinik
Das Mammakarzinom ist im Frühstadium häufig asymptomatisch und wird nicht selten im Rahmen des Screenings entdeckt. Klinische Symptome treten meist erst bei zunehmender Tumorgröße oder lokaler Infiltration auf.
Lokale Zeichen
Das häufigste klinische Zeichen ist ein tastbarer, meist derber, unscharf begrenzter Knoten der Brust. Im Gegensatz zu vielen benignen Veränderungen sind Mammakarzinome häufig schlecht verschieblich und können durch Infiltration des umliegenden Gewebes fixiert erscheinen.
Weitere lokale Veränderungen können sein:
- Hauteinziehungen über dem Tumorareal
- Retraktion oder Deviation der Mamille, insbesondere bei retromamillärer Lokalisation
- Peau d'orange durch lymphatische Stauung
- neu aufgetretene Asymmetrie oder Konturveränderung der Brust
- Spontane, einseitige Mamillensekretion, teilweise blutig
- Ekzematöse Veränderungen im Sinne eines Morbus Paget
- Hautfixierte Einziehung bei Kompression (Plateauphänomen) kann ein Hinweis auf eine Infiltration der Cooper-Ligamente sein. Diese kann durch eine Kompression der Haut über dem tastbaren Knoten dargestellt werden (Jackson-Test).
Inflammatorisches Mammakarzinom
Das inflammatorische Mammakarzinom präsentiert sich typischerweise mit diffuser Rötung, Überwärmung und Schwellung der Brust, oft ohne klar abgrenzbaren Knoten. Klinisch kann es einer Mastitis ähneln, zeichnet sich jedoch durch rasche Progredienz und fehlendes Ansprechen auf antibiotische Therapie aus.
Lymphknotenbefall
Ein vergrößerter, harter, schlecht verschieblicher axillärer Lymphknoten kann auf eine nodale Metastasierung hinweisen.
Fortgeschrittene Stadien
In fortgeschrittenen Stadien kann es zu Hautulzerationen (exulzeriertes Mammakarzinom), Blutungen oder sekundären Infektionen kommen. Systemische Symptome treten meist erst im metastasierten Stadium auf und sind abhängig von der Lokalisation der Metastasen (z.B. Knochenschmerzen, Dyspnoe, neurologische Ausfälle).
Befallsmuster
Bei etwa 3–5 % der Patientinnen liegt zum Zeitpunkt der Erstdiagnose ein synchron bilaterales Mammakarzinom vor. Davon abzugrenzen sind metachrone kontralaterale Zweitkarzinome, die im Verlauf auftreten können.
Die Lokalisation innerhalb der Brust zeigt eine charakteristische Verteilung. Etwa 50 % der Mammakarzinome entstehen im oberen äußeren Quadranten, was der hohen Dichte an Drüsengewebe in diesem Bereich entspricht. Rund 15–20 % sind retro- bzw. perimamillär lokalisiert. Die übrigen Tumoren verteilen sich annähernd gleichmäßig auf die restlichen Quadranten.
Treten mehrere Tumorherde innerhalb desselben Quadranten auf, spricht man von einem multifokalen Befall. Bei Tumorherden in unterschiedlichen Quadranten derselben Brust liegt ein multizentrischer Befall vor.
Metastasierung
Mammakarzinome metastasieren lymphogen und hämatogen. Das Metastasierungsrisiko korreliert insbesondere mit Tumorgröße, histologischem Grad, Lymphknotenbefall und biologischem Subtyp. Das individuelle Metastasierungsrisiko hängt wahrscheinlich auch von genetischen Faktoren ab. Bei Patientinnen mit homozygoten Mutationen des PCSK9-Gens (rs562556, V474I) scheint beispielsweise das Risiko für Fernmetastasen erhöht zu sein.[4]
Lymphogene Metastasierung
Der primäre lymphatische Abfluss erfolgt in die axillären Lymphknoten. Bei Tumoren der äußeren Quadranten ist die axilläre Metastasierung am häufigsten. Karzinome der inneren Quadranten können zusätzlich oder primär in die parasternalen Lymphknoten entlang der Arteria thoracica interna metastasieren. Seltener sind supraklavikuläre oder infraklavikuläre Lymphknotenstationen betroffen.
Hämatogene Metastasierung
Über die hämatogene Streuung können prinzipiell zahlreiche Organe betroffen sein. Typische Manifestationsorte sind:
Das Metastasierungsmuster hängt teilweise vom molekularen Subtyp ab. Hormonrezeptor-positive Tumoren metastasieren häufiger ossär, während HER2-positive und triple-negative Tumoren häufiger viszerale oder zerebrale Metastasen aufweisen.
Lokoregionäre Ausbreitung
Fortgeschrittene Mammakarzinome können in Haut und Thoraxwand infiltrieren. Eine ausgeprägte dermale Lymphangiosis kann zum klinischen Bild eines Cancer en cuirasse führen.
Diagnostik
Die Diagnostik des Mammakarzinoms umfasst die klinische Untersuchung, bildgebende Verfahren sowie die histopathologische Sicherung durch Biopsie. Ziel ist die Bestätigung der Diagnose, die Bestimmung biologischer Tumoreigenschaften sowie die Stadieneinteilung.
Klinische Untersuchung
Die körperliche Untersuchung muss stets im Seitenvergleich durchgeführt werden und beinhaltet:
- Inspektion: Asymmetrie, Haut- oder Mamillenveränderungen
- Palpation der Mamma
- Palpation der Lymphknotenstationen (Verschieblichkeit, Lymphadenopathien)
Bildgebung
Die bildgebende Basisdiagnostik besteht aus:
- Mammographie: Standardverfahren
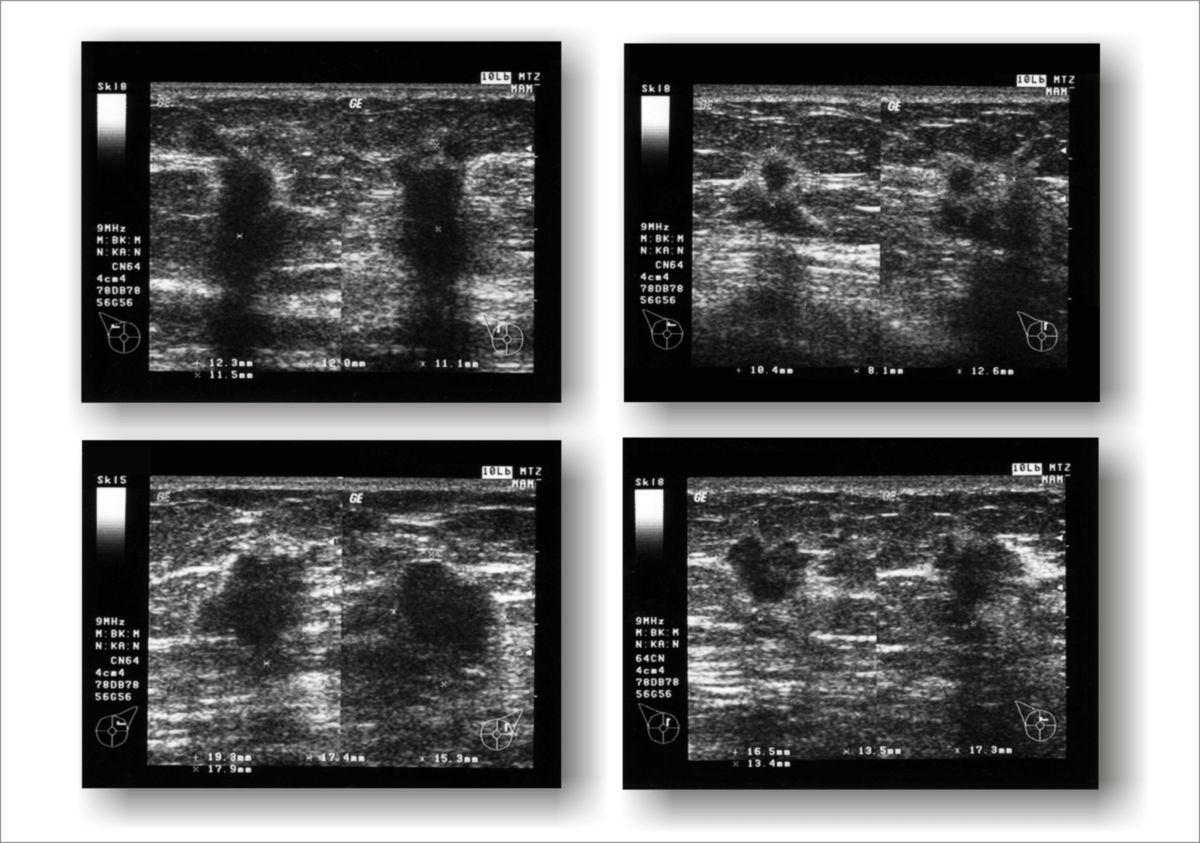
- Mammasonographie: insbesondere bei dichter Brust
- Mamma-MRT: bei unklaren oder diskrepanten Befunden, Hochrisikopatientinnen, zur präoperativen Ausdehnungsdiagnostik vor neoadjuvanter Therapie
In seltenen Fällen kommt Galaktographie bei pathologischer Mamillensekretion zum Einsatz.
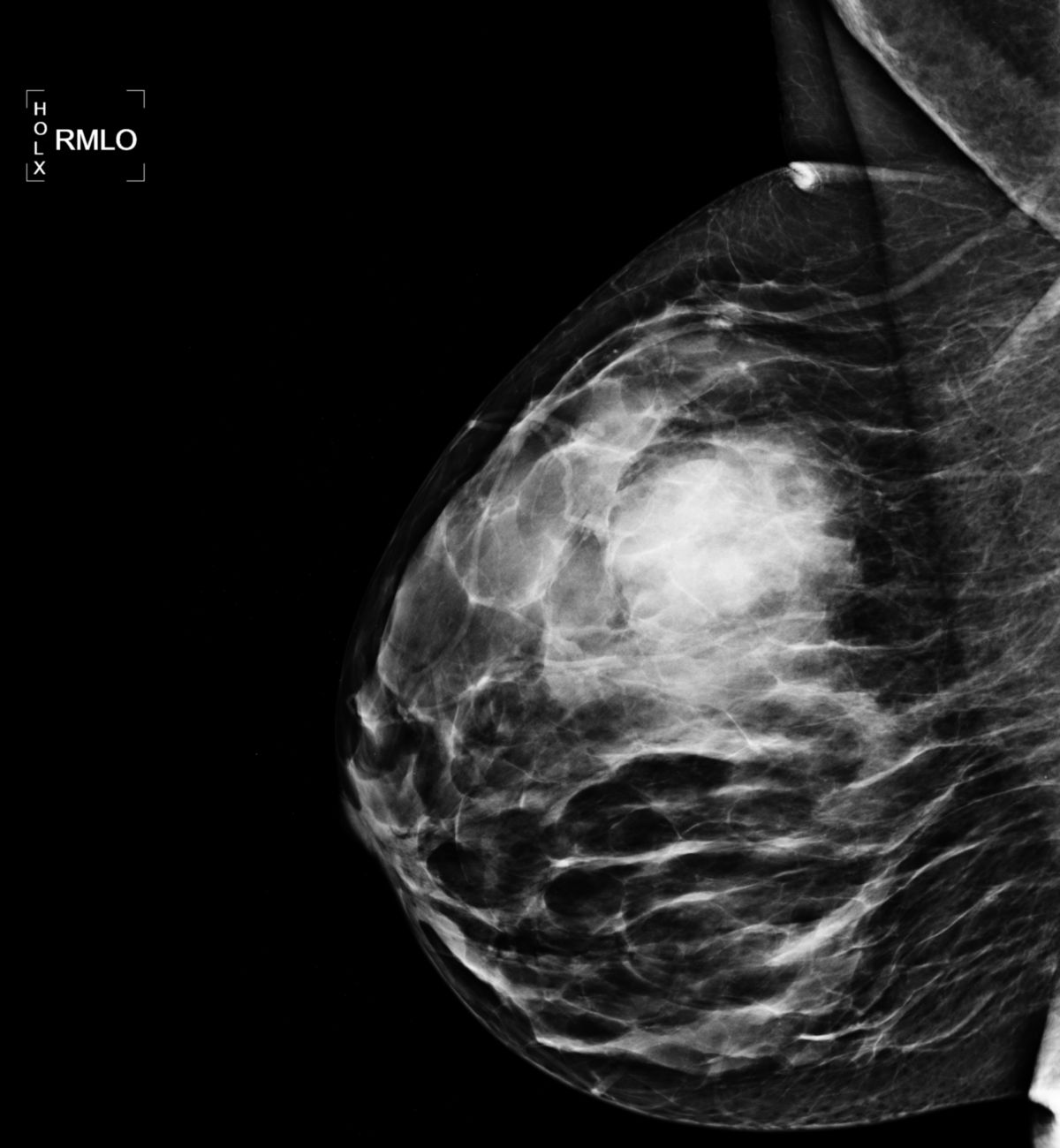
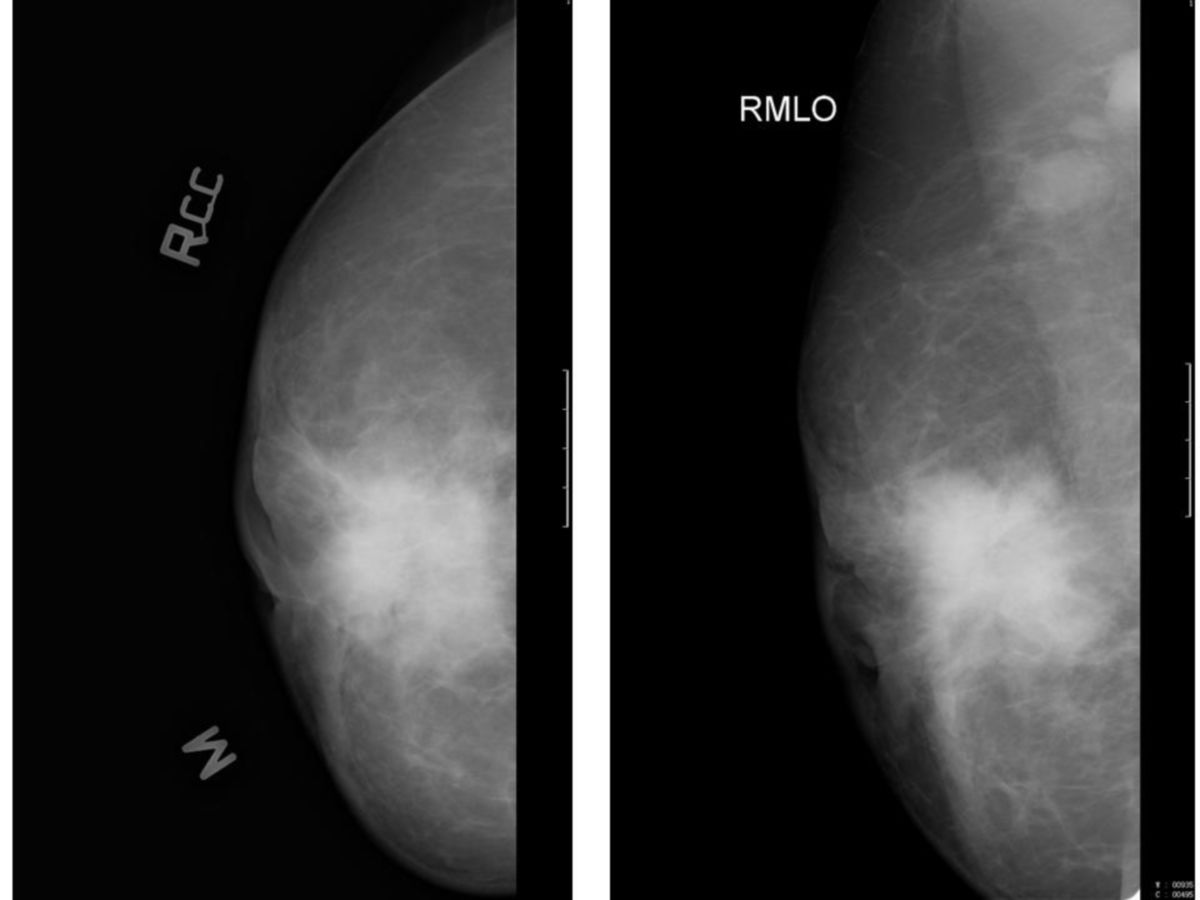
Mammographie
Die Mammographie ist das primäre bildgebende Verfahren zur Detektion und Abklärung suspekter Mammaläsionen. Sie erlaubt die Beurteilung von Raumforderungen, Architekturstörungen und Mikroverkalkungen. Typische mammographische Zeichen eines Mammakarzinoms sind:
- Raumforderung: dichte Raumforderung mit irregulärer oder spikulierter Begrenzung, unscharfer oder sternförmiger Kontur und architektonischer Verzerrung des umgebenden Parenchyms. Spikulationen entstehen durch eine desmoplastische Stromareaktion und sind ein hochspezifisches Malignitätszeichen.
- Mikroverkalkungen: insbesondere DCIS manifestiert sich häufig primär durch Mikroverkalkungen. Malignitätstypische Konfigurationen sind pleomorphe Mikroverkalkungen, lineare oder verzweigte Verkalkungen ("casting type") und/oder segmentale oder lineare Verteilung. Benigne Verkalkungen sind meist grob, rundlich oder diffus verteilt.
- Architekturstörung: Eine isolierte Architekturstörung ohne klar abgrenzbare Raumforderung kann das einzige Zeichen eines invasiven Karzinoms sein.
Die Sensitivität der Mammographie ist abhängig von der Brustdichte. Bei dichtem Drüsengewebe (ACR C/D) kann ein Karzinom maskiert sein. Hier gewinnt die ergänzende Sonographie oder MRT an Bedeutung.
Mamma-MRT
Die kontrastmittelgestützte Mamma-MRT ist das sensitivste bildgebende Verfahren zur Detektion invasiver Mammakarzinome. Sie basiert auf der Darstellung der Tumorvaskularisation und Kontrastmittelkinetik. Ein Mammakarzinom erscheint typischerweise als irregulär begrenzte Raumforderung mit spikulierten oder unscharfen Rändern und heterogener Kontrastmittelaufnahme. Bei größeren Tumoren können zentrale Nekrosen auffallen. Alternativ kann sich ein Karzinom als non-mass enhancement (NME) darstellen, insbesondere bei ausgedehntem DCIS. Wichtig bei der Beurteilung ist die Kontrastmitteldynamik:
- rascher initialer Anstieg (wash-in)
- Plateau- oder Wash-out-Kinetik (Typ II oder III-Kurve): Ein Wash-out-Verhalten ist mit einer höheren Wahrscheinlichkeit für Malignität assoziiert, jedoch nicht pathognomonisch.
Pathohistologie
Die definitive Diagnosesicherung erfolgt durch eine bildgesteuerte perkutane Stanzbiopsie. Je nach Befundkonstellation kommen unterschiedliche Verfahren zum Einsatz:
- Sonographisch gesteuerte Stanzbiopsie (Standardverfahren bei sonographisch darstellbarer Läsion)
- Stereotaktische Vakuumbiopsie bei ausschließlich mammographisch sichtbarem Befund (z. B. Mikrokalk)
- MRT-gestützte Biopsie bei ausschließlich MRT-sichtbarer Läsion
Eine offene Probeexzision zur primären Diagnosesicherung ist heute nur noch in Ausnahmefällen indiziert.
Die histopathologische Untersuchung umfasst:
- Histologischer Typ
- Grading (Nottingham-System)
- Hormonrezeptorstatus (ER, PR)
- HER2-Status
- Proliferationsmarker Ki-67
Die immunhistochemische Bestimmung dieser Marker ermöglicht die Einteilung in therapeutisch relevante molekulare Subtypen (HR+, HER2+, triple-negativ).
Tumorgenomik
Bei ausgewählten Patientinnen mit frühem, hormonrezeptorpositivem, HER2-negativem Mammakarzinom können validierte Multigen-Assays zur Abschätzung des Rezidivrisikos und zur Therapieentscheidung hinsichtlich einer Chemotherapie herangezogen werden.
Labor
Tumormarker wie CA 15-3 oder CEA sind nicht zur Primärdiagnostik geeignet. Sie können im Verlauf bei metastasierter Erkrankung ergänzend zur Therapiekontrolle eingesetzt werden. Eine routinemäßige Bestimmung von Sexualhormonen (Östrogen, FSH, Prolaktin) ist nicht Bestandteil der Mammakarzinomdiagnostik.
Staging
Das Staging dient der Bestimmung der lokalen Tumorausdehnung, des Lymphknotenstatus sowie dem Nachweis oder Ausschluss von Fernmetastasen. Die Stadieneinteilung erfolgt nach der aktuellen TNM-Klassifikation der UICC/AJCC.
Lokoregionäres Staging
Die Beurteilung der lokalen Tumorausdehnung erfolgt mittels Mammographie, Sonographie und ggf. Mamma-MRT. Die axilläre Lymphknotenbeurteilung erfolgt klinisch und sonographisch. Bei klinisch nodal-negativen Patientinnen wird der axilläre Status operativ durch Sentinel-Lymphknotenbiopsie bestimmt. Bei nachgewiesenem Lymphknotenbefall erfolgt das pathologische N-Staging.
Systemisches Staging
Ein routinemäßiges Fernmetastasen-Staging ist bei asymptomatischen Patientinnen mit frühem Mammakarzinom (cT1-T2, cN0) nicht indiziert. Ein systemisches Staging wird empfohlen bei:
- klinisch positivem Lymphknotenbefall (cN+)
- Tumorgröße ≥ T3
- inflammatorischem Mammakarzinom
- klinischem Verdacht auf Fernmetastasen
- geplanter neoadjuvanter Therapie (je nach Risikokonstellation)
Zur systemischen Ausbreitungsdiagnostik werden in der Regel eingesetzt:
- CT von Thorax und Abdomen
- ggf. Knochenszintigraphie
- ggf. PET-CT bei lokal fortgeschrittener Erkrankung oder unklaren Befunden
Die Wahl der Untersuchungsmethode erfolgt risikoadaptiert entsprechend der klinischen Situation.
Primärtumor
| T-Kategorie | Bedeutung |
|---|---|
| T0 | Kein Anhalt für Primärtumor |
| Tis | Carcinoma in situ |
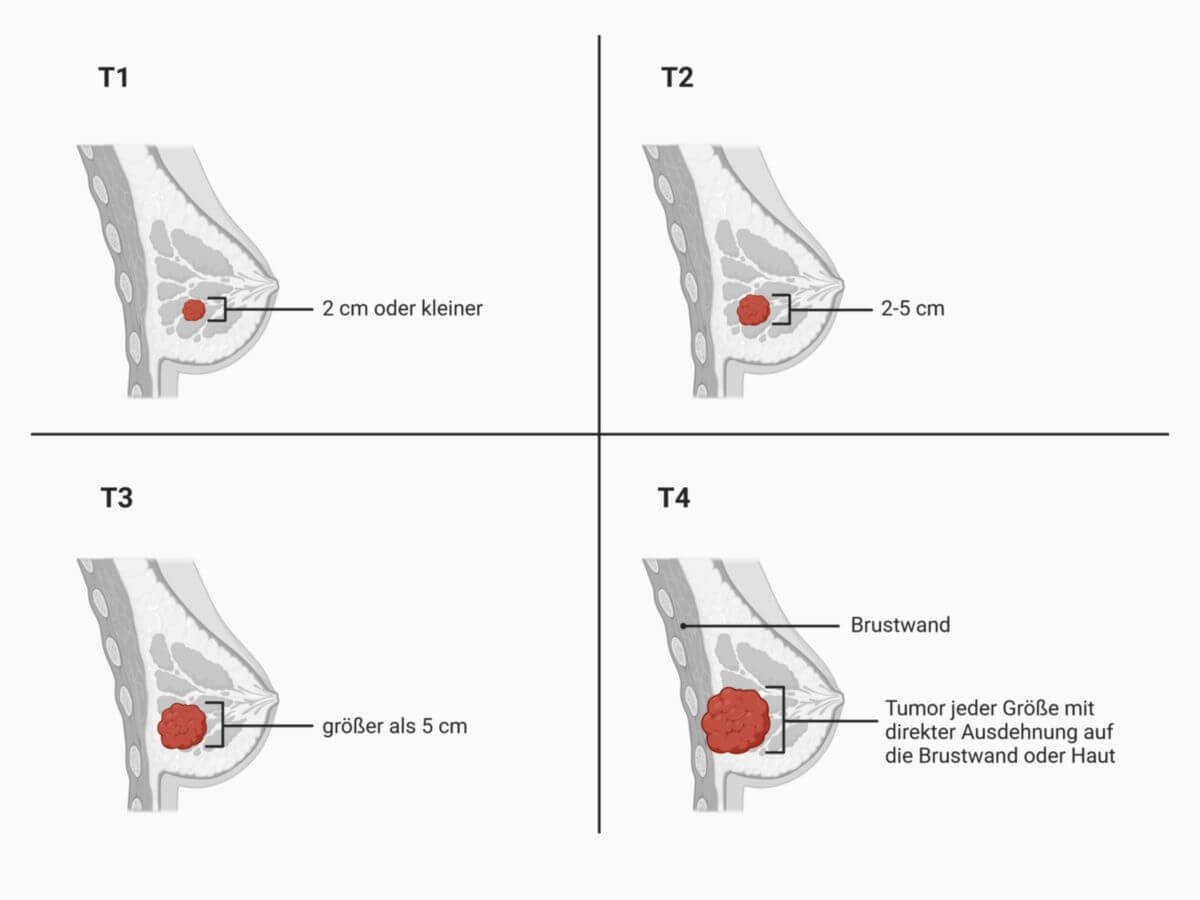
| T1 | Tumor ≤ 2 cm T1mi - ≤ 1 mm |
| T2 | > 20–50 mm |
| T3 | > 50 mm |
| T4 | Tumor jeder Größe mit direkter Ausdehnung auf die Brustwand oder Haut T4a - Infiltration der Brustwand (Rippen, Interkostalmuskulatur, Musculus serratus anterior; Musculus pectoralis major allein genügt nicht für T4) |
| TX | Primärtumor kann nicht beurteilt werden |
Regionäre Lymphknoten
| cN-Kategorie | Bedeutung | |
|---|---|---|
| cN0 | Keine regionären Lymphknotenmetastasen | |
| cN1 | Metastase(n) in beweglichen ipsilateralen axillären Lymphknoten (Level I-II) | |
| cN2 | cN2a | Fixierte oder untereinander verbackene ipsilaterale axilläre Lymphknoten (Level I-II) |
| cN2b | Klinisch erkennbare ipsilaterale interne mammäre Lymphknoten ohne axillären Befall | |
| cN3 | cN3a | Infraklavikuläre Lymphknoten (Level III) |
| cN3b | Lymphknoten entlang Arteria thoracica interna mit axillärem Befall | |
| cN3c | Supraklavikuläre Lymphknoten | |
| cNX | Lymphknoten nicht beurteilbar | |
| pN-Kategorie | Bedeutung | |
|---|---|---|
| pN0 | Keine regionären Lymphknotenmetastasen | |
| pN0(i+) | Isolierte Tumorzellen ≤ 0,2 mm | |
| pN1mi | Mikrometastasen > 0,2–2 mm | |
| pN1 | 1–3 axilläre Metastasen und/oder mikroskopische interne mammäre Metastasen | |
| pN2 | pN2a | 4–9 axilläre Lymphknotenmetastasen |
| pN2b | Nur histologisch nachgewiesene interne mammäre Metastasen ohne axillären Befall | |
| pN3 | pN3a | ≥ 10 axilläre Metastasen oder infraklavikuläre Metastasen |
| pN3b | Interne mammäre Metastasen mit axillärem Befall | |
| pN3c | Supraklavikuläre Lymphknoten | |
| pNX | Lymphknoten nicht beurteilbar | |
Fernmetastasen
| M-Kategorie | Bedeutung |
|---|---|
| M0 | Keine Fernmetastasen |
| M1 | Fernmetastasen |
UICC-Stadien
| Stadium | TNM | |
|---|---|---|
| 0 | Tis, N0, M0 | |
| I | IA | T1, N0, M0 |
| IB | T0 oder T1 mit pN1mi, M0 | |
| II | IIA | T0 oder T1, N1, M0 |
| T2, N0, M0 | ||
| IIB | T2, N1, M0 | |
| T3, N0, M0 | ||
| III | IIIA | T0-T2, N2, M0 |
| T3, N1-N2, M0 | ||
| IIIB | T4, N0-N2, M0 | |
| IIIC | jedes T, N3, M0 | |
| IV | jedes T, jedes N, M1 | |
Prognostische Stadien
Neben der rein anatomischen Stadieneinteilung nach TNM (UICC/AJCC) wird seit der 8. Edition der AJCC zusätzlich ein sogenanntes prognostisches Stadium (Prognostic Stage Grouping) definiert. Dieses berücksichtigt neben der Tumorausdehnung auch biologische Tumoreigenschaften und spiegelt damit die prognostische Relevanz moderner molekularer Marker wider. In das prognostische Stadium gehen ein:
- TNM, Grading
- Östrogenrezeptor-Status (ER)
- Progesteronrezeptor-Status (PR)
- HER2-Status
Bei ausgewählten Patientinnen mit hormonrezeptorpositivem, HER2-negativem, nodal-negativem Mammakarzinom kann zusätzlich ein validierter Multigen-Assay berücksichtigt werden.
Das Prognostic Stage Grouping gilt für invasive Mammakarzinome ohne Fernmetastasen (M0). Bei Nachweis von Fernmetastasen (M1) liegt unabhängig von biologischen Parametern weiterhin Stadium IV vor.
Differentialdiagnose
Bei klinischem oder bildgebendem Verdacht auf ein Mammakarzinom kommen verschiedene benigne und selten auch andere maligne Erkrankungen in Betracht. Die definitive Abgrenzung erfolgt in der Regel histologisch.
Entzündliche Erkrankungen
- Mastitis: Typischerweise schmerzhaft, mit Rötung, Überwärmung und systemischen Entzündungszeichen. Im Gegensatz zum inflammatorischen Mammakarzinom meist rasches Ansprechen auf antibiotische Therapie.
- Abszess: Fluktuierende, schmerzhafte Raumforderung mit entzündlicher Begleitreaktion.
Gutartige Tumoren
- Fibroadenom der Mamma: Häufigste benigne Raumforderung bei jüngeren Frauen. Meist gut verschieblich, glatt begrenzt und sonographisch homogen.
- Intraduktales Papillom (Milchgangspapillom): Typischerweise mit einseitiger, ggf. blutiger Mamillensekretion assoziiert.
Fibrozystische Veränderungen
- Mastopathie/fibrozystische Veränderungen: Knotige, teils zyklusabhängige Veränderungen mit möglicher Mikrokalkbildung; können mammographisch ein DCIS imitieren.
- Brustzysten: Sonographisch glatt begrenzt und echofrei mit dorsaler Schallverstärkung.
Weitere Differentialdiagnosen
- Narben- oder Fettgewebsnekrose: Kann klinisch und mammographisch ein Karzinom imitieren (z. B. spikulierte Läsion nach Trauma oder Operation).
- Phylloides-Tumor: Seltene fibroepitheliale Neoplasie mit meist raschem Wachstum.
- Primäre Mammalymphome oder Metastasen anderer Tumoren: Selten, jedoch differenzialdiagnostisch zu berücksichtigen.
- Primäre Mammarsarkome (z.B. Angiosarkom): seltene mesenchymale Tumoren der Brust, die sich klinisch als rasch wachsende Raumforderung präsentieren können. Im Gegensatz zum Mammakarzinom erfolgt die Metastasierung überwiegend hämatogen; eine axilläre Lymphknotenbeteiligung ist untypisch.
Therapie
Die Therapie des Mammakarzinoms erfolgt stadien- und biologisch adaptiert und wird interdisziplinär im Rahmen einer Tumorkonferenz festgelegt. Entscheidend für die Therapieplanung sind Tumorstadium (TNM), histologischer Typ und Grading, Hormonrezeptorstatus (ER/PR), HER2-Status, Proliferationsmarker (Ki-67), ggf. genetische Prädisposition (z.B. BRCA) und Menopausenstatus.
Man unterscheidet:
- kurative Therapie (nicht metastasiert)
- palliative Therapie (metastasiert)
Operative Therapie
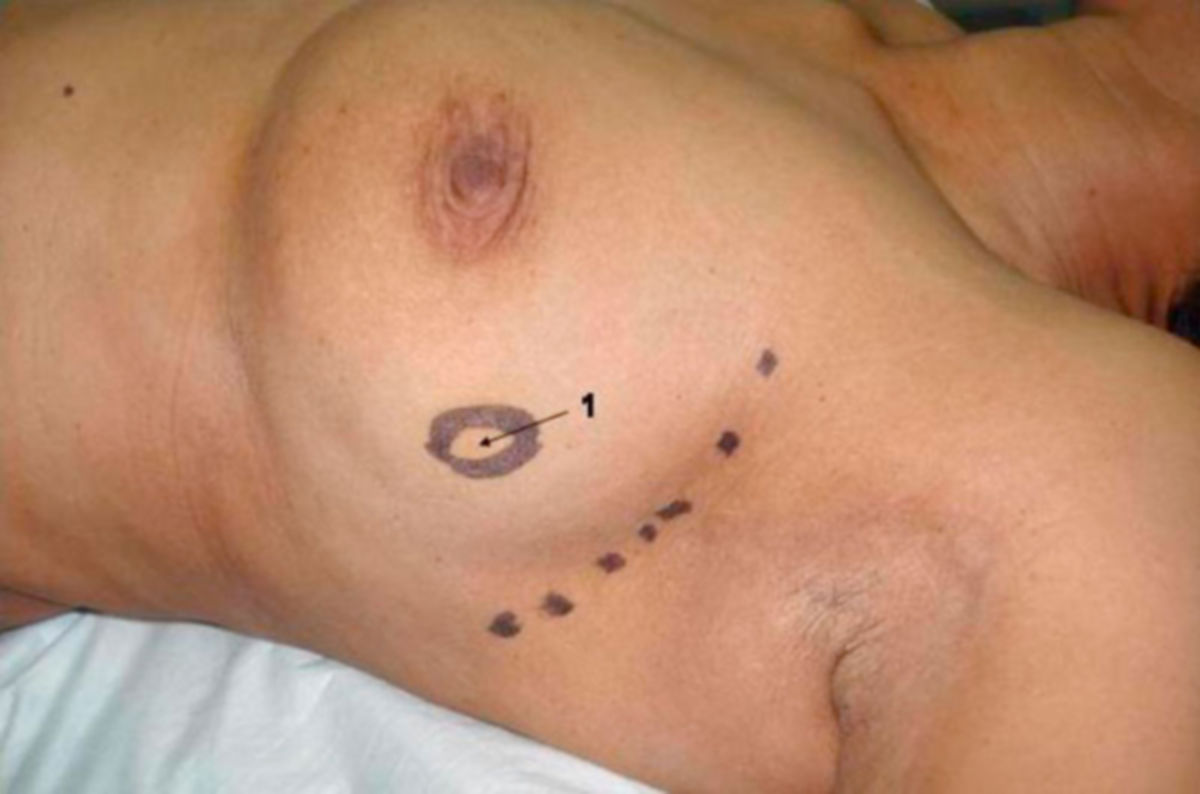
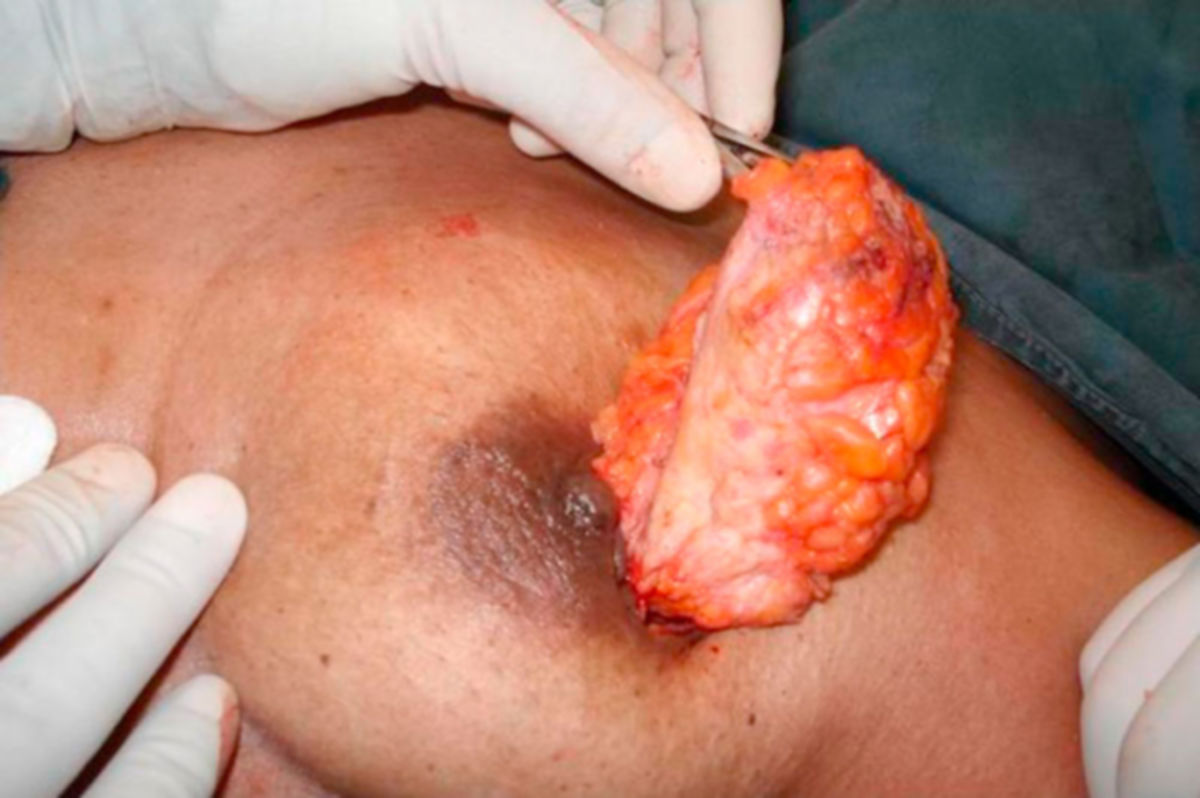
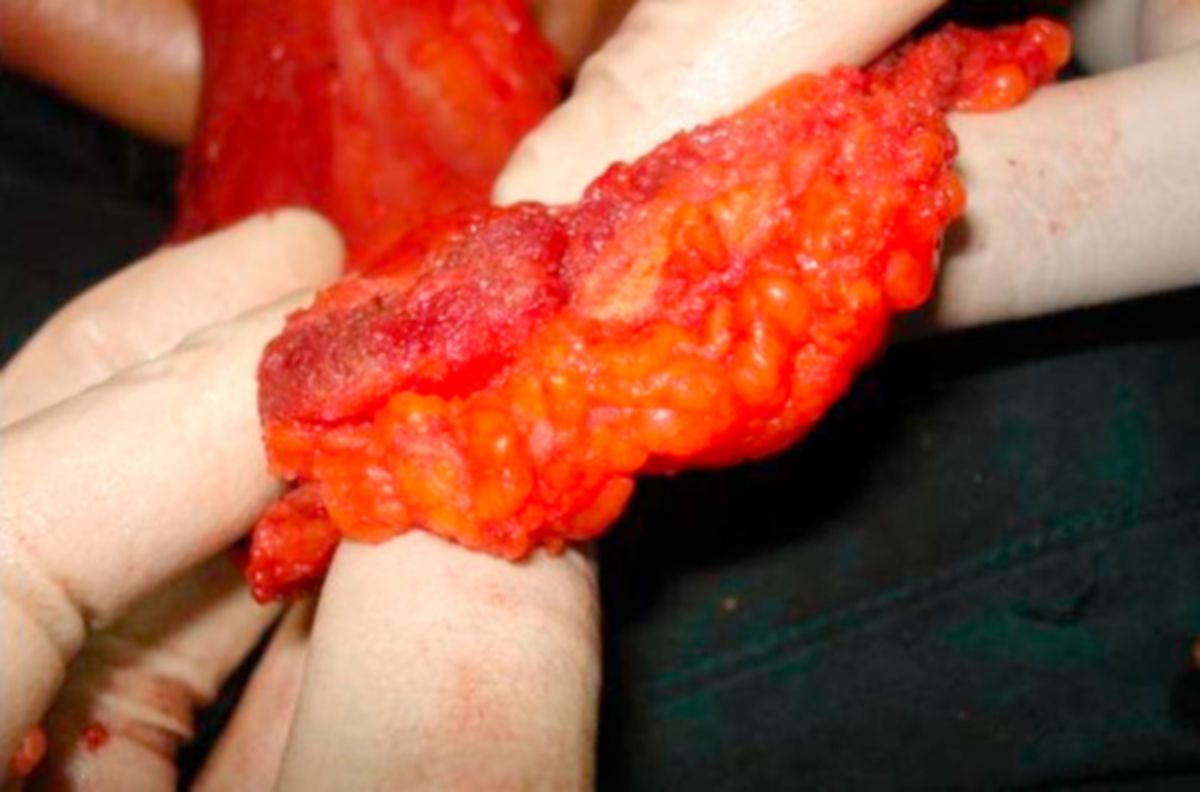
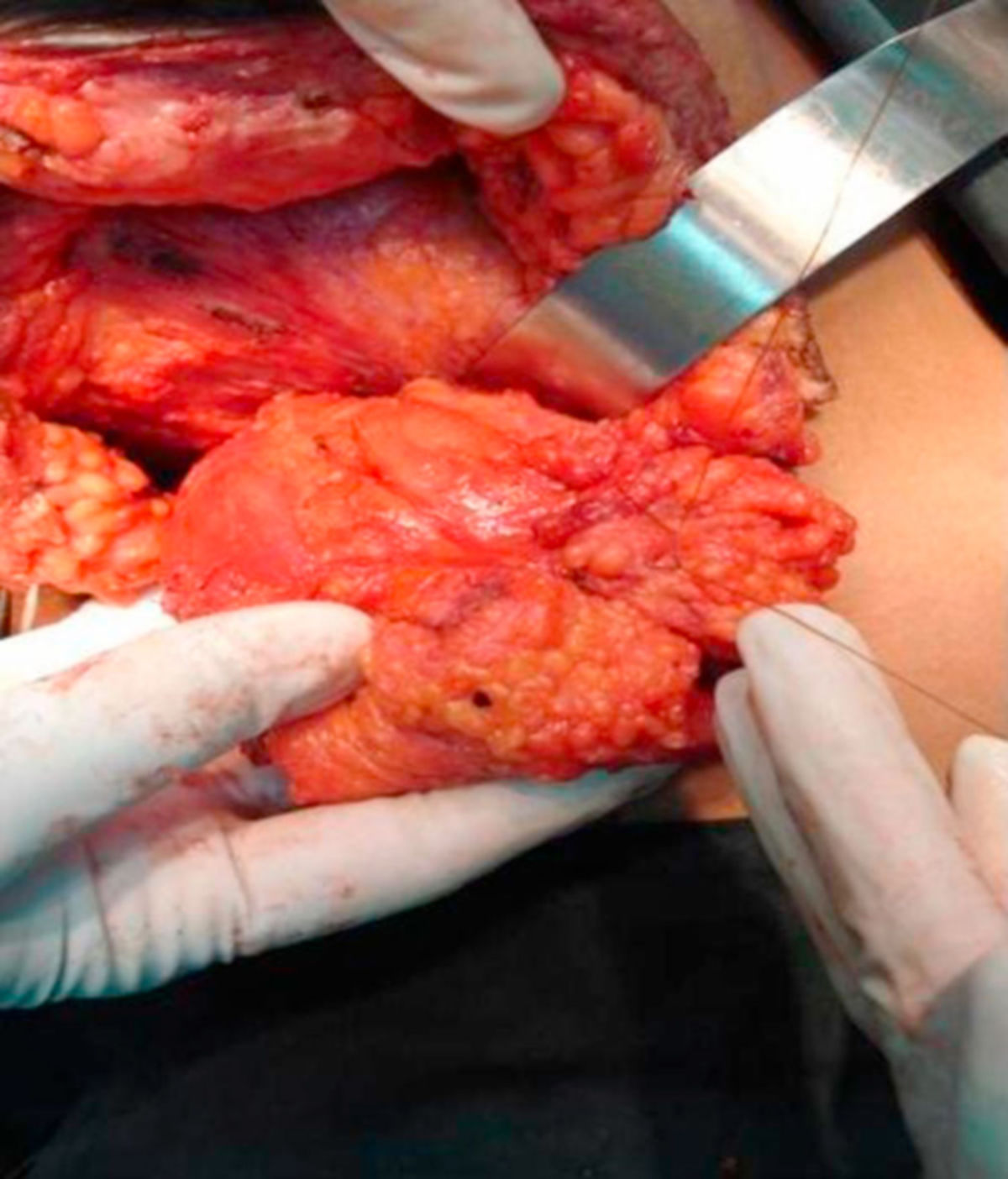
Die operative Therapie ist zentraler Bestandteil des kurativen Behandlungskonzepts beim nicht metastasierten Mammakarzinom. Ziel ist die vollständige Tumorentfernung (R0-Resektion) unter Berücksichtigung funktioneller sowie kosmetischer Aspekte. Die Entscheidung über das operative Vorgehen erfolgt interdisziplinär unter Berücksichtigung von Tumorgröße und -lokalisation, Multifokalität/Multizentrizität, Verhältnis Tumorgröße zu Brustvolumen, Biologie des Tumors, Notwendigkeit einer Radiotherapie und Patientinnenwunsch. Beim invasiven Mammakarzinom gilt als ausreichender Sicherheitsabstand wenn kein Tumor am Tuscherand erkennbar ist ("no ink on tumor"). Eine Nachresektion ist bei formal tumorfreien Resektionsrändern auch bei knappem Abstand nicht indiziert. Ziel sollte die R0-Resektion möglichst bereits bei der Primäroperation sein. Bei geplanter primärer systemischer Therapie (neoadjuvante Therapie) sollte das Tumorareal vor Therapiebeginn markiert werden, um nach Tumorregression eine sichere Resektion des ursprünglichen Tumorbetts zu gewährleisten.
Brusterhaltende Operation
Die brusterhaltende Therapie (BET) mit anschließender Ganzbrustbestrahlung ist onkologisch mindestens gleichwertig zur Mastektomie hinsichtlich des Gesamtüberlebens. Eine brusterhaltende Operation ist möglich bei:
- invasivem Mammakarzinom oder DCIS,
- günstiger Relation von Tumorgröße zu Brustvolumen,
- erreichbarer R0-Resektion,
- Möglichkeit einer adjuvanten Radiotherapie.
Auch bei multifokalem oder multizentrischem Befall kann in ausgewählten Fällen eine brusterhaltende Therapie durchgeführt werden, sofern vollständige Tumorfreiheit histologisch gesichert werden kann. Nicht tastbare Läsionen müssen präoperativ bildgebungsgestützt markiert werden. Die intraoperative Sonographie kann zur exakten Resektion sonographisch sichtbarer Tumoren eingesetzt werden. Das Tumorbett sollte intraoperativ mit Clips markiert werden, um eine gezielte Boost-Bestrahlung zu ermöglichen. Moderne onkoplastische Techniken (z.B. glanduläre Verschiebelappen, tumorlagenadaptierte Reduktionsplastiken, Rotationslappen) erlauben auch bei größeren Resektionsvolumina eine ästhetisch akzeptable Rekonstruktion bei gleichzeitiger onkologischer Sicherheit.
Mastektomie
Eine Mastektomie ist indiziert, wenn eine BET keine sichere R0-Resektion ermöglicht oder mit einem erhöhten Lokalrezidivrisiko verbunden wäre. Typische Indikationen sind:
- persistierend positive Resektionsränder trotz Nachresektion,
- inflammatorisches Mammakarzinom,
- Kontraindikation gegen eine notwendige Radiotherapie,
- ausdrücklicher Wunsch der Patientin.
Beim inflammatorischen Mammakarzinom ist nach neoadjuvanter Systemtherapie die modifizierte radikale Mastektomie Standardverfahren. Unter Berücksichtigung tumorfreier Resektionsränder kann eine Mastektomie hautsparend ("skin-sparing") oder mit Erhalt des Mamillen-Areola-Komplexes ("nipple-sparing") durchgeführt werden. Eine kontralaterale prophylaktische Mastektomie ist bei fehlender genetischer Hochrisikokonstellation nicht routinemäßig empfohlen.
Operative Therapie der Axilla
Die operative Axillatherapie dient primär dem Staging und der Abschätzung des Rezidivrisikos. Sie hat prognostische Bedeutung und beeinflusst adjuvante Therapieentscheidungen. Bei klinisch und bildmorphologisch unauffälliger Axilla (cN0) ist die Sentinel-Lymphknoten-Exzision (SLNE) das Standardverfahren. Sie ermöglicht eine zuverlässige Beurteilung des nodalen Status bei deutlich geringerer Morbidität im Vergleich zur Axilladissektion. Die axilläre Rezidivrate nach korrekt durchgeführter SLNE ist sehr niedrig. In ausgewählten Niedrigrisikokonstellationen kann auf ein operatives axilläres Staging verzichtet werden, insbesondere bei postmenopausalen Patientinnen mit kleinen, hormonrezeptorpositiven, HER2-negativen Tumoren, wenn eine adäquate Systemtherapie und Ganzbrustbestrahlung geplant sind.
Eine routinemäßige Axilladissektion ist heute nicht mehr Standard. Bei Patientinnen mit ein oder zwei befallenen Sentinel-Lymphknoten und geplanter adjuvanter Bestrahlung kann auf eine Axilladissektion verzichtet werden, da kein Überlebensnachteil und keine erhöhte axilläre Rezidivrate gezeigt wurden. Bei ausschließlicher Mikrometastasierung ist ebenfalls keine weiterführende axilläre Therapie erforderlich. Bei nachgewiesener Fernmetastasierung (M1) soll kein operatives axilläres Staging erfolgen.
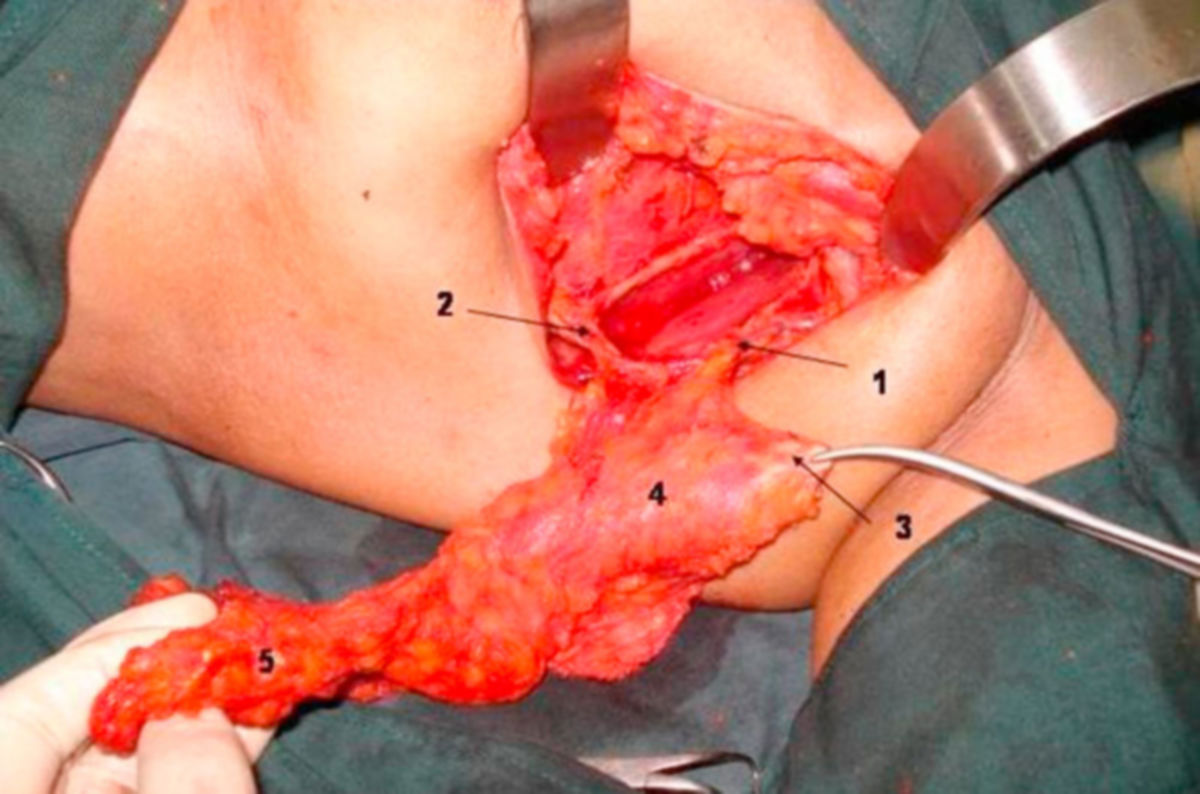
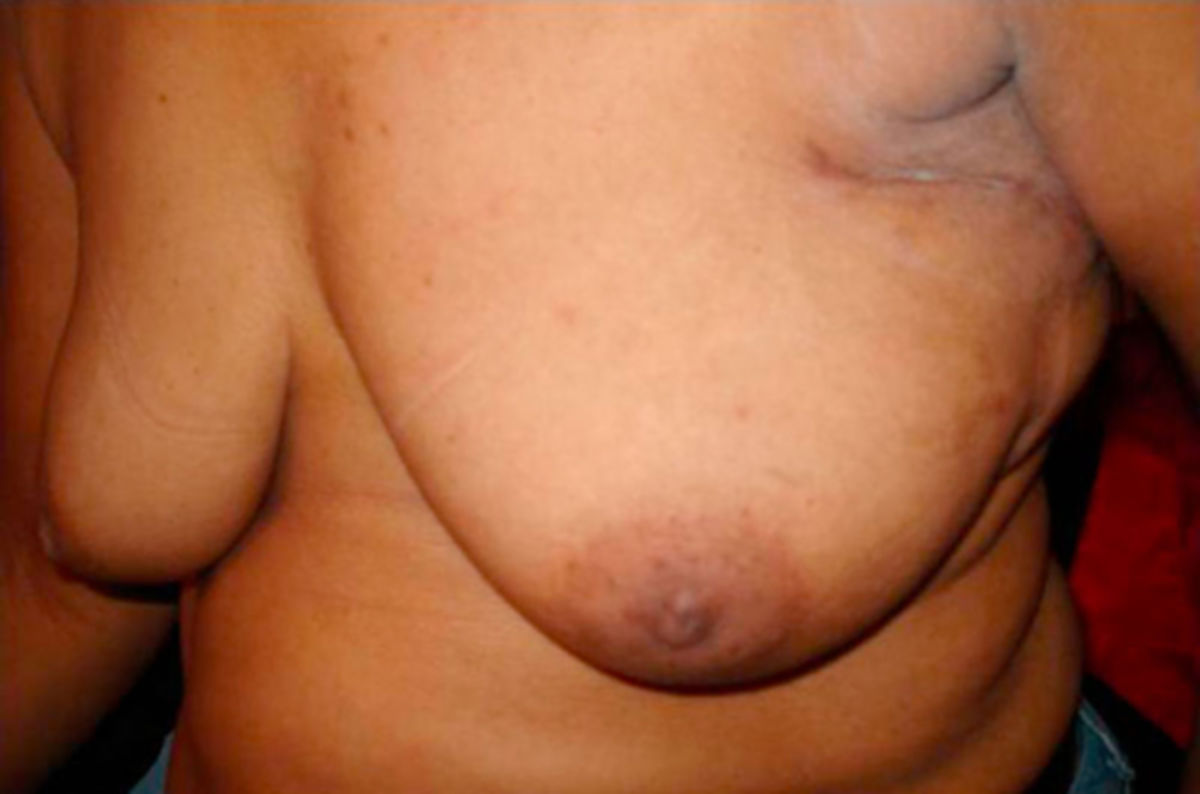
Rekonstruktive Verfahren
Nach Mastektomie kann eine primäre oder sekundäre Brustrekonstruktion erfolgen. Die Rekonstruktion kann alloplastisch (Implantat/Expander) oder autolog (z.B. Lappenplastiken) vorgenommen werden. Bei geplanter oder erfolgter Radiotherapie ist die autologe Rekonstruktion häufig mit besseren funktionellen und ästhetischen Ergebnissen verbunden.
Systemische Therapie
Die systemische Therapie ist integraler Bestandteil des kurativen und palliativen Behandlungskonzepts beim Mammakarzinom. Sie umfasst endokrine Therapie, Chemotherapie, anti-HER2-gerichtete Therapie, Immuntherapie sowie zielgerichtete Substanzen (z.B. CDK4/6- oder PARP-Inhibitoren). Die Therapieentscheidung erfolgt interdisziplinär unter Berücksichtigung von Tumorstadium, Grading, molekularem Subtyp, Menopausenstatus, genetischer Prädisposition, Komorbiditäten und Patientinnenpräferenz. Systemische Therapien können im kurativen Setting neoadjuvant oder adjuvant sowie auch palliativ eingesetzt werden.
Neoadjuvante Systemtherapie
Die neoadjuvante Therapie wird vor der Operation durchgeführt und ist heute bei biologisch aggressiveren Subtypen Standard. Ziele sind die Tumorverkleinerung und Erhöhung der Rate brusterhaltender Operationen, das Erreichen einer pathologischen Komplettremission (pCR), eine frühe Beurteilung des Therapieansprechens sowie eine prognostische Stratifikation anhand des Residualtumors. Indikationen sind:
- HER2-positives Mammakarzinom ≥ cT2 oder nodal positiv
- triple-negatives Mammakarzinom ≥ cT2 oder nodal positiv
- lokal fortgeschrittene Tumoren
- inflammatorisches Mammakarzinom
Beim hormonrezeptorpositiven, HER2-negativen Tumor wird eine primäre Operation häufig bevorzugt; eine neoadjuvante Chemotherapie kann jedoch bei hohem Risiko sinnvoll sein.
| Typ | Therapie |
|---|---|
| HER2-positives Mammakarzinom |
|
| Triple-negatives Mammakarzinom |
|
| HR-positives, HER2-negatives Mammakarzinom |
|
Adjuvante Systemtherapie
Die adjuvante Therapie dient der Eliminierung mikroskopischer Tumorreste und der Senkung des Rezidivrisikos:
| Therapie | Hinweise |
|---|---|
| Endokrine Therapie |
|
| Chemotherapie |
|
| Anti-HER2-Therapie |
|
| CDK4/6-Inhibition |
|
...bei metastasiertem Mammakarzinom
Im metastasierten Stadium ist die Therapie in der Regel palliativ ausgerichtet. Ziele sind Lebensverlängerung, Symptomkontrolle und Erhalt der Lebensqualität. Die Therapiestrategie richtet sich primär nach dem molekularen Subtyp. Eine primäre operative Therapie ist im metastasierten Setting nicht Standard und erfolgt nur in ausgewählten Situationen.
| Subtyp | Therapie |
|---|---|
| HR+/HER2- |
|
| HER2+ |
|
| Triple-negativ |
|
Nebenwirkungen
Systemische Therapien sind mit charakteristischen Nebenwirkungen verbunden, u.a.:
- Kardiotoxizität unter HER2-Therapie
- Osteoporose unter Aromatasehemmern
- Endometriumkarzinomrisiko unter Tamoxifen
- Myelosuppression und Neuropathie unter Chemotherapie
Vor Einleitung einer Chemotherapie sollte bei bestehendem Kinderwunsch eine Beratung zur Fertilitätserhaltung erfolgen.
Prophylaxe
Jede Frau sollte einmal im Monat selbst die Brust schematisch abtasten. Der optimale Zeitpunkt liegt kurz nach der Menstruation. Ab dem 30. Lebensjahr sollte eine jährliche Tastuntersuchung durch den Arzt erfolgen.
Zwischen dem 35. und 40. Lebensjahr wird eine einmalige Mammographie empfohlen, die sogenannte Basis-Mammographie, die für spätere Aufnahmen als Vergleichsaufnahme dient. Vom 50. bis 69. Lebensjahr sollte dann alle 2 Jahre eine Mammographie durchgeführt werden. Bei Risikopatienten wird sie jährlich empfohlen.
Nachsorge
- In den ersten 3 Jahren nach Behandlung des Primärtumors vierteljährliche Kontrolle
- Ab dem 4. Jahr postoperative Kontrollen alle 6 Monate
- Ab dem 6. Jahr dann jährliche Kontrollen
Fallbeispiel
Leitlinie
Quellen
- ↑ Breast Cancer Association Consortium;Breast Cancer Risk Genes — Association Analysis in More than 113,000 Women; NEJM January 20, 2021; DOI: 10.1056/NEJMoa1913948
- ↑ S3-Leitlinie Mammakarzinom (Stand 2026)
- ↑ Gogiashvili, M. et al.; Impact of intrattumoral heterogenity of breast cancer tissue on quantitative metabolomics using high-resolution magic angle spinning. H NMR spectroscopy.; WILEY NMR in Biomedicine 2018; 31:e3862 (14 Seiten)
- ↑ Mei W et al. A commonly inherited human PCSK9 germline variant drives breast cancer metastasis via LRP1 receptor. Cell. 2025
Literatur
- Eucker, J. / Possinger K.; Mammakarzinome: Adjuvante Situation; Der Bayerische Internist 29 (2009). H.3, S.123-130.
- Regierer, A. C. / Bolbrinker, J. / Possinger, K.; Individualisierung der systemischen Therapie beim Mammakarzinom; Der Bayerische Internist 29 (2009). H.3, S.141-144.
- Wittekind C., Meyer H. J. (Ed); TNM Klassifikation maligner Tumoren; Weinheim: Wiley- Blackwell; 2010.
- Romagnolo A. P., Romagnolo D. F., Selmin O. I.; BRCA1 as target for breast cancer prevention and therapy; Anticancer Agents Med Chem. 2015;15(1):4-14.
- Paul A., Paul S.: The breast cancer susceptibility genes (BRCA) in breast and ovarian cancers; Front Biosci (Landmark Ed). 2014 Jan 1;19:605-18.
- Howell A., Anderson A. S., Clarke R. B., Duffy S. W., Evans D. G., Garcia-Closas M., Gescher A. J., Key T. J., Saxton J. M., Harvie M. N.; Risk determination and prevention of breast cancer; Breast Cancer Res. 2014 Sep 28;16(5):446; DOI: 10.1186/s13058-014-0446-2.
- Pschyrembel Online; Plateauphänomen; aufgerufen am 06.09.2021.
- Weyerstahl T. et al.; Duale Reihe - Gynäkologie und Geburtshilfe; Georg Thieme Verlag KG, 2014.