Sepsis
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
Loslegenvon altgriechisch: σήψη ("sipsi") - Fäulnis
Synonym: Blutvergiftung (Laienbegriff)
Englisch: sepsis
Definition
Die Sepsis ist ein lebensbedrohliches Multiorganversagen, dem eine fehlgesteuerte systemische Immunreaktion zugrunde liegt, die durch eine Infektion mit Krankheitserregern ausgelöst wird. Dabei handelt es sich meist um Bakterien, es können aber auch Viren, Pilze oder Parasiten ursächlich sein.
Hintergrund
Die Definition der Sepsis ist uneinheitlich und Gegenstand laufender Diskussionen. Aktuell (2026) gibt es keinen international akzeptierten "Goldstandard".[1]
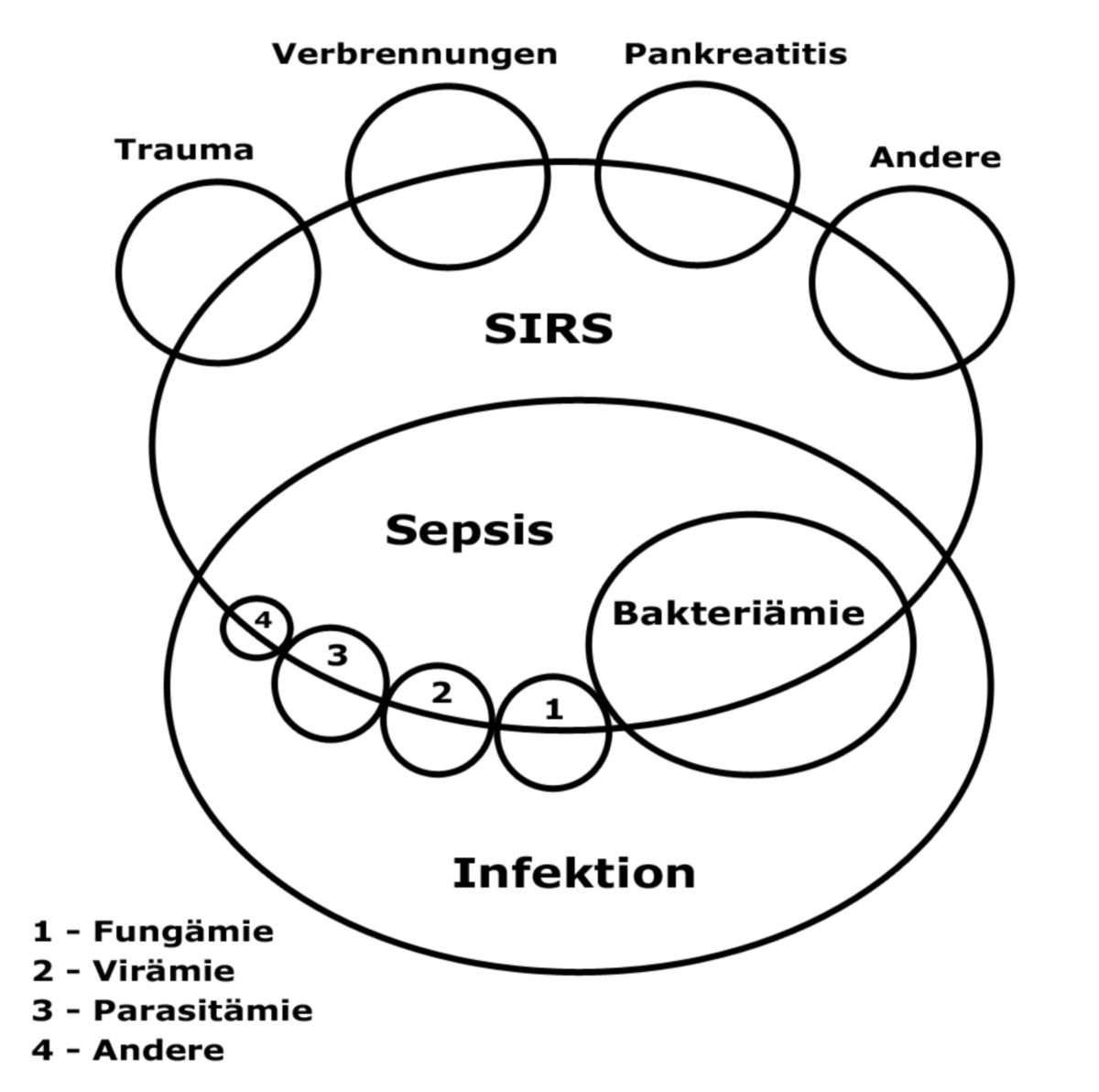
Ältere Definitionen basieren vor allem auf dem Nachweis von Krankheitserregern im Blut ("Bakteriämie"). Nach den Empfehlungen einer Konsensuskonferenz des American College of Chest Physicians (ACCP) und der Society of Critical Care Medicine (SCCM) aus dem Jahr 1991 liegt eine Sepsis vor, wenn ein systemisches inflammatorisches Response-Syndrom (SIRS) besteht und klinisch oder mikrobiologisch eine Infektion nachgewiesen werden kann. Diese Definition gilt mittlerweile als überholt, da die SIRS-Kriterien weder spezifisch, noch besonders sensitiv für eine Infektion sind.[1]
Schuster und Werdan (2005) definieren Sepsis wie folgt: "Sepsis ist die Gesamtheit der lebensbedrohlichen klinischen Krankheitserscheinungen und pathophysiologischen Veränderungen als Reaktion auf die Aktion pathogener Keime und ihrer Produkte, die aus einem Infektionsherd in den Blutstrom eindringen, die großen biologischen Kaskadensysteme und spezielle Zellsysteme aktivieren und die Bildung und Freisetzung humoraler und zellulärer Mediatoren auslösen".[2]
Der Sepsis-3-Konsensus aus dem Jahr 2016 schlug vor, dass die Sepsis ein lebensbedrohendes (Multi-)Organversagen ist, das durch eine fehlgesteuerte Immunreaktion des Wirts auf eine Infektion ausgelöst wird. Die Definition nimmt dabei Abstand von den ursprünglich dominanten SIRS-Kriterien und basiert stattdessen auf dem SOFA-Score als Ausdruck der Sepsis-assoziierten Organdysfunktion. Definitionsgemäß muss bei einer Sepsis ein Anstieg des SOFA-Scores um 2 oder mehr Punkte vorliegen.[3][4] Die aktuelle deutsche S3-Leitlinie folgt dieser Definition (Stand 2026).
Einteilung
Grundsätzlich unterscheidet man zwischen:
- Bakteriämie
- Sepsis
- Pyämie bzw. Septikopyämie
- SIRS
Man kann zusätzlich nach Entstehung und Art der Sepsis unterscheiden:
- Urosepsis (z.B. bei Pyelonephritis)
- Kathetersepsis/Fremdkörpersepsis (z.B. durch Venenkatheter)
- Sepsis bei Wundinfekt
- Sepsis bei Knochenmarkinsuffizienz
- Cholangiosepsis (z.B. bei Gallensteinen)
- Tonsillogene Sepsis
- Sepsis bei Endokarditis
- Neugeborenensepsis
Pathophysiologie
Eine Sepsis entsteht durch eine fehlregulierte Wirtsantwort auf eine Infektion. Ihre zentralen Elemente sind eine Fehlregulation von pro- und antiinflammatorischen Abläufen und eine endotheliale Dysfunktion. Auslöser sind pathogene Erreger oder ihre Toxine, die eine systemische Immunreaktion anstoßen – unabhängig davon, ob sie im Blutkreislauf nachweisbar sind oder nicht.
Normalerweise ist das Immunsystem des Körpers in der Lage, diese lebensbedrohliche Störung zu verhindern, so dass erst eine bestimmte Konstellation begünstigender Faktoren vorhanden sein muss. Zu ihnen zählen zum Beispiel:
- gestörte Immunabwehr
- massive Infektion mit hoher Erregeranzahl
- gesteigerte Pathogenität der Erreger
- Infektion schlecht abgrenzbarer Körperregionen (z.B. Abdomen)
Nach der traditionellen Vorstellung verläuft eine Sepsis in drei Phasen:
- In der Initialphase liegt unbehandelt ein hypodynames Initialstadium vor ("kalter Schock"). Typische Zeichen sind eine Hypotonie, ein niedriges Herzzeitvolumen und ein erhöhter systemischer Gefäßwiderstand:
- Durch Entzündungsmediatoren kommt es anschließend zu einer Vasodilatation mit Reduktion des systemischen Widerstands. Dieses hyperdyname Schockstadium führt zu einem relativen intravasalen Volumenmangel. In einigen Fällen entsteht eine erhöhte Gefäßpermeabilität, die mit einem zusätzlichen absoluten Volumenmangel einhergeht. Typisch für diese Phase ist ein kompensatorisch gesteigertes Herzzeitvolumen. Der gesteigerte Katecholaminspiegel, die gestörte myokardiale Mikrozirkulation und eine verminderte Empfindlichkeit der kardialen β-Rezeptoren sorgen jedoch für eine relative Herzinsuffizienz (akute septische Kardiomyopathie).
- Bei einem Teil der Patienten kommt es im Verlauf der Sepsis zur Dekompensation in eine hypodyname Schockphase: Das Herzzeitvolumen sinkt, der Gefäßwiderstand steigt erneut an. Unbehandelt führt die Gewebshypoxie infolge der Mikrozirkulationsstörung zum (Multi-)Organversagen, insbesondere der Lunge, Niere und Leber.
Dieser streng dreiphasige Modellverlauf gilt heute (2026) als überholt, da viele Patienten von Beginn an eine hyperdyname Kreislaufsituation zeigen. Die Abläufe einer Sepsis können interindividuell sehr verschieden sein.
Erreger
Eine Sepsis kann durch eine Vielzahl verschiedener Erreger ausgelöst werden. Hauptverantwortliche Bakterien für eine Sepsis sind – nach Häufigkeit sortiert:
- Staphylococcus aureus
- Escherichia coli
- Bakterien der Gattungen Klebsiella, Enterobacter, Serratia
- Pseudomonas spp.
- Streptococcus viridans, Enterococcus faecalis und Streptococcus pneumoniae
Bei immunsupprimierten Patienten ist das in Frage kommende Erregerspektrum deutlich größer, da hier auch Mikroorganismen pathogen werden können, die bei immunkompetenten Personen keine Rolle spielen.
Leitsymptome
- warme, trockene Haut in der hyperdynamen Phase
- blasse, kühle Haut während der hypodynamen Phasen
- intermittierendes hohes Fieber
- Tachypnoe
- Oligurie bis Anurie
- Bewusstseinsstörungen (Verwirrtheit, Unruhe, Somnolenz)
- Diarrhoen
- Nausea, Erbrechen
- Schüttelfrost
- Tachykardien
- Hypotension
- Schock
Immunsupprimierte Patienten zeigen oft weniger klassische Entzündungszeichen (z.B. Fieber, Rötung), die pathophysiologischen Reaktionen (z.B. Tachykardie, Tachypnoe) treten jedoch in der Regel trotzdem auf.
siehe auch: SIRS, Septischer Schock, Bakteriämie
Diagnose
Die rechtzeitige Identifizierung der Sepsis ist wichtig, da eine frühzeitige Therapie das Überleben wesentlich verbessern kann.[1] Da die Symptome häufig unspezifisch und heterogen sind, wird die Anwendung von Screening-Instrumenten empfohlen. Bisher (2026) gibt es keine ausreichende Evidenz für die Verwendung eines bestimmtes Screening-Instruments. Häufig genutzt werden z.B.:
- qSOFA-Score
- NEWS
- SIRS-Kriterien
Neben klinischen und organspezifischen Untersuchungen umfasst die Diagnostik vor allem die Fokussuche und Mikrobiologie (Blutkulturen). Die Fokussuche lässt sich durch das Akronym LUCCAASS strukturieren.
Labormedizinisch werden u.a. folgende Parameter bestimmt:
Diagnosekriterien
Die aktuellen Diagnosekriterien unterscheiden nicht mehr zwischen leichter und schwerer Sepsis.[1][5] Definiert wird die Sepsis durch eine lebensbedrohliche Organdysfunktion durch eine inadäquate Wirtsantwort auf eine Infektion. Das Vorhandensein von positiven SIRS-Kriterien kann zur Diagnosestellung herangezogen werden, ist aber keine notwendige Bedingung.
Nachweis eines infektiösen Ursprungs der Inflammation
Der Nachweis gelingt z.B. durch:
- mikrobiologisch gesicherte Infektion
- klinisch gesicherte Infektion
- Procalcitonin > 2,0 µg/l
Infektionsbezogene lebensgefährliche Organdysfunktion
Voraussetzung ist ein Anstieg des SOFA-Scores um mindestens zwei Punkte, der sich durch folgende Organschäden äußern kann:
- Akute Enzephalopathie (reduzierte Vigilanz, Unruhe, Desorientiertheit, Delir ohne Beeinflussung durch Psychotropika)
- Thrombozytopenie (Thrombozyten < 150.000/µl ohne Blutverlust als Ursache)
- Arterielle Hypoxämie (paO2/FiO2 < 400 mmHg ohne manifeste pulmonale o. kardiale Erkrankung als Ursache)
- Arterielle Hypotension (mittlerer arterieller Blutdruck < 70 mmHg über mind. 1 Stunde trotz adäquater Volumenzufuhr bei Abwesenheit anderer Schockursachen)
- Renale Dysfunktion (Serumkreatinin > 1,2 mg/dl)
- Leberfunktionsstörung (Bilirubin > 1 mg/dl)
Verlaufparameter
Wichtige Verlaufsparameter bei einer Sepsis sind u.a.
- Blutkulturen
- RR, wenn möglich kontinuierlich (arterielle Druckmessung), mittlerer arterieller Druck (MAP) ≥ 65 mmHg
- zentralvenöse O2-Sättigung
- ZVD (zentralvenöser Druck) > 8–12 mmHg
- Wedge-Druck (PCWP = Pulmonary Capillary Wedge Pressure, Verschlussdruck)
- Lungenödem
- Lungenfunktion: pO2/FiO2-Verhältnis
- Peripherer Widerstand (Nachlast, afterload, total vascular resistance, TVR)
- Nierenfunktion: Kreatinin
- Hb, Hämatokrit > 24–30 % (Hb 8–10 g/dL)
- Harnstoff (Anstieg bei gleichbleibendem Kreatinin → Hinweis auf katabole Stoffwechsellage)
- DIC: Thrombozyten
- Glasgow Coma Scale
- Leberfunktion: Bilirubin
- Gewebsoxygenierung: Lactat
- Glucose
- Procalcitonin
Therapie
Sepsis-Patienten sollten intensivmedizinisch behandelt und überwacht werden. Die sogenannten "Sepsis-Bündel" fassen die wichtigsten Maßnahmen zusammen:[6]
- Innerhalb der ersten drei Stunden:
- Messung Laktat-Spiegel
- Blutkulturen vor Antibiotikagabe, dann Breitspektrum-Antibiotika (möglichst innerhalb der ersten Stunde)[1]
- Elektrolytlösungen (30 ml/kgKG) bei Hypotension oder Laktat über 4 mmol/l
- Innerhalb der ersten sechs Stunden:
- Vasopressoren, falls die Hypotension nicht auf eine initiale Volumengabe anspricht, um einen mittleren arteriellen Blutdruck (MAP) von über 65 mmHg zu erzielen
- Bei anhaltender Hypotension nach initialer Volumengabe oder initialem Laktat über 4 mmol/l erneute Beurteilung des Volumenstatus und Gewebeperfusion (kapilläre Füllungszeit, Pulsqualität, Hautbefund, ZVD-Messung, Echokardiographie etc.)
Initiale Kreislaufstabilisierung
Innerhalb der ersten drei Stunden werden Elektrolytlösungen infundiert (mindestens 30 ml/kgKG). Die weitere Volumengabe ist abhängig von der Hämodynamik. Eine Zielwert-orientierte Gabe (early-goal directed therapy, EGDT) der Leitlinien 2012 (unter anderem ZVD 8 - 12 mmHg) wird nicht mehr gefordert, da neuere Studien den Stellenwert der EGDT nicht bestätigen konnten. Wird im Rahmen der initialen hämodynamischen Stabilisierung durch die Volumentherapie kein ausreichender MAP (<65 mmHg) erreicht, wird mittlerweile die überbrückende Gabe eines Vasopressors auch periphervenös vorgeschlagen, wenn noch kein zentraler Venenkatheter gelegt wurde (Stand 2026).[1]
Antimikrobielle Therapie
Die antimikrobielle Therapie sollte möglichst innerhalb der ersten Stunde nach Diagnose eines septischen Schocks begonnen werden. Liegt keine Schocksymptomatik vor, wird eine Gabe innerhalb von drei Stunden vorgeschlagen.[1]
Das Untersuchungsmaterial für Blutkulturen (mindestens 2 Blutkultur aus peripheren Venen und je eine aus jedem Lumen jedes Gefäßzuganges älter als 48 Stunden) sowie gegebenenfalls weitere Kulturen (z.B. Urin, Wundsekret, Bronchialsekret) soll vorher gewonnen werden. Allerdings darf die Probengewinnung die antimikrobielle Therapie nicht wesentlich verzögern![1]
Empirisch wird ein Breitspektrumantibiotikum intravenös verabreicht. Eine routinemäßige Gabe von zwei verschiedenen gegen gramnegative Erreger wirksamen Antibiotika bei Patienten ohne Risiko für einen multiresistenten Erreger ist nicht empfohlen. Auch Antimykotika bzw. Virustatika sollen nur bei hohem Risiko für eine entsprechende Infektion verabreicht werden. Für die Verwendung von Beta-Laktam-Antibiotika (z.B. Piperacillin plus Tazobactam) wird nach Gabe des initialen Bols eine prolongierte oder kontinuierliche Infusion empfohlen.[1]
Meist ist eine Therapiedauer von 7 bis 10 Tagen ausreichend. Procalcitonin-Spiegel sind hilfreich, den möglichen Endzeitpunkt einer antimikrobiellen Therapie zu erkennen.
Fokuskontrolle
Eine zügige Diagnose und Beseitigung des septischen Fokus ist entscheidend. Falls intravaskuläre Katheter eine potenzielle Sepsisquelle darstellen, müssen sie entfernt werden.
Volumentherapie
Bei schwerer Sepsis bzw. septischem Schock werden Elektrolytlösungen empfohlen. HAES oder Gelatine werden nicht mehr verwendet. Falls notwendig, kann Humanalbumin zusätzlich gegeben werden. Die Volumengabe erfolgt solange, bis sich die Hämodynamik bessert. Zur Beurteilung sind dynamische Verfahren geeignet (z.B. Schlagvolumenvariation).
Vasopressoren und Inotropika
Ziel ist ein mittlerer arterieller Blutdruck von über 65 mmHg. Als Vasopressor der Wahl wird Noradrenalin eingesetzt. Falls nicht ausreichend, kann zusätzlich Vasopressin eingesetzt werden. Als Ultima ratio kommt Adrenalin zum Einsatz. Dopamin wird nicht mehr empfohlen. Bei anhaltender Hypoperfusion aufgrund einer kardialen Dysfunktion trotz Volumen- und Vasopressorgabe kann Dobutamin erwogen werden.
siehe auch: Katecholamintherapie
Glukokortikoide
Niedrigdosiertes Hydrocortison (200 mg/d i.v.) kann bei anhaltendem Vasopressorbedarf (Noradrenalin ≥ 0,25 µg/kg/min) angewendet werden. Es wirkt antiinflammatorisch und reduziert den Vasopressorbedarf. Für Dexamethason und hochdosierte Glukokortikoide gibt es keine Empfehlung.
Blutprodukte
Bei einer Hämoglobinkonzentration unter 7,0 g/dl sollten Erythrozytenkonzentrate gegeben werden (Ziel-Hb 7,0 - 9,0). Erythropoetin oder Antithrombin III sind nicht empfohlen. Fresh Frozen Plasma kommt nur bei Blutungen oder invasiven Eingriffen in Frage. Thrombozytenkonzentrate kommen bei einer Thrombozytenzahl unter 10.000/mm3 oder unter 20.000 bei hohem Blutungsrisiko zum Einsatz. Bei aktiver Blutung, Operation oder invasivem Eingriff wird eine Thrombozytenzahl von über 50.000 gefordert.
Sonstige Aspekte
- allgemein gilt die Tarragona-Strategie
- Bei Sepsis-induziertem ARDS ist eine Beatmung notwendig:
- Tidalvolumen von 6 ml/kgKG, oberes Druckniveau unter 30 cmH2O bei Erwachsenen, höherer PEEP zum Vermeiden von Atelektasen
- Leichte Hyperkapnie wird toleriert
- Bauchlage (prone over supine position) und Lagerungstherapie bei Oxygenierungsindex unter 150 mmHg
- bei maschineller Beatmung 30 bis 45° Oberkörperhochlagerung zur Vermeidung von Aspiration und Ventilator-assoziierter Pneumonie
- Adäquate Analgesie
- Eine Sedierung sollte insbesondere bei Beatmungspatienten minimiert werden; falls notwendig tägliche Unterbrechung
- Blutzuckerkontrolle: intravenöse Insulingabe bei einem Blutzucker über 180 mg/dl mit Zielwert unter 180 mg/dl; Messung alle 1 bis 2 Stunden bis stabil, dann alle 4 Stunden
- Hämodialyse oder Hämofiltration bei Sepsis mit akutem Nierenversagen
- Venöse Thrombembolieprophylaxe
- Niedermolekulares Heparin sofern keine aktive Blutung oder eine HIT vorliegt
- Alternativ unfraktioniertes Heparin (insbesondere bei hochgradiger Niereninsuffizienz)
- Stressulkusprophylaxe bei Risikofaktoren für eine gastrointestinale Blutung, in der Regel mit Protonenpumpenhemmer
- Ernährung:
- Immer enterale Ernährung einer parenteralen Ernährung vorziehen
- Erste Tage falls möglich niederkalorisch Ernährung mit Glukose i.v. und enteraler Kost
- Keine Empfehlung für Omega-3-Fettsäuren, Selen i.v., Glutamin oder Arginin
- Bikarbonat wird nur noch bei einer metabolischen Azidose mit pH-Wert unter 7,15 eingesetzt
- Intravenöse Immunglobuline werden nicht empfohlen
Prognose
Die Prognose der Sepsis ist von verschiedenen Faktoren abhängig. Hierzu zählen insbesondere:
- der Schweregrad und die Persistenz der Organdysfunktion
- das Vorliegen eines septischen Schocks
- Alter und Komorbiditäten des Patienten
- die Zeit bis zur Einleitung einer adäquaten Therapie
- der Infektionsfokus und das Erregerspektrum
Die Mortalität variiert erheblich in Abhängigkeit von Setting, Population und Definition. Sie liegt in Deutschland bei ca. 26 %, im septischen Schock kann sie sogar über 40 % betragen.[7]
Ein entscheidender prognostischer Faktor ist die Zeit bis zur initialen antimikrobiellen Therapie sowie zur adäquaten Fokuskontrolle.
Nachsorge
Überlebende einer Sepsis können langfristige gesundheitliche Beeinträchtigungen aufweisen, die als Post-Sepsis-Syndrom bezeichnet werden. Zu den typischen Beschwerden zählen:
- körperliche Einschränkungen, z.B. Muskelschwäche und reduzierte Belastbarkeit
- kognitive Defizite, z.B. Gedächtnisstörungen und Aufmerksamkeitsstörungen
- psychische Erkrankungen, z.B. Depression, Angststörung oder posttraumatische Belastungsstörung
Zusätzlich besteht ein erhöhtes Risiko für eine Rehospitalisierung und erneute Infektionen. Die Nachsorge umfasst daher vor allem
- strukturierte ärztliche Verlaufskontrollen,
- frühzeitige Rehabilitation in physischer und kognitiver Hinsicht,
- psychosoziale Betreuung und
- die Optimierung der Therapie von Komorbiditäten.
Empfohlen wird ein interdisziplinärer Ansatz unter Einbeziehung von Hausarzt, Intensivmedizin und Rehabilitationseinrichtungen.
Podcast

Bildquelle
- Bildquelle LightLinie: © Anne Nygård / / Unsplash
Quellen
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 1,8 DSG (Deutsche Sepsis-Gesellschaft), DGAI (Deutsche Gesellschaft für Anästhesiologie und Intensivmedizin), DIVI (Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin et al. (2025): S3-Leitlinie: Sepsis – Prävention, Diagnose, Therapie und Nachsorge – Update 2025. Langfassung. Version: 4.0, Stand: 30.04.2025. (Zugriffsdatum: 29.07.2025).
- ↑ Schuster HP, Müller-Werdan U: Definition und Diagnose von Sepsis und Multiorganversagen in Sepsis und MODS, Springer Verlag Berlin Heidelberg (2005)
- ↑ Mervyn S et al.: The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3) JAMA. 2016;315(8):801-810. doi:10.1001/jama.2016.0287
- ↑ Epidemiologisches Bulletin, RKI, 9/2017
- ↑ Deutsch Sepsis Gesellschaft: Sepsis-3 Kodierung und Definition, zuletzt abgerufen am 29.07.2025
- ↑ Surviving Sepsis Campaign (SSC) International Guidelines für Management of Sepsis and Septic Shock 2016, abgerufen am 09.07.2019
- ↑ Bauer et al.: Sterblichkeit bei Sepsis und septischem Schock in Deutschland. Ergebnisse eines systematischen Reviews mit Metaanalyse. Der Anaesthesist, 2021
Literatur
- Deutsche Sepsis-Gesellschaft et al., S3-Leitlinie Sepsis – Prävention, Diagnose, Therapie und Nachsorge, 2025
- Evans et al., Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock 2026, 2026