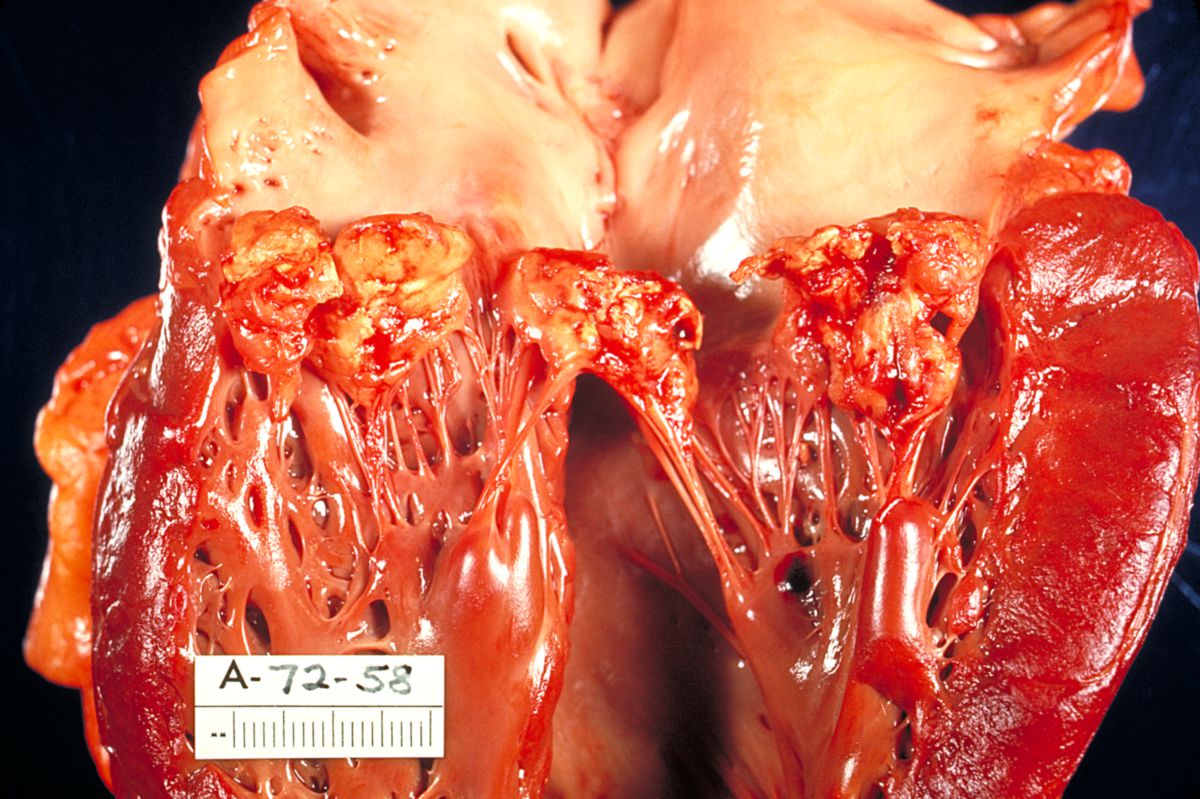
Endokarditis
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
Loslegenvon altgriechisch: ἔνδον ("éndon") - innen; καρδία ("kardia") - Herz
Synonyme: Endocarditis, Endokardentzündung, Herzinnenhautentzündung
Englisch: endocarditis
Definition
Die Endokarditis ist eine im Rahmen verschiedener krankhafter Prozesse auftretende Entzündung der Herzinnenhaut (Endokard).
ICD10-Codes
- I01.1: Akute rheumatische Endokarditis
- I09.1: Rheumatische Krankheiten des Endokards, Herzklappe nicht näher bezeichnet; chronisch-rheumatische Endokarditis
- I33: Akute und subakute Endokarditis
- I38: Endokarditis, Herzklappe nicht näher bezeichnet
Systematik
Endokarditiden lassen sich nach verschiedenen Kriterien klassifizieren.
...nach Ätiologie
Die gängigste Einteilung erfolgt nach der Ätiologie. Demnach wird zwischen den folgenden Formen eine Endokarditis unterschieden:
- Nicht-infektiöse (abakterielle) Endokarditis
- Antigen-Antikörper-Reaktionen
- Endocarditis rheumatica (verrucosa): Klassische Form der nicht-infektiösen Endokarditis, die meist ca. 2 Wochen nach einer Infektion mit beta-hämolysierenden A-Streptokokken warzenähnliche Auflagerungen (Fibrin, Thrombozyten) v.a. in den Schließungsrändern der Mitral- oder Aortenklappe auftreten. Die Endokarditis rheumatica ist Teilerscheinung einer Perikarditis bzw. des rheumatischen Fiebers.
- Ablagerung von Immunkomplexen
- Endokarditis Libmann-Sacks bei systemischem Lupus erythematodes (SLE): Abakterielle Endokarditis mit größeren Fibrinablagerungen auf der Mitral-, aber auch an der Aorten- und Pulmonalklappe mit starker Neigung zur lokaler entzündlicher Infiltration. Häufig begleitet von Perikarditis oder Pleuritis.
- Zelluläre Immunreaktionen
- Löffler-Endokarditis: Endomyokarditis eosinophilica
- Endokarditis bei Karzinoid
- Antigen-Antikörper-Reaktionen
- Infektiöse Endokarditis bzw. infektive Endokarditiden (IE)
- Bakterielle Endokarditis
- Akute Endokarditis ("Endocarditis acuta")
- Subakute Endokarditis ("Endocarditis lenta")
- Virale Endokarditis
- Mykotische Endokarditis
- Bakterielle Endokarditis
- Mischformen
- Bakterielle Besiedlung eines abakteriell entstandenen Endokarditisherds (Superinfektion)
...nach Lokalisation
Auch die Lokalisation gibt Ansatzpunkte für eine Klassifikation:
- Endocarditis valvularis: Die überwiegende Zahl der Entzündungen tritt an den Herzklappen auf. Bakteriell akute Endokarditiden (Endocarditis ulcerosa acuta), zumeist durch Staphylococcus aureus verursacht, rufen häufig gelbgrüne Vegetationen im Bereich des Schlussrandes der Herzklappen hervor.
- Endocarditis parietalis: In selteneren Fällen kann auch die Wand der Atrien und Ventrikel betroffen sein.
...nach Aspekt
In der Pathologie werden Endokarditiden auch nach ihrem makroskopischen Aspekt unterschieden, z.B. in:
- Endocarditis serosa: Rötlich glasige Aufquellung der Herzklappe
- Endocarditis ulcerosa: Entzündungsreaktion mit Bildung von Ulzerationen
- Endocarditis polyposa: Polypenartige Wucherungen des Endokards
- Endocarditis ulceropolyposa: Mischform aus Polypen und Ulzerationen
- Endocarditis verrucosa: Warzenförmige Gewebeveränderungen am Schlussrand der Herzklappen.
Ätiologie
Die Entstehung der Endokarditiden ist ein multifaktorielles Geschehen und bei den verschiedenen Unterformen unterschiedlich. Ursächlich ist üblicherweise eine Veränderung von Blutfluss und Blutgerinnung mit der Entstehung von nichtbakteriellen thrombotischen Vegetationen (NBTV). In diesen Bereichen von Blutaggregaten und Endothelschäden kann es dann zu einer Ablagerung von Immunkomplexen oder zu einer Besiedlung mit Krankheitserregern kommen. Im weiteren Verlauf kann dann die Zerstörung von Herzklappen, Herzinnenhaut, Papillarmuskeln und Chordae tendineae folgen.
Die infektiöse Endokarditis (IE), verursacht durch hoch virulente Bakterien wie Staphylococcus aureus, setzt keine kongenitalen Anomalien der Herzklappen oder erworbene Herzklappenfehler voraus. Die akute Form der IE kann auch an zuvor gesunden Herzklappen entstehen. Ausgehend von Lokalinfektionen (z.B. kontaminierten Wunden) gelangen die Bakterien ins Blut und bilden so die Grundlage für eine infektiöse Endokarditis.
Häufig treten infektiöse Endokarditiden bei Drogenabhängigen mit intravenösem Konsum auf. In diesen Fällen ist der Verlauf oft perakut, wobei es sich meist um eine rechtsseitige Endokarditis handelt. Bei diesen Patienten besteht bei fortdauerndem Konsum eine hohe Rezidivgefahr.
Auch eine verminderte Immunabwehr, z.B. nach einer Chemotherapie oder bei einer HIV-Infektion, begünstigt das Auftreten einer infektiösen Endokarditis.
Symptomatik
Die Symptome einer Endokarditis hängen von der Art der Entzündung sowie vom Ausmaß der Zerstörungen ab. Neben allgemeinen Zeichen einer Infektion können Symptome einer valvulären oder ischämischen Herzinsuffizienz auftreten.
Das klinische Bild eines Patienten mit akuter infektiöser Endokarditis sieht wie folgt aus:
- Fieber, evtl. Schüttelfrost (in ca. 80 bis 90 % der Fälle)
- Herzgeräusche und Tachykardie (in ca. 80 bis 85 % der Fälle), zunehmende Zeichen einer Herzinsuffizienz
- Kältegefühl und Nachtschweiß (in ca. 40 bis 75 % der Fälle)
- Anorexie, Gewichtsverlust, sowie Unbehagen (in ca. 25 bis 50 % der Fälle), Arthralgien, Anämie
- Periphere Manifestationsformen: Roth-Flecken, Osler-Knötchen, Janeway-Läsionen sowie subunguale Hämorrhagien/Splinter-Hämorrhagien, Petechien (in 2 bis 15% der Fälle)
- Nierenbeteiligung mit Hämaturie, Proteinurie: Glomeruläre (Löhlein-) Herdnephritis, Niereninfarkte im Rahmen embolischer Ereignisse
- Es besteht erhöhte Emboliegefahr: Embolische Herdenzephalitis (Bewusstseinseintrübung), evtl. mit Hemiparesen, evtl. Mikroembolien an der Retina (Roth-Flecken)
Diagnostik
Duke-Kriterien
Zur Diagnostik der infektiösen Endokarditis können die 2023 aktualisierten Duke-Kriterien angewendet werden. Sie umfassen Haupt- und Nebenkriterien.
Es handelt sich definitiv um eine Endokarditis, wenn:
- 2 Hauptkriterien oder
- 1 Hauptkriterium und 3 Nebenkriterien oder
- 5 Nebenkriterien
erfüllt werden.
Es handelt sich wahrscheinlich um eine Endokarditis, wenn:
- Haupt- oder Nebenkriterien vorliegen, die aber die oben genannten Bedingungen noch nicht vollständig erfüllen
- 3 Nebenkriterien erfüllt werden
Hauptkriterien
Mikrobiologisch
- Mindestens zwei positive Blutkulturen mit typischen Erregern
- Nachweis von Mikroorganismen mittels molekularbiologischer Verfahren (z.B. PCR, Metagenomik oder IFA) aus Herzgewebe oder prothetischem Material
Bildgebung
- Positiver Echo-Befund (flottierende Vegetation, Abszess, neue Klappeninsuffizienz, etc.)
- FDG-PET/CT mit anomaler Stoffwechselaktivität an nativen oder prothetischen Herzklappen, an aufsteigendem Aortentransplantat, an intrakardialen Ableitungen oder anderem prothetischen Material
Chirurgisch/Intraoperativ
- Direkter intraoperativer Nachweis einer aktiven Endokarditis (z.B. Vegetationen, Klappen- oder Nahtkomplikation) bei Operation oder an explantiertem Material
Nebenkriterien
Zu den Nebenkriterien zählen:
- Prädisposition (z.B. Vitien, Zustand nach prothetischem Klappenersatz, andere strukturelle Herzveränderungen, die eine Keimabsiedlung begünstigen sowie i.v.-Medikation oder i.v.-Drogenabusus)
- Fieber ≥ 38 °C
- Gefäßphänomene (z.B. Embolien, zerebrale oder splenische Abszesse, mykotische Aneurysmen und Janeway-Läsionen)
- Immunologische Phänomene (z.B. positives Rheumafaktor-Ergebnis, Osler-Knötchen, Glomerulonephritis)
- Mikrobiologischer Nachweis: positive Blutkultur oder serologischer/molekularer Erregernachweis, der nicht die Anforderungen eines Hauptkriteriums erfüllt
- Bildgebender Hinweis: echokardiografische oder PET/CT-Befunde, die verdächtig, aber nicht eindeutig sind (z.B. FDG-PET-Nachweis unter drei Monaten nach Herzoperation)
- Körperliche Untersuchung: klassische Haut- oder Schleimhautbefunde, die auf eine infektiöse Endokarditis hinweisen (z.B. Petechien oder Splinter-Hämorrhagien)
Bildgebung
Die transösophageale Echokardiographie gilt aufgrund der hohen Sensitivität als Basisdiagnostik. Ein unauffälliger Befund schließt eine Endokarditis jedoch nicht aus. Ergänzend kommen die FDG-PET/CT und die Leukozyten-SPECT/CT in Frage. Erstere sollte aufgrund falsch-positiver Befunde frühestens 3 Monate nach Klappenimplantation durchgeführt werden.
Labormedizin
Der Erregernachweis bei Endokarditis erfolgt mithilfe von Blutkulturen. Die Proben sind mit der Fragestellung "Endokarditis" zu kennzeichnen, da viele Labore in diesem Fall eine längere Bebrütung vornehmen, um langsam wachsende Bakterien nachzuweisen. Zudem werden folgende Parameter bestimmt:
Auch der Urinstatus kann erhoben werden.
Material
Für die Diagnostik können je nach Verfahren folgende Materialien benötigt werden:
- Blutkultur
- 4 ml EDTA-Blut
- 2 ml Serum
- 10 ml frischer Spontanurin
Häufige Erreger
Die Häufigkeit bestimmter Erreger ist abhängig vom Zeitpunkt nach Prothesenimplantation. In den ersten 2 Monaten ist Staphylococcus aureus für die meisten Fälle verantwortlich, gefolgt von koagulase-negativen Staphylokokken sowie deutlich seltener gramnegativen Bakterien und Candida-Spezies. Im Zeitraum von 2 bis 12 Monaten nach dem Eingriff sind Streptokokken, Staphylococcus aureus und koagulase-negative Staphylokokken die häufigsten Erreger, gefolgt von Enterokokken. Bei der späten Prothesenendokarditis (> 12 Monate) entspricht das Erregerspektrum dem der nativen Klappenendokarditis (Streptokokken und Staphylococcus aureus, gefolgt von Enterokokken und koagulasenegativen Staphylokokken).
Therapie
Die Therapie der infektiösen Endokarditis verfolgt das Ziel einer vollständigen Erregereradikation aus avaskulärem, fibrin- und thrombozytenreichem Vegetationsmaterial. Daraus ergibt sich die Notwendigkeit einer hochdosierten, bakteriziden und ausreichend langdauernden Antibiotikatherapie, die sich nach Erreger, Resistenzprofil, Klappentyp (native vs. prothetische Klappe), Infektionsdauer und Komplikationen richtet. Die Behandlungsdauer beträgt bei nativer Klappe meist 4–6 Wochen, bei prothetischer Endokarditis grundsätzlich ≥ 6 Wochen.[1] Nicht-infektiöse Endokarditiden werden z.B. mit Immunsuppressiva behandelt.
Empirische Initialtherapie
Die empirische Therapie wird unmittelbar nach Abnahme von Blutkulturen begonnen, sofern eine hohe klinische Wahrscheinlichkeit für eine infektiöse Endokarditis besteht. Ziel ist die rasche Abdeckung der wahrscheinlichsten Erreger mit einem bakteriziden, hochdosierten intravenösen Regime, bis Erregeridentifikation und Resistenztestung eine gezielte Deeskalation erlauben. Die Empfehlungen zur Auswahl des Antibiotikums sind uneinheitlich und werden kontrovers diskutiert.[2][1]
Bei ambulant erworbener nativer Klappenendokarditis ohne Hinweise auf nosokomiale Genese oder Fremdmaterial wird meist eine Kombination aus Ampicillin plus Flucloxacillin (oder Oxacillin) empfohlen. Bei erhöhtem MRSA-Risiko wird das Isoxazolylpenicillin durch Vancomycin ersetzt. Ein routinemäßiger Zusatz von Gentamicin wird bei nativer Endokarditis nicht mehr generell empfohlen, da kein gesicherter Mortalitätsvorteil besteht und relevante nephro- und ototoxische Risiken auftreten können.[2] Ein Aminoglykosid kann jedoch in ausgewählten Situationen (z.B. Enterokokkenverdacht oder schwere Sepsis) erwogen werden.
Bei nosokomialer nativer Endokarditis oder kritisch kranken Patienten wird Vancomycin plus ein Breitspektrum-β-Laktam mit Pseudomonas-Aktivität (z.B. Cefepim oder ein Carbapenem) eingesetzt.
Native Klappenendokarditis
Streptokokken
Bei penicillinsensiblen Streptokokken (z.B. Streptococcus viridans oder Streptococcus gallolyticus) ist ein β-Laktam-Antibiotikum Mittel der Wahl, da Streptokokken hochgradig empfindlich sind und β-Laktame eine exzellente bakterizide Wirkung bei guter Verträglichkeit besitzen. Standard ist Penicillin G, Amoxicillin oder Ceftriaxon für 4 Wochen. Der Zusatz eines Aminoglykosids dient der bakteriellen Synergie, ist jedoch nephrotoxisch und wird heute zurückhaltender eingesetzt. Bei relativer Penicillinresistenz ist eine 4-wöchige β-Laktam-Therapie plus initial 2 Wochen Gentamicin indiziert. Vancomycin ist Reserveoption bei schwerer β-Laktam-Allergie.
Staphylococcus aureus
Staphylococcus aureus verursacht meist aggressive Verläufe mit hoher Komplikationsrate. Bei MSSA ist Flucloxacillin (oder Oxacillin) Mittel der Wahl, da diese Substanzen β-Laktamasestabil sind und gegenüber Vancomycin eine überlegene bakterizide Aktivität aufweisen. Bei MRSA ist Vancomycin Standard, alternativ Daptomycin (insbesondere bei erhöhter Vancomycin-MIC oder Nephrotoxizität).
Enterokokken
Enterokokken (v.a. Enterococcus faecalis) sind intrinsisch weniger empfindlich gegenüber β-Laktamen. Eine Monotherapie ist nicht ausreichend bakterizid. Standard ist daher eine Kombinationstherapie, z.B. mit Ampicillin und Gentamicin. Aufgrund der Nephrotoxizität von Aminoglykosiden wird teilweise auch die duale β-Laktam-Therapie aus Ampicillin und Ceftriaxon eingesetzt. Bei Vancomycin-resistenten Enterokokken (VRE) kommen Linezolid oder hochdosiertes Daptomycin zum Einsatz.
Prothetische Klappenendokarditis
Die prothetische IE ist prognostisch ungünstiger, da Biofilm-Bildung auf Fremdmaterial die Antibiotikaempfindlichkeit reduziert. Daher ist die Therapie grundsätzlich prolongiert (≥ 6 Wochen) und häufig kombiniert.
Man unterscheidet eine frühe PVE (< 12 Monate nach Implantation) von einer späten Form, da das Erregerspektrum variiert. Die initiale kalkulierte Therapie umfasst typischerweise Vancomycin, plus ein Breitspektrum-β-Laktam und ggf. Gentamicin in der Initialphase. Bei gesichertem Staphylokokkenbefall wird zusätzlich Rifampicin eingesetzt, da es eine hohe Biofilmpenetration besitzt.
Pilzendokarditis
Selten, aber prognostisch ungünstig. Therapie besteht aus liposomalem Amphotericin B oder einem Echinocandin, meist in Kombination mit chirurgischer Sanierung. Eine alleinige konservative Therapie ist selten ausreichend.
Orale Step-down-Therapie
Bei stabilen Patienten ohne Komplikationen, mit sensiblen Erregern und gesicherter Adhärenz kann nach mindestens 10–14 Tagen effektiver intravenöser Therapie eine Umstellung auf hochbioverfügbare orale Kombinationen erfolgen (z. B. Amoxicillin + Rifampicin oder Linezolid-basierte Schemata). Voraussetzung sind stabile Echokardiographie, negative Blutkulturen und interdisziplinäre Entscheidung im Endokarditis-Team.
Chirurgische Therapie
Eine operative Intervention ist z.B. indiziert bei:
- akuter schwerer Klappeninsuffizienz mit Herzinsuffizienz,
- unkontrollierter Infektion (z.B. persistierende Bakteriämie, Abszess, Fistel)
- großen Vegetationen mit hohem Embolierisiko
- prothetischer Klappenendokarditis mit mechanischer Dysfunktion
Die Indikation ist häufig dringlich oder notfallmäßig. Wenn möglich, wird eine klappenerhaltende Rekonstruktion bevorzugt, da sie mit einer besseren Langzeitprognose und geringerer Reinfektionsrate assoziiert ist. Bei ausgedehnter Zerstörung oder Prothesenbeteiligung ist jedoch häufig ein vollständiger Ersatz notwendig.
Prophylaxe
Bei Patienten mit hohen Endokarditisrisiko kann die Indikation für eine Antibiotikaprophylaxe bestehen, die in diesem Zusammenhang als Endokarditisprophylaxe bezeichnet wird. Dies gilt besonders für Eingriffe, bei denen es zu einer Bakteriämie kommen kann. Eine Antibiotikaprophylaxe sollte z.B. bei zahnärztlichen Eingriffen am Parodont durchgeführt werden.
Literatur
- Laborlexikon.de; abgerufen am 21.02.2021
Quellen
- ↑ 1,0 1,1 DGK: ESC Pocket Guidelines Endokarditis, Version 2023, zuletzt abgerufen am 12.03.2026
- ↑ 2,0 2,1 Rieg et al.: Kontroversen und Herausforderungen im Management der infektiösen Endokarditis. Positionspapier der Deutschen Gesellschaft für Infektiologie. Dtsch Med Wochenschr, 2025