Aspergillose
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenDefinition
Die Aspergillose ist ein Überbegriff für alle Erkrankungen, die durch Schlauchpilze der Gattung Aspergillus verursacht werden. Haupterreger ist der aerobe Schimmelpilz Aspergillus fumigatus.
Einteilung
Man unterscheidet folgende Formen der Aspergillose, die wiederum verschiedene Organmanifestationen aufweisen können:
- invasive Aspergillose
- chronische Aspergillose
- saprophytische Aspergillose
- allergische Aspergillose
Erreger
Aspergillen sind unpigmentierte, septierte, verzweigt wachsende Schimmelpilze, die viele Sporen bilden können und ubiquitär vorkommen. Sie wachsen beispielsweise auf Heu, Baumwollstoffen, Brot, Früchten, Holz, Papier, Tapeten und Blumenerde in einem feuchten Milieu. Aspergillen bilden eine große Menge an Konidien (Sporen), die sich an Stielen auf dem Myzel befinden.
Von den über 350 bekannten Arten sind ca. 50 für den Menschen relevant, insbesondere:
- Aspergillus fumigatus: für die meisten Fälle invasiver, chronischer sowie allergischer Aspergillosen verantwortlich
- Aspergillus flavus: überwiegt in einigen Standorten. Verursacht häufiger Sinusitiden, Hautinfektionen und Keratitiden
- Aspergillus niger: kolonisiert häufig die oberen Atemwege und kann invasive Infektionen und eine Otitis media hervorrufen
- Aspergillus terreus: verursacht nur invasive Infektionen
- Aspergillus nidulans: ruft gelegentlich invasive Infektionen hervor, v.a. bei Patienten mit chronischer Granulomatose
Epidemiologie
Die Häufigkeit der verschiedenen Manifestationsformen variiert stark je nach geografischer Region. Beispielsweise kommt die chronische granulomatöse Sinusitis fast nur im Nahen Osten und Indien vor. Bei der chronischen Aspergillose wird die Inzidenz auf 10,4 und die Prävalenz auf 32,8 pro 100.000 Einwohner geschätzt. Weltweit sind etwa 3 Millionen Menschen erkrankt. Ohne Behandlung versterben ca. 50 %.
Bei der invasiven Aspergillose geht man von einer Inzidenz von 3,5/100.000 aus. Die weltweite Erkrankungszahl wird auf ca. 250.000 geschätzt. Der Verlauf ist ohne Behandlung fast immer letal.
Die allergischen Formen weisen eine geschätzte Prävalenz von 286/100.000 auf. Weltweit sind etwa 10 Millionen Menschen betroffen.
Ätiologie
Die Aspergillus-Sporen befinden sich ubiquitär in der Umgebungsluft. Das für eine Erkrankung notwendige Ausmaß der Exposition ist unbekannt. Eine regelmäßige vermehrte Exposition kann zu allergischen Aspergillosen führen, wobei eine kontinuierliche Allergenexposition über Kolonisation von Nasennebenhöhlen oder Atemwegen oder durch Nagelinfektionen hervorgerufen wird. Invasive Aspergillosen treten bei Immunsuppression auf, wobei nosokomiale Infektionen am häufigsten sind.
Manifestationen
| Form | Organ | Klinik |
|---|---|---|
| Invasiv | Lunge |
|
| Nasennebenhöhlen |
| |
| Gehirn | ||
| Haut |
| |
| Herz | ||
| Auge | ||
| Chronisch | Lunge |
|
| Nasennebenhöhlen |
| |
| Gehirn |
| |
| Haut | ||
| Saprophytisch | Lunge |
|
| Nasennebenhöhlen |
| |
| Allergisch | Lunge | |
| Nasennebenhöhlen |
|
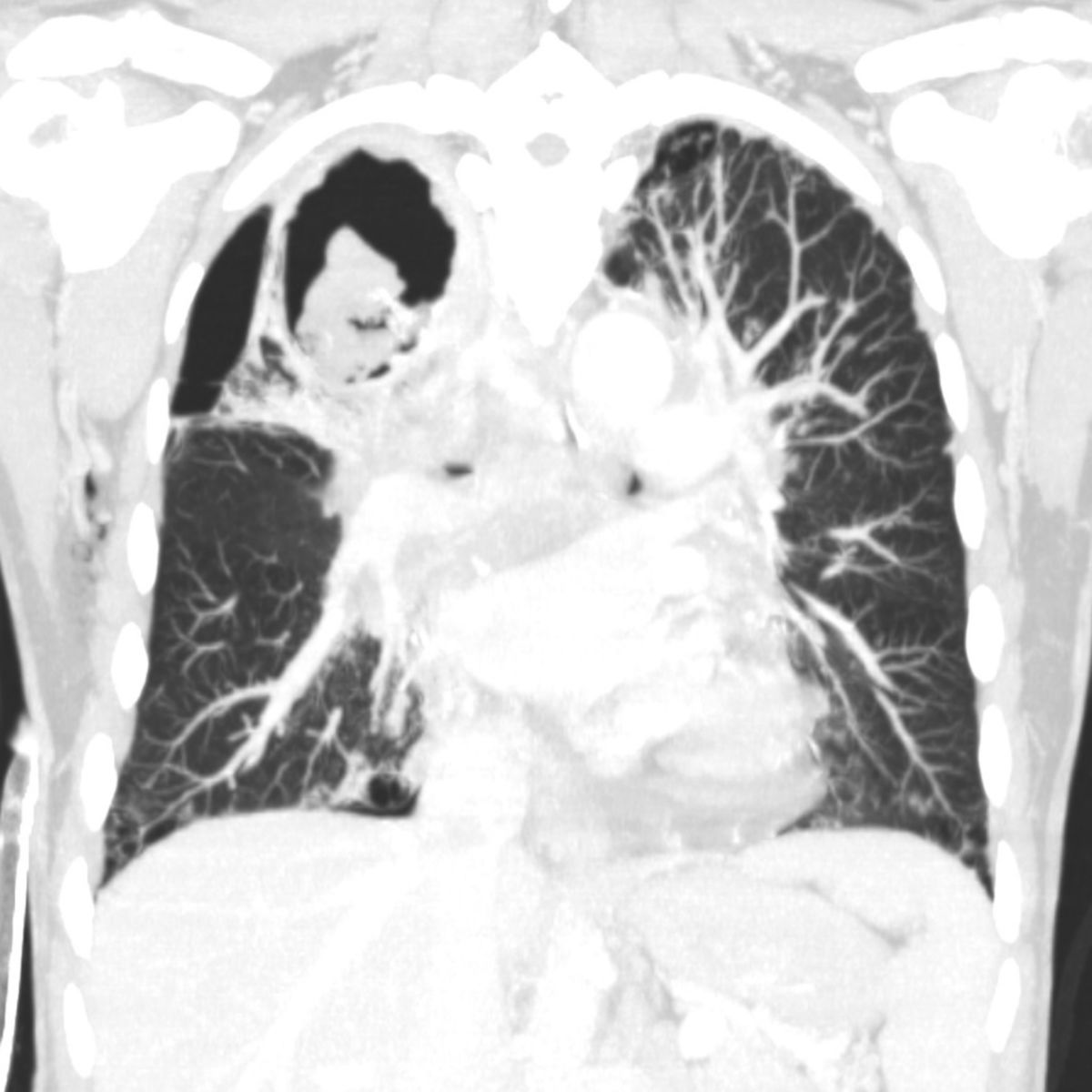
Invasive pulmonale Aspergillose
Bei der invasiven Aspergillose, die bei Immunschwäche auftritt (z.B. im Rahmen von AIDS, Alkoholismus, Diabetes mellitus, Glukokortikoidtherapie, Krebspatienten, Leukopenie), unterscheidet man zwischen einem akuten (< 1 Monat) und einem subakuten Verlauf (1-3 Monate). In über 80 % d.F. ist die Lunge betroffen, wobei es häufig zum Eindringen der Erreger in die Pulmonalarterien kommt. Als Komplikation kann ein hämorrhagischer Lungeninfarkt entstehen. Das klinische Bild der invasiven pulmonalen Aspergillose ist sehr variabel und reicht von Fieber, Husten, Thoraxschmerzen, Hämoptysen und Dyspnoe bis hin asymptomatischen Patienten. Sie zählt zu den am häufigsten übersehenen Todesursachen bei Intensivpatienten und wird oft erst bei Autopsien erkannt.
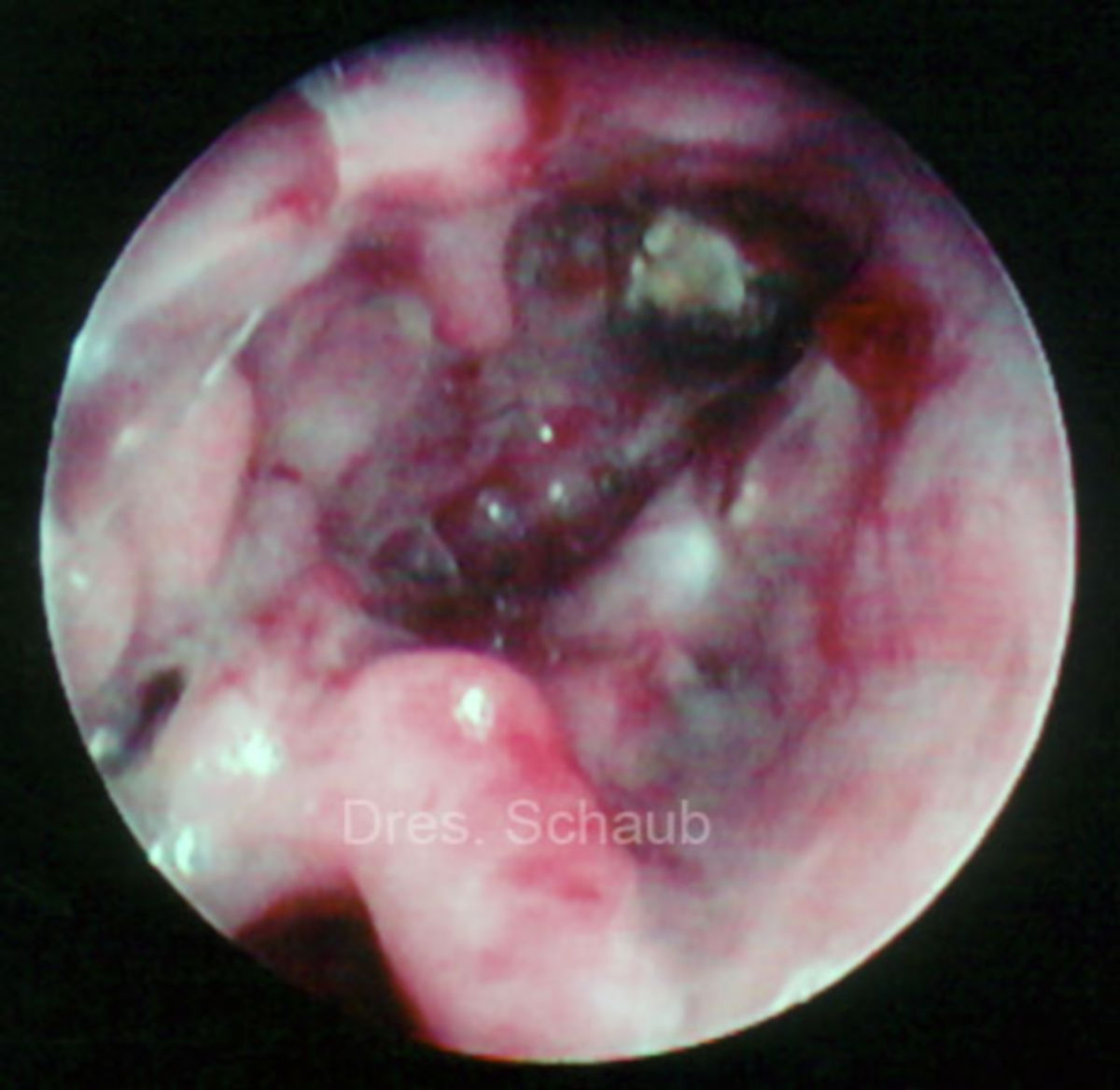
Invasive Sinusitis
Die Nasennebenhöhlen sind bei 5-10 % der Patienten mit invasiver Aspergillose betroffen, insbesondere bei Patienten mit Leukämie und hämatopoetischer Stammzelltransplantation. Symptome sind Fieber, behinderte Nasenatmung sowie eine vermehrte, z.T. blutige Nasensekretion.
Bronchitis
In seltenen Fällen sind lediglich die Atemwege im Sinne einer Tracheobronchitis betroffen, insbesondere bei Lungentransplantierten und bei maschinell beatmeten Patienten.
Rezidivierende thorakale Infektionen, die mit starker Dyspnoe, produktivem Husten mit zähem Auswurf einhergehen, sind typisch für eine Aspergillusbronchitis. Diese Patienten weisen häufig prädisponierende Lungenerkrankungen (Bronchiektasen, Mukoviszidose) auf. Eine gleichzeitige bakterielle Bronchitis ist häufig.
Disseminierte Aspergillose
Bei ausgeprägter Immunsuppression können sich die Aspergillen nach Einbruch ins Gefäßsystem in andere Organe ausbreiten. Am häufigsten betroffen sind das Gehirn, die Haut, die Schilddrüse, das Skelettsystem sowie Nieren, Leber, Darm, Auge und Herzklappen. Bei dieser disseminierten Aspergillose entwickelt sich schnell eine Sepsis. Die Blutkulturen sind meistens negativ.
Zerebrale Aspergillose
Bei der hämatogenen Disseminierung in das Gehirn im Rahmen einer invasiven Aspergillose entwickeln sich häufig ein hämorrhagischer Hirninfarkt sowie Abszesse. Eher seltenere Manifestationen sind Meningitis, ein mykotisches Aneurysma und Hirngranulome. Postoperative Infektionen kommen nur selten vor.
Typische Beschwerden sind akute und subakute Stimmungsveränderungen, fokal-neurologische Defizite, epileptische Anfälle und kognitive Störungen.
Aspergillus-Endokarditis
Endokarditiden durch Aspergillen betreffen meist künstliche Herzklappen, die während des operativen Eingriffs kontaminiert werden. Bei nativen Klappen muss an eine disseminierte Erkrankung und an ein intravenösen Drogenkonsum gedacht werden. Die Blutkulturen sind meist negativ.
Kutane Aspergillose
Bei hämatogener Disseminierung von Aspergillen können erythematöse oder violett indolente Hautläsionen vorkommen, die nekrotisieren und verschorfen. Nach Verbrennungen, bei Operationswunden sowie über Gefäßzugänge bei neutropenischen Patienten kann es auch zu einer direkten Erregerinvasion kommen. Haupterreger ist Aspergillus flavus.
Chronische pulmonale Aspergillose
Die chronische kavernöse pulmonale Aspergillose ist durch eine oder mehrere Lungenkavernen gekennzeichnet, die sich über Monate oder Jahre entwickeln. Die meisten Patienten weisen dabei pulmonale Vorerkrankungen wie Tuberkulose, atypische Mykobakteriosen, Sarkoidose oder Lungenemphysem auf. Die Kavernen können einen Flüssigkeitsspiegel oder einen Pilzball (Aspergillom) enthalten. Sie wird meist durch Aspergillus fumigatus, v.a. bei Diabetiker auch durch Aspergillus niger hervorgerufen. Typische Symptome sind Müdigkeit und Gewichtsverlust. Komplikationen sind lebensbedrohliche Hämoptysen. In 95 % finden sich IgG-Antikörper gegen Aspergillus. Unbehandelt schreitet die chronische kavernöse pulmonale Aspergillose in eine unilaterale oder apikale Fibrose fort (chronische fibrosierende pulmonale Aspergillose).
Eine weitere Form der chronischen pulmonalen Aspergillose sind Aspergillus-Knötchen. Sie ähneln einem Bronchialkarzinom im Frühstadium und können Kavernen bilden. Die Knötchen treten einzeln oder multipel auf und sind ca. 5-50 mm groß. IgG-Antikörper sind bei 65 % der Patienten nachweisbar.
Chronische Sinusitis
Man unterscheidet drei Formen der chronischen Sinusitis durch Aspergillen:
- Pilzball der Nasennebenhöhlen: betrifft fast immer den Sinus maxillaris, selten den Sinus sphenoidalis. Assoziiert mit vorangegangenen Wurzelbehandlungen am Oberkiefer und chronischen (bakteriellen) Sinusitiden. In der CT hyperdens, in der MRT hypointens in T2-Wichtung.
- chronische invasive Pilzsinusitis: langsam destruierender Prozess, der meist die Sinus ethmoidalis oder sphenoidalis betrifft. Meist bei immunsupprimierten Patienten. Typische Komplikationen sind das Orbitaspitzensyndrom und seltener Sinusvenenthrombosen oder eine Invasion in das Hirngewebe.
- chronische granulomatöse Sinusitis: meist im mittleren Osten und Indien vorkommend und v.a. durch Aspergillus flavus ausgelöst. Manifestiert sich erst spät durch Gesichtsschwellungen und einseitige Proptosis. Meist sind IgG-Antikörper gegen Aspergillus flavus nachweisbar.
Pilzasthma
Die allergische bronchopulmonale Aspergillose (ABPA) ist meist eine Hypersensitivitätsreaktion auf Aspergillus fumigatus und tritt v.a. bei Patienten mit Asthma bronchiale und Mukoviszidose auf. Typisch sind Episoden mit Dyspnoe und Aushusten von zähem, braunem Sputum. Diagnostisch wegweisend sind erhöhte IgE-Antikörper gegen Aspergillus (rASP f4 und f6) und ein erhöhtes Gesamt-IgE (meist > 1.000 IE/ml). In der Bildgebung fallen hyperdense Mukusimpaktionen und Bronchiektasen auf. Einige Patienten entwickeln eine chronisch kavernöse pulmonale Aspergillose.
Einige Patienten mit schwerem Asthma bronchiale erfüllen zwar nicht die Kriterien für eine ABPA, reagieren jedoch trotzdem allergisch auf Pilze. Man spricht in diesem Fall von schwerem Asthma mit Sensibilisierung auf Pilze (SAFS). Neben Aspergillus fumigatus sind aber auch z.B. Cladosporium und Alternaria spp. relevant.
Allergische Rhinosinusitis
Viele Patienten mit allergischer fungaler Rhinosinusitis leiden an einer Polyposis nasi und klagen über eine behinderte Nasenatmung sowie Verschleimungen der Nasennebenhöhlen. Histologisch fallen eine lokale Eosinophilie sowie Charcot-Leyden-Kristalle auf.
Diagnostik
Derzeit (2022) existiert kein Goldstandard für die Diagnose einer invasiven Aspergillose. Es kommen verschiedene Verfahren zum Einsatz, die in der Regel kombiniert werden.
Labordiagnostik
PCR
Der Nachweis von Aspergillus fumigatus kann auch durch eine Realtime-PCR erfolgen. Zielsequenz ist die mitochondriale DNA des Erregers. Das Untersuchungsmaterial richtet sich nach der Lokalisation der Infektion. In Frage kommen u.a. Punktate, Lavageflüssigkeit, Trachealsekret oder Biopsien. Daüber hinaus ist auch eine Bestimmung aus eingebettetem Gewebe möglich.
IgG-Aspergillus-Antikörper
Der Test auf Aspergillus-Antikörper vom Typ IgG ist die Methode der Wahl bei abgekapselten Mykosen an unzugänglichen Stellen (z.B. Lungenmyzetom) bzw. chronischen Aspergillosen. Insbesondere bei Mykosen an Körperoberflächen sind falsch negative Befunde möglich, weshalb in diesem Fall ein kultureller Nachweis indiziert ist.
Aspergillus-spezifische IgE-Antikörper
Bei ABPA und SAFS sind erhöhte Serumspiegel von Gesamt-IgE und Aspergillus-spezifischem IgE sowie ein Hautpricktest wegweisend. Die allergische Sinusitis wird meist mittels histologischer Untersuchung diagnostiziert, wobei der Nachweis von IgE-Antikörpern im Blut hilfreich ist.
Für den Nachweis des Aspergillus-Antikörper wird 1 ml Serum bzw. EDTA- oder Heparin-Plasma benötigt.
Galactomannan-Test
Der Galactomannan-Test ist ein immunologischer Labortest zum Nachweis von zirkulierendem Galactomannan. Galactomannan ist ein Polysaccharid, das ein Zellwandbestandteil der Gattung Aspergillus ist. Die zirkulierenden Antigene können bei einer invasiven Aspergillose etwa 5 bis 8 Tage vor dem Auftreten klinischer Symptome nachgewiesen werden.
1,3-β-D-Glucan-Test
Der 1,3-β-D-Glucan-Test basiert auf dem Nachweis des Zellwandbestandteils 1,3-β-D-Glucan im Serum. Ein positiver 1,3-β-D-Glucan-Test ist hinweisgebend auf eine Aspergillose, aber nicht spezifisch. Ein positives Testergebnis kann auch bei Pneumocystis- und Candida-Infektionen auftreten.
Mikrobiologie
Der Erregernachweis kann per Anzucht aus Blut, bronchoalveolärer Lavage (BAL), Abstrich, Punktat oder Sputum erfolgen. Die Anzüchtung dauert mindestens 10 Tage. Der Endbefund liegt nach etwa 3 Wochen vor. Der kulturelle Nachweis ist nur in 10-30 % der Fälle positiv. Bei chronischer Aspergillose sind die Kulturen selten positiv. Falsch positive Ergebnisse können bei Kontamination oder Kolonisierung der Luftwege mit Aspergillus entstehen.
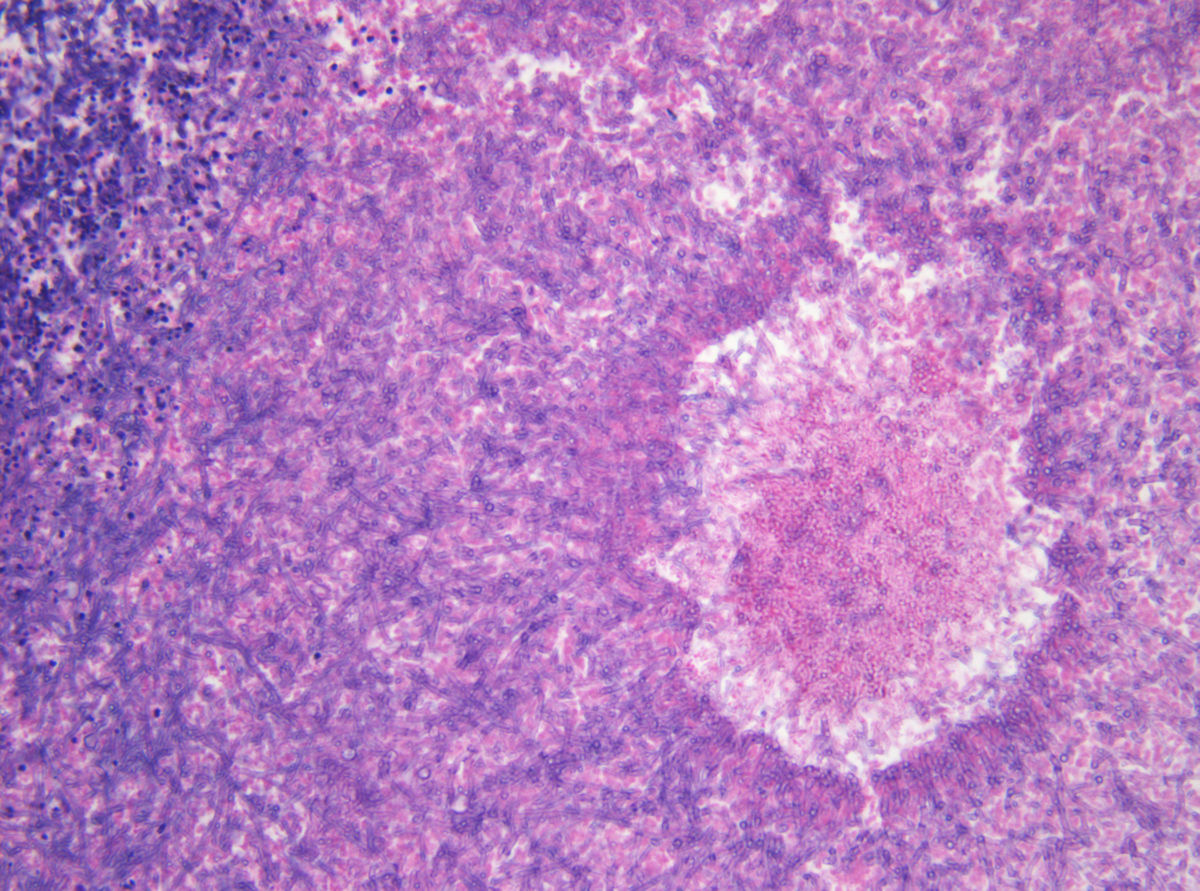
Histopathologie
Histopathologisch lassen sich Aspergillushyphen im nekrotischen Gewebe nachweisen. Die Darstellung gelingt zum Beispiel durch eine PAS- oder Grocott-Färbung.
Bildgebung
Im CT-Thorax finden sich z.B. folgende Befunde:
- Halo-Zeichen
- Konsolidierungen
- Kavernen
- Pleuraergüsse
Therapie
Medikamentöse Therapie
Gegen Aspergillus wirksame Medikamente sind:
- Triazol-Antimykotika: Voriconazol, Isavuconazol, Itraconazol, Posaconazol
- Echinocandine: Caspofungin, Micafungin
- Polyen-Antimykotikum: Amphotericin B
Entsprechend den Manifestationsarten gestaltet sich die Therapie unterschiedlich:
Invasive Aspergillose
Therapie der Wahl bei invasiver Aspergillose sind Voriconazol oder Isavuconazol. Alternativ kommen Amphotericin B, Caspofungin, Posaconazol oder Micafungin in Frage. Die Therapiedauer beträgt 6-12 Monate bis mehrere Jahre. Bei akuter invasiver Aspergillose wird initial eine parenterale Gabe empfohlen. Ein Therapiemonitoring ist mittels Titerbestimmung von Galactomannan möglich.
Amphotericin B ist gegen Aspergillus terreus und Aspergillus nidulans unwirksam. In < 5 % d.F. weist Aspergillus fumigatus eine Multiresistenz gegen Azol-Antimykotia auf. Weiterhin ist Aspergillus niger resistent gegen Itraconazol und Isavuconazol. Während der Erholungsphase kann es zu einem Immunrekonstitutionssyndrom kommen.
Chronische und allergische Aspergillosen
Itraconazol ist das Antimykotikum der Wahl bei chronischen und allergischen Formen. Alternativ kommen Voriconazol, Posaconazol sowie bei der chronischen Lungenaspergillose Amphotericin B in Frage. Bei akuten Exazerbationen der ABPA helfen Glukokortikoide. Bei chronischer nekrotisierender pulmonaler Aspergillose werden sie nur angewendet, wenn gleichzeitig eine adäquate Antimykotikatherapie erfolgt.
Bei der chronischen nekrotisierende Aspergillose ist eine Behandlung über 6 Monate notwendig. Die Therapiedauer bei anderen Formen der chronischen und allergischen Aspergillose wird individuell festgelegt.
Chirurgische Therapie
Eine chirurgische Behandlung kommt bei einigen Aspergilloseformen zur Anwendung, z.B. bei:
- Pilzball der Kieferhöhle
- singulärem Aspergillom der Lunge (bei mehreren Kavernen besser Itraconazol oder Voriconazol oder Instillation von Amphotericin B)
- invasiver Aspergillose der Knochen, der Herzklappen, der Nasennebenhöhlen, zentraler Lungenareale, bzw. Areale mit Kontakt zu großen Blutgefäßen
- Hirnabszesse
- Keratitiden, Endophthalmitiden
Bei der allergischen Pilzsinusitis kann die Entfernung von Mukus und Polypen sowie eine lokale oder systemische Gabe von Glukokortikoiden hilfreich sein. In einigen Fällen sind weitergehende chirurgische Maßnahmen (z.B. Ethmoidektomie) und die Gabe von Antimykotika notwendig.
Prophylaxe
Bei bestimmten Patienten mit mittlerem oder hohem Risiko für eine Pilzinfektion wird eine antimykotische Prophylaxe gegen invasive Aspergillosen (und Candidainfektionen) durchgeführt:[1][2]
- Neutropenie durch Induktionschemotherapie (z.B. bei AML):
- Posaconazol
- oder liposomales Amphotericin B per inhalationem
- und Fluconazol
- Neutropenie bei allogener Stammzelltransplantation:
- Voriconazol
- oder Itraconazol
- GvHD:
- Posaconazol
- Itraconazol
Prognose
Die invasive Aspergillose ist grundsätzlich heilbar, trotzdem beträgt die Mortalität 30-70 % bei adäquater Therapie und 100 % ohne Behandlung. Eine besonders schlechte Prognose weisen Patienten mit zerebraler Aspergillose, Aspergillus-Endokarditis und bilateraler invasiver Lungenaspergillose auf.
Die allergischen und chronischen Formen sind nicht heilbar. Die 5-Jahres-Letalität der chronischen kavitären pulmonalen Aspergillose beträgt bei antimykotischer Therapie etwa 40 %. Ein Therapieversagen der antimykotischen Behandlung findet sich bei etwa 30 % der Patienten.
60-80 % Patienten mit ABPA und SAFS sprechen auf eine antimykotische Therapie an. Rezidive nach Beendigung der Therapie sind häufig.
Literatur
- Laborlexikon.de; abgerufen am 04.02.2021
- Jacobi T, Suttorp N. 212 Aspergillose. In: Suttorp N, Möckel M, Siegmund B et al., Hrsg. Harrisons Innere Medizin. 20. Auflage. Berlin: ABW Wissenschaftsverlag; 2020.