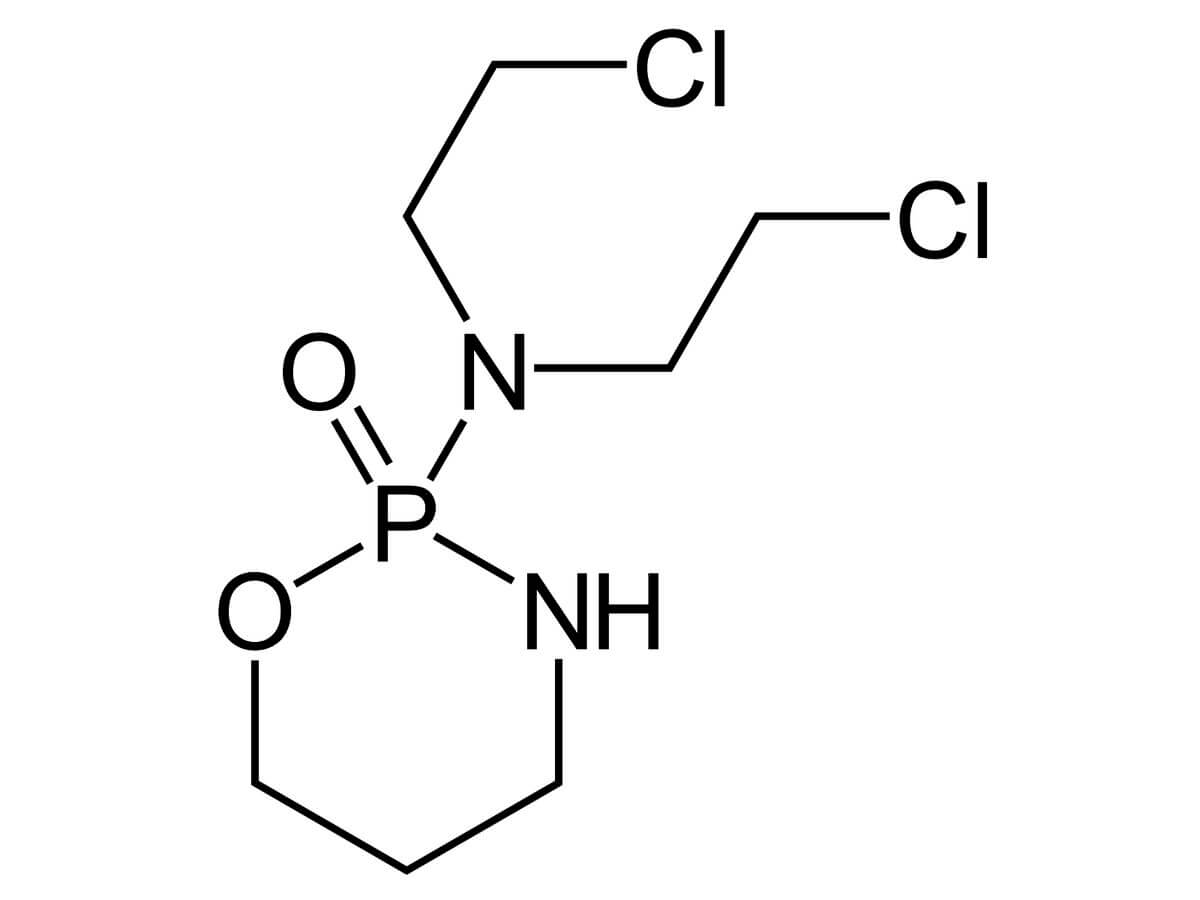
Cyclophosphamid
Handelsname: Endoxan®
Englisch: cyclophosphamide, cytophosphane
Definition
Cyclophosphamid ist ein alkylierender Arzneistoff aus der Gruppe der Oxazophosphorine bzw. der Stickstofflost-Verbindungen. Es wird als Zytostatikum zur Behandlung von Tumorerkrankungen sowie zur Immunsuppression eingesetzt.
Geschichte
Cyclophosphamid wurde in den 1950er-Jahren als besser handhabbares Derivat der Stickstofflost-Verbindungen entwickelt.
Klinisch wurde der Wirkstoff zunächst vor allem in der Onkologie eingesetzt und später auch bei schweren Autoimmunerkrankungen etabliert. Trotz neuerer Therapieoptionen besitzt Cyclophosphamid weiterhin einen festen Stellenwert, insbesondere in der Hämatoonkologie, in Konditionierungsregimen vor Stammzelltransplantationen und bei ausgewählten schweren entzündlich-rheumatologischen Erkrankungen.
Chemie
Cyclophosphamid ist chemisch ein bifunktionelles Oxazaphosphorin mit der Summenformel C7H15Cl2N2O2P und einer molaren Masse von 261,1 g/mol.
Es handelt sich um ein zyklisches Phosphorsäureamid mit zwei 2-Chlorethyl-Seitenketten. Die alkylierende Wirkung beruht nicht auf der Muttersubstanz selbst, sondern auf reaktiven Metaboliten, die nach enzymatischer Aktivierung entstehen.
Wirkmechanismus
Cyclophosphamid ist ein Prodrug, das erst nach Aktivierung in der Leber seine zytotoxischen und immunsuppressiven Eigenschaften entfaltet. In der Leber wird es durch Cytochrom P450-Enzyme, insbesondere CYP2B6 sowie weitere Isoenzyme (u.a. CYP2A6, CYP2C9, CYP2C19 und CYP3A4), zu 4-Hydroxycyclophosphamid hydroxyliert. Dieses steht im Gleichgewicht mit seinem Tautomer Aldophosphamid.
Aldophosphamid wird entweder durch das Enzym Aldehyddehydrogenase (ALDH) zu inaktiven Metaboliten (z.B. Carboxycyclophosphamid) oxidiert oder zerfällt zu Acrolein und Phosphoramidmustard. Acrolein ist wesentlich für die urotoxischen Nebenwirkungen verantwortlich.
Phosphoramidmustard bildet reaktive Zwischenprodukte, die kovalent an nukleophile Gruppen von Nukleinsäuren und Proteinen binden. Besonders betroffen ist das N7-Atom des Guanins. Dies führt zu intra- und interstrangulären DNA-Quervernetzungen sowie DNA-Protein-Crosslinks, wodurch DNA-Replikation, Transkription und Zellteilung gehemmt werden und letztlich eine Apoptose der Tumorzellen ausgelöst wird.
Die immunsuppressive Wirkung beruht vor allem auf der Schädigung proliferierender T-Zellen und B-Zellen sowie auf Veränderungen immunologischer Signalwege.
Pharmakokinetik
Cyclophosphamid kann oral oder intravenös appliziert werden. Nach oraler Gabe ist die Resorption in der Regel gut.
Die Elimination erfolgt über hepatische und renale Wege, überwiegend in Form von Metaboliten, zu einem geringeren Anteil auch unverändert im Urin. Die Plasmahalbwertszeit liegt typischerweise im Bereich von etwa 3 bis 12 Stunden und ist dosis-, alters- und patientenabhängig.
Pharmakogenetische Unterschiede, insbesondere in CYP-vermittelten Stoffwechselwegen, können die Exposition gegenüber aktiven Metaboliten und damit Wirksamkeit und Toxizität beeinflussen.
Indikation
Cyclophosphamid wird bei malignen und nicht malignen Erkrankungen eingesetzt.
Onkologische Indikationen
- Malignes Lymphom
- Morbus Hodgkin
- Non-Hodgkin-Lymphom
- Chronische lymphatische Leukämie
- Akute lymphatische Leukämie
- Akute myeloische Leukämie
- Multiples Myelom
- Mammakarzinom
- Ovarialkarzinom
- Neuroblastom
- Retinoblastom
- Mycosis fungoides
- Ewing-Sarkom
- Rhabdomyosarkom
Nicht onkologische Indikationen
- schwere ANCA-assoziierte Vaskulitis
- Granulomatose mit Polyangiitis
- Mikroskopische Polyangiitis
- Systemischer Lupus erythematodes (v.a. bei Lupusnephritis)
- Systemische Sklerose mit interstitieller Lungenerkrankung
- Goodpasture-Syndrom
- Minimal-Change-Glomerulonephritis
- ausgewählte schwere Glomerulonephritiden
Der Einsatz bei Autoimmunerkrankungen erfolgt heute in der Regel bei schweren, organ- oder lebensbedrohlichen Verläufen und meist als Induktionstherapie.
Darreichungsformen
Verfügbar sind insbesondere:
- überzogene Tabletten bzw. Kapseln zur oralen Anwendung
- Pulver zur Herstellung einer Injektionslösung bzw. Infusionslösung zur intravenösen Anwendung.
Dosierung
Die Dosierung ist streng indikationsabhängig und richtet sich unter anderem nach Erkrankung, Therapieschema, Körpergewicht, Körperoberfläche, Organfunktion und Begleittherapie.
In der Onkologie wird Cyclophosphamid häufig als Bestandteil von Kombinationsschemata angewendet.
Dosisanpassungen können bei Knochenmarksuppression, eingeschränkter Nierenfunktion, eingeschränkter Leberfunktion und im Rahmen myelotoxischer Kombinationstherapien erforderlich sein.
Nebenwirkungen
Zu den wichtigsten Nebenwirkungen zählen:
- Leukopenie
- Neutropenie
- Thrombozytopenie
- Übelkeit bzw. Zytostatika-induziertes Erbrechen.
- Erbrechen
- Alopezie
Spezifisch ist die hämorrhagische Zystitis, die vor allem durch den Metaboliten Acrolein verursacht wird und durch die parallele Gabe von MESNA (Mercapto-ethansulfonat-Natrium) verhindert werden soll.
Weitere relevante Nebenwirkungen sind:
- Infektionen bis hin zu schweren opportunistischen Infektionen
- Myelosuppression mit Anämie, febriler Neutropenie und Sepsis
- Syndrom der inadäquaten ADH-Sekretion (SIADH)
- Kardiotoxizität, insbesondere bei hohen kumulativen Dosen
- Pneumonitis und Lungenfibrose
- Hepatotoxizität
- Amenorrhö, Ovarialinsuffizienz, Oligospermie und Azoospermie
- Infertilität
- Teratogenität und embryofetale Toxizität
- sekundäre Malignome, insbesondere Leukämien und Urothelkarzinome
Selten kommt es aufgrund der Bildung von Chloracetaldehyd zu neurotoxischen Nebenwirkungen (Psychosen, Ataxie, Krampfanfälle, Koma).
Aufgrund der karzinogenen Wirkung von Cyclophosphamid ist das Risiko z.B. für sekundäre Lymphome, Leukämien, kutane Malignome und Urothelkarzinome deutlich erhöht.
Wechselwirkungen
Cyclophosphamid weist klinisch relevante Wechselwirkungen mit Arzneistoffen auf, welche die hepatische Biotransformation beeinflussen.
Mögliche Interaktionspartner sind insbesondere:
- CYP-Induktoren, die die Metabolisierung verändern können
- CYP-Inhibitoren, die die Aktivierung bzw. Elimination beeinflussen können
- andere myelotoxische oder immunsuppressive Arzneimittel mit Verstärkung der Knochenmarksuppression und des Infektionsrisikos
- Anthrazykline oder Trastuzumab mit potenzieller Zunahme kardiotoxischer Effekte
- Succinylcholin, dessen Wirkung durch Verminderung der Pseudocholinesterase-Aktivität verlängert werden kann.
Kontraindikationen
Zu den Kontraindikationen bzw. wesentlichen Gegenanzeigen zählen insbesondere:
- Überempfindlichkeit gegen Cyclophosphamid
- Harnabflussstörung
- schwere, nicht kontrollierte Infektionen
- ausgeprägte Knochenmarkdepression
- Schwangerschaft, sofern keine zwingende vital bedingte Indikation besteht.
Relative Kontraindikationen bzw. besondere Vorsicht bestehen bei vorausgegangener starker Myelosuppression, eingeschränkter Leber- oder Nierenfunktion sowie bestehender Urotoxizität.
Verordnungshinweis
Vor und während der Therapie sind regelmäßige Kontrollen erforderlich, insbesondere von:
Zur Reduktion der Urotoxizität sind ausreichende Hydratation und forcierte Diurese wichtig. Bei höher dosierter intravenöser Therapie wird häufig zusätzlich Mesna eingesetzt.
Patientinnen und Patienten sind über Fertilitätsrisiken, Kontrazeption und die potenzielle Langzeittoxizität aufzuklären.
Zulassung
Die erste Zulassung von Cyclophosphamid in den USA erfolgte im Jahr 1959.
In der EU besteht für Cyclophosphamid keine einheitliche zentrale Zulassung über die EMA. Die Zulassung erfolgte bzw. erfolgt in den einzelnen EU- und EWR-Staaten über nationale Verfahren oder im Rahmen wechselseitiger Anerkennung.
In Deutschland ist Cyclophosphamid weiterhin national zugelassen und im Handel. Für das Präparat Endoxan liegen aktuelle deutsche Fachinformationen vor.
ATC-Code
- L01AA01 – Cyclophosphamid
Quellen
- Fachinformation – Endoxan, abgerufen am 08.04.2026
- Rote Liste – Endoxan, abgerufen am 08.04.2026
- BFArM – Zulassungsantrag, abgerufen am 08.04.2026
- Prescription Information – Cyclophosphamide, abgerufen am 08.04.2026
- EMA – Cyclophosphamide, abgerufen am 08.04.2026
- NIPH – ATC/DDD Index, abgerufen am 08.04.2026