Ebolafieber
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
Loslegennach dem Ebola-Fluss (Demokratische Republik Kongo) benannt
Synonyme: Ebola, Ebola-Krankheit, Maridi-Fieber
Englisch: Ebola virus disease (EVD), Ebola hemorrhagic fever (EHF)
Definition
Das Ebolafieber ist eine häufig tödlich verlaufende Infektionskrankheit, die mit hämorrhagischem Fieber einhergehen kann und durch das Ebolavirus aus der Familie der Filoviridae ausgelöst wird. Das Fieber gehört zu den Zoonosen.
- ICD10-Code: A98.4 Ebola-Viruskrankheit
Erreger
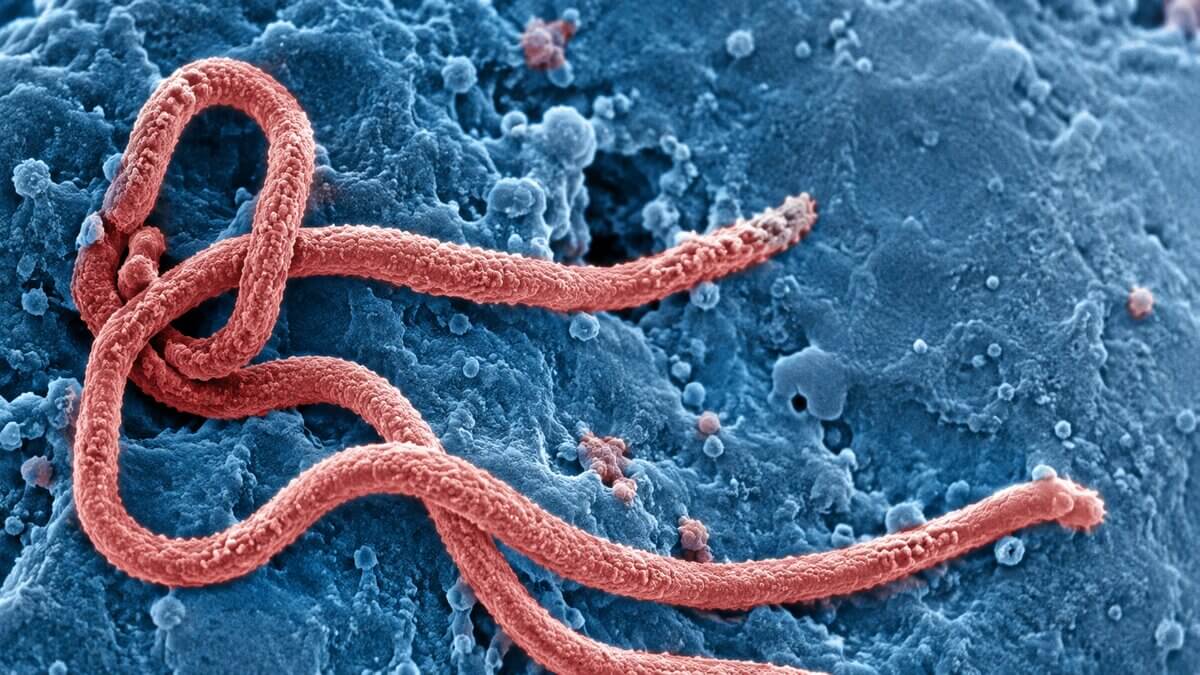
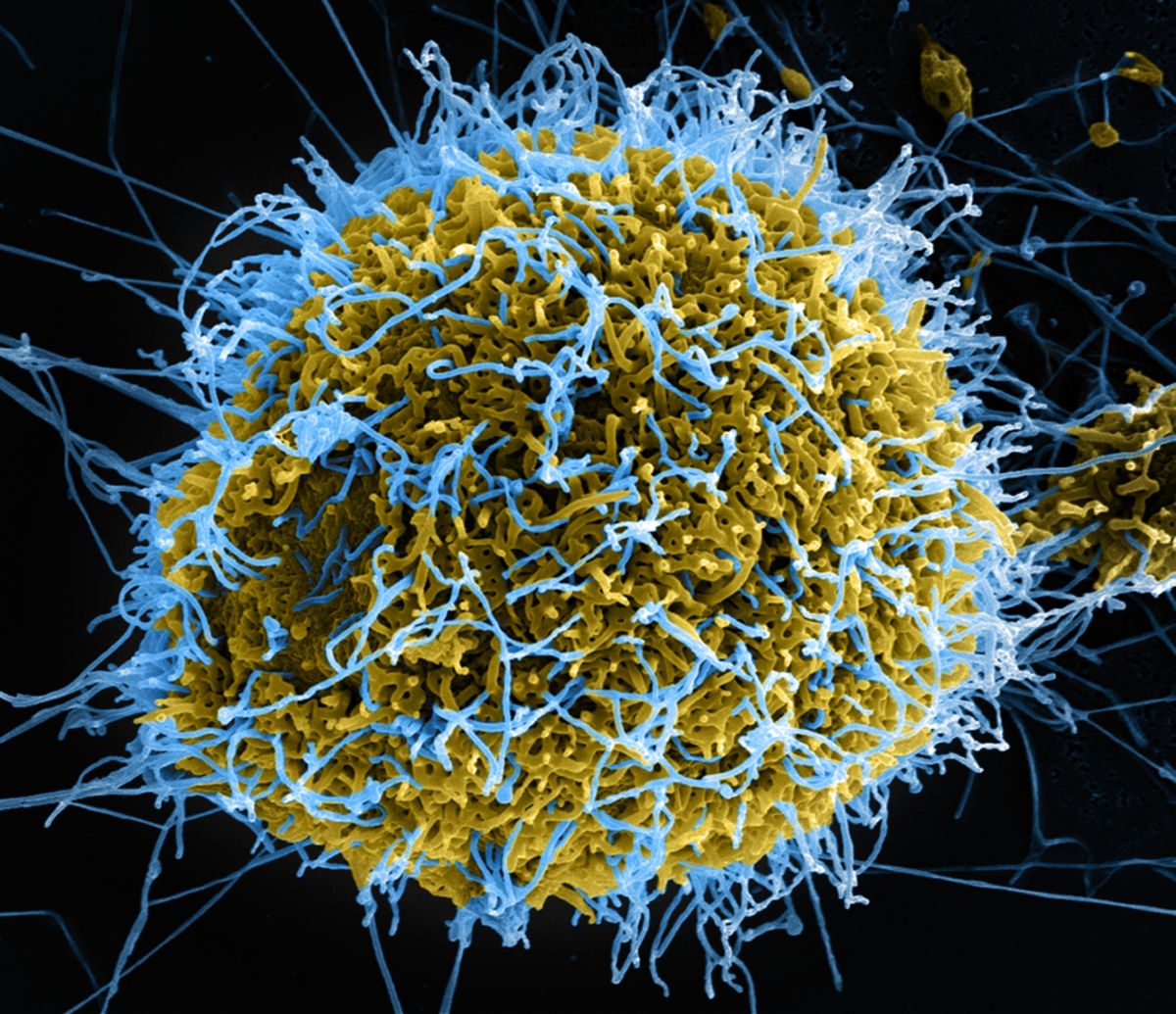
Ebolaviren sind große RNA-Viren von lang gestreckter, fadenförmiger Gestalt. Sie können gelegentlich auch U-förmig gebogen sein. Die Länge kann bis zu 14.000 nm betragen, der Durchmesser liegt bei 80 nm. Ebolaviren sind vielseitig und können sich in fast allen Zellen des infizierten Wirts vermehren. Aufgrund der schnellen Virensynthese bildet sich ein Viruskristall (Crystalloid), der vom Zellkern nach außen dringt und nach der Lyse der Zelle einzelne Viren frei lässt.
Das Ebolafieber kann durch 5 verschiedene Arten der Gattung Orthoebolavirus (früher Ebolavirus) ausgelöst werden, wobei nicht alle Spezies einen gleich schweren Krankheitsverlauf zeigen. Dazu zählen:
- Zaire-Ebolavirus (EBOV)
- Sudan-Ebolavirus (SUDV)
- Reston-Ebolavirus (RESTV)
- Taï-Forest-Ebolavirus (TAFV)
- Bundibugyo-Ebolavirus (BDBV)
Das britische Advisory Committee on Dangerous Pathogens (ACDP) stuft das Virus aufgrund der hohen Infektionsgefahr in die Klasse 4 der Krankheitserreger ein. Die hohe Letalität der Infektion zeigt, dass das Ebolavirus nicht an den Menschen als Wirt angepasst ist. Für den langfristigen Erhalt einer Viruspopulation ist es unvorteilhaft, den Endwirt zu töten, da das Virus seinen eigenen Lebensraum und die Möglichkeit der Vermehrung zerstört.
Um in die Zelle einzudringen und sich zu replizieren, benötigen Ebolaviren das Cholesterin-Transportprotein NPC1. Zellen von Patienten, die eine Mutation von NPC1 aufweisen (Morbus Niemann-Pick Typ C) sind immun gegen das Virus.[1]
Epidemiologie
In der Vergangenheit kam es – vor allem in Zentralafrika (z.B. Zaire, Gabun) – mehrfach zu lokalen Ausbrüchen von Ebolafieber. Eine größere Anzahl von Erkrankungsfällen wurde u.a. 1976 in Yambuku, 1995 in Kikwit (beide Zaire), 2001 in Uganda und 2007 in der Demokratischen Republik Kongo registriert.
2014–2016 bestand die bislang größte Ebola-Epidemie in Westafrika, deren Auslöser das Zaire-Ebolavirus war. Insgesamt wurden mehr als 28.000 Infizierte und mehr als 11.000 Todesfälle dokumentiert.[2] Die tatsächlichen Zahlen dürften nach Einschätzung der WHO deutlich höher liegen, da nicht alle Fälle gemeldet werden. Betroffen waren Guinea, Sierra Leone, Liberia sowie einzelne Fälle in Nigeria, Mali und im Senegal. Am 8. August 2014 erklärte die WHO die Epidemie zum Internationalen Gesundheitsnotfall (PHEIC). Im März 2016 wurde die Westafrika-Epidemie durch die WHO als beendet erklärt.[3]
Ende August 2014 wurden weitere Ebolafälle im Kongo gemeldet, die jedoch wahrscheinlich auf einen anderen Virusstamm zurückzuführen sind. Anfang Oktober 2014 traten die ersten Erkrankungs- und Verdachtsfälle in den USA und in Spanien auf. Darüber hinaus wurden in mehreren europäischen Ländern aus dem Endemiegebiet ausgeflogene Ebola-Infizierte behandelt. Nigeria gilt seit Mitte Oktober 2014 wieder als ebolafrei, Mali seit Mitte Januar 2015.
2018–2020 kam es in den Provinzen Nord-Kivu und Ituri der Demokratischen Republik Kongo zum bisher (Mai 2026) zweitgrößten Ebola-Ausbruch der Geschichte (ebenfalls Zaire-Ebolavirus) mit über 2.200 Todesfällen.[4]
Im Mai 2026 rief die WHO erneut den Internationalen Gesundheitsnotfall aus: Der aktuell (Mai 2026) laufende Ausbruch in der Provinz Ituri (Demokratische Republik Kongo) wird durch das Bundibugyo-Ebolavirus (BDBV) verursacht.[5]
Die folgende Tabelle zeigt historische Ebola-Fälle in Afrika von 1976 bis 2026:
| Land | Stadt | Infektionen | Todesfälle | Stamm | Jahr |
|---|---|---|---|---|---|
| Dem. Rep. Kongo | Yambuku | 318 | 280 | Zaïre-Ebola | 1976 |
| Südsudan | Nzara | 284 | 151 | Sudan-Ebola | 1976 |
| Dem. Rep. Kongo | Tandala | 1 | 1 | Zaïre-Ebola | 1977 |
| Südsudan | Nzara | 34 | 22 | Sudan-Ebola | 1979 |
| Gabun | Mekouka | 52 | 31 | Zaïre-Ebola | 1994 |
| Elfenbeinküste | Taï Forest | 1 | 0 | Taï Forest-Ebola | 1994 |
| Dem. Rep. Kongo | Kikwit | 315 | 250 | Zaïre-Ebola | 1995 |
| Gabun | Mayibout | 37 | 21 | Zaïre-Ebola | 1996 |
| Gabun | Booue | 60 | 45 | Zaïre-Ebola | 1996 |
| Südafrika | Johannesburg | 2 | 1 | Zaïre-Ebola | 1996 |
| Uganda | Gulu | 425 | 224 | Sudan-Ebola | 2000 |
| Gabun | Libreville | 65 | 53 | Zaïre-Ebola | 2001 |
| Republik Kongo | – | 57 | 43 | Zaïre-Ebola | 2001 |
| Republik Kongo | Mbomo | 143 | 128 | Zaïre-Ebola | 2002 |
| Republik Kongo | Mbomo | 35 | 29 | Zaïre-Ebola | 2003 |
| Südsudan | Yambio | 17 | 7 | Sudan-Ebola | 2004 |
| Dem. Rep. Kongo | Luebo | 264 | 187 | Zaïre-Ebola | 2007 |
| Uganda | Bundibugyo | 149 | 37 | Bundibugyo-Ebola | 2007 |
| Dem. Rep. Kongo | Luebo | 32 | 15 | Zaïre-Ebola | 2008 |
| Uganda | Luwero-Distrikt | 1 | 1 | Sudan-Ebola | 2011 |
| Uganda | Distrikt Kibaale | 11 | 4 | Sudan-Ebola | 2012 |
| Dem. Rep. Kongo | Isiro | 36 | 13 | Bundibugyo-Ebola | 2012 |
| Uganda | Luwero-Distrikt | 6 | 3 | Sudan-Ebola | 2012 |
| Westafrika | diverse | 28.652 | 11.325 | Zaïre-Ebola | 2014–2016 |
| Dem. Rep. Kongo | diverse | 66 | 49 | Zaïre-Ebola | 2014 |
| Dem. Rep. Kongo | Likati | 8 | 4 | Zaïre-Ebola | 2017 |
| Dem. Rep. Kongo & Uganda | diverse | 3.463 | 2.280 | Zaïre-Ebola | 2018–2020 |
| Uganda | diverse | 14 | 4 | Sudan-Ebola | 2025 |
| Dem. Rep. Kongo & Uganda | Ituri/Kampala | > 254 Verdachtsfälle, 8 bestätigt (Stand 18.05.2026)[5] | > 80 Verdachtstodesfälle (Stand 18.05.2026)[5] | Bundibugyo-Ebola | 2026 |
Übertragung
Die Infektionswege sind nicht vollständig geklärt. Als natürliches Erregerreservoir der Ebolaviren dienen wahrscheinlich Flughunde. Auf welchem Weg sich der Wirtswechsel vollzieht ist noch unklar. Diskutiert wird die Verunreinigung von Früchten oder Blättern durch Flughundspeichel oder -kot und die anschließende Aufnahme durch andere Tierarten. Wahrscheinlich ist eine Übertragung durch direkten Kontakt mit infizierten kranken oder toten Tieren.
Das Virus ist hoch kontagiös. Die Übertragung zwischen Menschen erfolgt primär durch direkte Kontakt- bzw. Schmierinfektion und Körperflüssigkeiten (u.a. Blut, Speichel, Stuhl, Erbrochenes). Ebolaviren ließen sich auch im Schweiß, in der Tränenflüssigkeit, in der Muttermilch und im Sperma nachweisen.[6] Der Erreger wird meist peroral inkorporiert. Darüber hinaus sind die Konjunktiven ein möglicher Infektionsweg. Die aerogene Übertragung in Aerosolen per Tröpfcheninfektion soll dagegen – nach allgemeiner Lehrbuchmeinung – nur eine untergeordnete Rolle spielen. Das gilt jedoch nicht, wenn zum Beispiel durch Niesen oder Husten in unmittelbarer Nähe eine größere Menge kontaminierter Speichel oder Nasensekret auf die Haut gelangen. In Tierversuchen gab es ebenfalls Hinweise darauf, dass eine Übertragung von Ebolaviren über die Luft möglich ist.[7]
Ebola-Epidemien treten bevorzugt in Gebieten mit eingeschränkter Gesundheitsversorgung auf und werden vor allem durch unzureichende Krankenhaushygiene begünstigt, z.B. durch Mangel an sterilem Einmalmaterial sowie adäquater Schutzkleidung. Der laufende Ausbruch 2026 in der Provinz Ituri illustriert dies erneut: Mindestens vier Todesfälle unter Gesundheitsfachpersonal mit klinischem Bild eines hämorrhagischen Fiebers wurden gemeldet.[5]
Für Reisende besteht ein Risiko, wenn sie sich während eines Ausbruchs im Endemiegebiet oder – bei diffuser geografischer Ausbreitung – in Nachbarregionen aufhalten.
Klinik
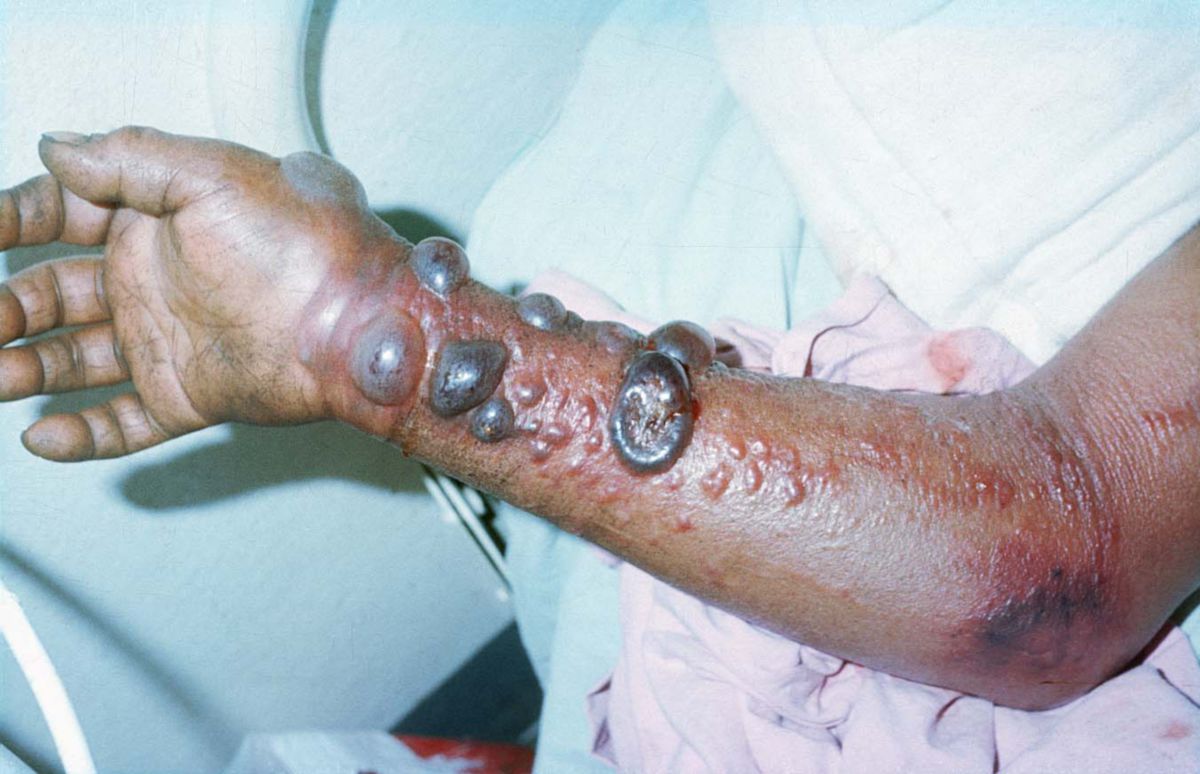
Symptome einer Ebola-Infektion treten in der Regel 6 bis 12 Tage nach Infektion auf, wobei auch kürzere und längere Inkubationszeiten beschrieben sind.[8] Die Erkrankung beginnt unspezifisch mit einem grippeähnlichen Krankheitsbild mit starkem Krankheitsgefühl. Je nach betroffenem Organsystem können folgende Symptome auftreten:
Das Auftreten hämorrhagischer Symptome (z.B. Hämatemesis, Hämoptyse, Meläna) weist auf einen schweren und prognostisch ungünstigen Krankheitsverlauf hin. Im Endstadium kommt es zum Multiorganversagen durch Störungen der Flüssigkeitsverteilung, Hypotension, disseminierte intravasale Koagulation und Gewebsnekrosen. Die Letalität liegt je nach Viren-Stamm zwischen 25 und 90 %. Jüngere Patienten haben eine bessere Überlebenschance als Patienten > 45 Jahre. In einigen Fällen kann die Infektion auch asymptomatisch verlaufen.
Verdachtsdiagnose
Die Verdachtsdiagnose stützt sich auf drei Punkte:
- Fieber > 38,5 °C
- Reiseanamnese: Aufenthalt in einem Endemiegebiet bzw. in Gebieten, in denen in den letzten zwei Monaten Ebolafieber auftrat < 3 Wochen vor Krankheitsbeginn
- Verdacht auf Kontakt mit an Ebolafieber erkrankten bzw. verstorbenen Personen oder Tieren
Diagnostik
Labordiagnostisch kann das Ebolafieber durch den Nachweis von Ebolavirus-Antigenen oder Ebolavirus-RNA mittels RT-PCR in Kombination mit ELISA im Blut bzw. Blutserum des Patienten oder anderen Körperflüssigkeiten (Urin, Speichel, Sperma) nachgewiesen werden. Die Labordiagnostik muss in einem Speziallabor der Schutzstufe 4 erfolgen.
Für den Virusnachweis des Zaire-Ebolavirus wird u.a. der EZ1 rRT-PCR-Assay (TaqMan®) verwendet, der Trizol-inaktivierte Blut- oder Plasmaproben bereits bei geringen klinischen Anzeichen und Expositionsrisiko identifiziert. Dieser sowie mehrere weitere RT-PCR-Tests (u.a. CDC Ebola Virus NP/VP40 Real-time RT-PCR Assay, RealStar® Ebolavirus RT-PCR Kit 1.0 von altona Diagnostics) werden in den USA unter einer Emergency Use Authorization (EUA) der FDA eingesetzt, die seit 2014 besteht. Lediglich der OraQuick Ebola Rapid Antigen Test erhielt zwischenzeitlich eine reguläre De-Novo-Zulassung der FDA.[9] Der Virusnachweis besitzt eine hohe Spezifität und Sensitivität, in frühen Infektionsstadien sind jedoch falsch-negative Testergebnisse möglich.
Alternativ kann das Virus durch Anzucht in geeigneten Zellkulturen (z.B. Vero E6-Nierenepithelzellen der Meerkatze) isoliert und anschließend aufgrund seines charakteristischen fadenförmigen Aussehens elektronenmikroskopisch identifiziert werden. Diese Methode kann jedoch nicht zwischen den verschiedenen Filoviren differenzieren. Die mikrobiologische Diagnostik von Filoviren wird in Deutschland von der Philipps-Universität Marburg und dem Bernhard-Nocht-Institut in Hamburg durchgeführt.
Differentialdiagnose
Andere hoch fieberhafte Infektionskrankheiten bzw. Tropenkrankheiten durch:
- Parasiten (Malaria)
- Viren (Gelbfieber, Dengue-Fieber, Lassa-Fieber, Krim-Kongo-Fieber oder Marburgfieber)
- Bakterien (z.B. Typhus, Rückfallfieber, Rickettsiose)
Therapie
Supportive Therapie
Die Behandlung des Ebolafiebers umfasst primär eine intensive symptomatische und supportive Therapie mit Aufrechterhaltung des Wasser- und Elektrolythaushalts, adäquater Analgesie sowie dem Ausgleich von Gerinnungsstörungen. Gegebenenfalls sind Thrombozytenkonzentrate, Frischplasma und Erythrozytenkonzentrate indiziert. Antibiotika und Antimykotika dienen der Kontrolle von Sekundärinfektionen.
Zugelassene Therapeutika (Zaire-Ebolavirus)
Für die Behandlung der durch das Zaire-Ebolavirus (EBOV) verursachten Erkrankung stehen seit 2020 zwei von der FDA zugelassene monoklonale Antikörpertherapien zur Verfügung:
- Inmazeb (Atoltivimab/Maftivimab/Odesivimab): Kombination aus drei humanen monoklonalen Antikörpern, die an nicht-überlappende Epitope des EBOV-Glykoproteins binden. Die FDA-Zulassung erfolgte im Oktober 2020 für Erwachsene und Kinder einschließlich Neugeborener. Grundlage war die randomisierte PALM-Studie.[10]
- Ebanga (Ansuvimab-zyk): Einzelner humaner monoklonaler Antikörper, der an das EBOV-Glykoprotein bindet und den Zelleintritt blockiert. FDA-Zulassung im Dezember 2020, ebenfalls für Erwachsene und Kinder einschließlich Neugeborener.[11]
Cave: Beide Therapeutika sind ausschließlich gegen das Zaire-Ebolavirus wirksam. Für den Bundibugyo-Ebolavirus, der den aktuellen Ausbruch 2026 verursacht, gibt es derzeit (Mai 2026) keine zugelassenen Therapeutika oder Impfstoffe.[5]
Experimentelle Therapieansätze
ZMapp
ZMapp besteht aus drei chimären monoklonalen Antikörpern (c13C6, c2G4, c4G4), die gegen das Glykoprotein des Zaire-Ebolavirus gerichtet sind. 2014 wurde ZMapp unter Compassionate Use an mehrere infizierte US-amerikanische Gesundheitsfachkräfte verabreicht. Die anschließende randomisiert-kontrollierte PREVAIL-II-Studie zeigte zwar einen Trend zu niedrigerer Mortalität unter ZMapp (22 % vs. 37 % in der Kontrollgruppe), verfehlte jedoch das vorspezifizierte Signifikanzniveau aufgrund zu geringer Fallzahl durch das Abklingen der Epidemie.[12] In der nachfolgenden PALM-Studie, in der ZMapp als aktive Kontrollbedingung diente, lag die Mortalität unter ZMapp unerwartet bei 50 %. Sowohl MAb114 (Ansuvimab) als auch REGN-EB3 (Inmazeb) erwiesen sich in dieser Studie als ZMapp überlegen.[10] ZMapp hat keine reguläre Zulassung erhalten und wird klinisch nicht mehr weiterentwickelt.
TKM-Ebola (TKM-130803)
TKM-Ebola ist ein auf Small interfering RNA (siRNA) basierendes Therapeutikum, das zwei siRNA-Moleküle (siLpol-2 und siVP35-2) enthält, welche die virale Replikation durch RNA-Interferenz hemmen. In Primatenstudien zeigte sich ein vollständiger Schutz vor letaler EBOV-Infektion. Die FDA nahm das Präparat in das Fast-Track-Programm auf. Im Jahr 2015 wurde eine Phase-II-Studie mit schwer erkrankten EVD-Patienten in Sierra Leone jedoch vorzeitig abgebrochen, da ein vorspezifizierter statistischer Endpunkt erreicht wurde, der eine therapeutische Wirksamkeit als unwahrscheinlich einstufte.[13] Tekmira stellte die Weiterentwicklung von TKM-Ebola 2015 ein.
Favipiravir
Favipiravir (T-705) ist ein Virostatikum, das die virale RNA-Polymerase hemmt und ursprünglich für die Behandlung schwerer Influenza entwickelt wurde. Im Mausmodell konnte es bei früher Gabe den Krankheitsverlauf deutlich abschwächen. Die JIKI-Studie testete Favipiravir als ersten spezifischen Wirkstoff überhaupt in einem klinischen EVD-Trial. Die Ergebnisse zeigten einen möglichen Nutzen bei Patienten mit moderater Virämie (Ct-Wert ≥ 20), jedoch keine Wirksamkeit bei hochvirämischen Patienten im Endstadium.[14] Ein zusätzlicher pharmakokinetischer Befund erklärte die begrenzte Wirksamkeit teilweise: Die im Studienprotokoll angestrebten Plasmaspiegel wurden bei schwer erkrankten Patienten nicht erreicht und fielen zwischen Tag 2 und Tag 4 unerwartet ab.[15] Favipiravir ist für EVD nicht zugelassen. Eine weitere klinische Entwicklung für diese Indikation findet derzeit (2026) nicht statt.
Ouabain
Ouabain, ein Herzglykosid, das das Virusprotein VP24 hemmt, konnte in Zellkulturen die EBOV-Replikation blockieren. Klinische Studien beim Menschen wurden für diese Indikation nicht durchgeführt. Der Wirkstoff befindet sich nicht in der klinischen Entwicklung gegen EVD.
Morpholino-basierte Antisense-Oligonukleotide (PMOs)
Phosphorodiamidat-Morpholino-Oligomere (PMOs) richten sich sequenzspezifisch gegen das Ebolavirus-Genom und konnten in Primatenstudien eine letale EBOV-Infektion verhindern. Eine klinische Entwicklung in der Indikation EVD wurde bisher (2026) nicht weiterverfolgt.
Impfung
Für das Zaire-Ebolavirus stehen zwei in der EU zugelassene Impfstoffe zur Verfügung:
- Ervebo: Rekombinanter Lebendimpfstoff auf Basis des Vesikulären Stomatitis-Virus, bei dem das VSV-Oberflächenprotein durch das Glykoprotein des Zaire-Ebolavirus ersetzt wurde. Einmalige Impfung. EU-Zulassung im November 2019, FDA-Zulassung im Dezember 2019. Ringimpfungen mit Ervebo wurden während des Ausbruchs 2018–2020 in der DRK erfolgreich eingesetzt.[16]
- Zabdeno/Mvabea: Zweidosen-Impfschema (Primärimmunisierung + Auffrischung nach 8 Wochen) auf Basis adenoviraler und MVA-Vektoren. EU-Zulassung Juli 2020. Bietet Kreuzschutz gegen mehrere Filoviren (EBOV, SUDV, MARV, TAFV).
Für das Bundibugyo-Ebolavirus existieren derzeit (Mai 2026) keine zugelassenen Impfstoffe. Die WHO empfiehlt im Rahmen des laufenden Ausbruchs die zügige Durchführung klinischer Studien zur Erprobung von Impfstoffkandidaten und experimentellen Therapeutika.
Infektionsschutz
Aufgrund der hohen Infektiosität des Erregers wird die Behandlung von Ebola-Erkrankten auf Sonderisolierstationen durchgeführt. Die Versorgung in der Klinik erfolgt in Ganzkörperschutzanzügen mit gesicherter Atemluftzufuhr, in denen ein durchgehender Überdruck herrscht. In Deutschland stehen etwa 50 Betten auf Sonderisolierstationen zur Verfügung.
Für den Infektionsschutz sollten die Empfehlungen des Robert Koch-Instituts (RKI) sowie die europäischen Leitlinien zur persönlichen Schutzausrüstung beachtet werden. Zur Mindest-Schutzausrüstung gehören:[17]
- ein Schutzanzug der Kategorie III/Typ 3B
- Überschuhe
- Handschuhe
- Schutzbrille
- FFP3-Maske
Handschuhe, Brille und Maske werden mit Klebeband am Schutzanzug fixiert.
Cave: Die FFP3-Maske gewährleistet nur für einen begrenzten Zeitraum Schutz und schränkt die Atemfähigkeit deutlich ein. Eine Dekontamination ist wegen des fehlenden Gasfilterschutzes nur bedingt möglich.
Immunität
Eine überstandene Erkrankung nach Infektion mit Ebolaviren macht die betroffene Person immun gegen den auslösenden Erreger. Die Immunität erstreckt sich jedoch nicht auf andere Ebolaviren.
Ein bislang (2026) ungelöstes Problem der Ebola-Infektion ist, dass die Erreger offensichtlich in der Lage sind in Körperzonen zu überleben, die für das Immunsystem schlecht zugänglich sind. Dazu zählen u.a. die Hoden, das Rückenmark und der Augapfel. Im Sperma konnte bei 26 % der infizierten Männer noch 7 bis 9 Monate nach der Erkrankung Virus-RNA nachgewiesen werden. Ob dieser Befund auch mit einer Ansteckungsgefahr verbunden ist, ist jedoch unklar.[18]
Spätfolgen
Überlebende einer Ebola-Infektion können langfristige Beschwerden entwickeln, die unter dem Begriff „Post-Ebola-Syndrom" zusammengefasst werden. Bekannte Spätfolgen umfassen Arthralgien, ophthalmologische Störungen (insbesondere Uveitis) sowie neurologische Symptome. Diese werden vermutlich durch Autoimmunmechanismen verursacht. In Einzelfällen ist bei schwerem Verlauf eine entzündungshemmende Therapie (NSAR, Glukokortikoide) notwendig.
Meldepflicht
Der Verdacht einer Ebolainfektion, die Erkrankung und der Tod sind in Deutschland namentlich meldepflichtig. In Deutschland wurden bislang keine Fälle von Ebola-Fieber bekannt.
Quiz
Quellen
- ↑ Carette et al.: Ebola virus entry requires the cholesterol transporter Niemann-Pick C1. Nature 477 (7364): 340–3 PMID 21866103
- ↑ Deutsches Ärzteblatt – Zehn Jahre nach Ebola-Epidemie in Westafrika: Fortschritte, aber auch Probleme. 2024
- ↑ WHO: Statement on the 9th meeting of the IHR Emergency Committee regarding the Ebola outbreak in West Africa. März 2016.
- ↑ Unicef – Demokratische Republik Kongo: Hilfe für Ebolabetroffene, abgerufen am 18.05.2026
- ↑ 5,0 5,1 5,2 5,3 5,4 WHO: Epidemic of Ebola Disease caused by Bundibugyo virus in the DRC and Uganda determined a PHEIC. 17. Mai 2026.
- ↑ Bausch et al.: Assessment of the Risk of Ebola Virus Transmission from Bodily Fluids and Fomites. The Journal of Infectious Diseases Volume 196, Issue Supplement 2Pp. S142-S147
- ↑ Weingartl HM et al.: Transmission of Ebola virus from pigs to non-human primates. Nature Scientific Reports 2, Article number: 811 doi:10.1038/srep00811 Published 15 November 2012
- ↑ Schieffelin JS er al.: Clinical Illness and Outcomes in Patients with Ebola in Sierra Leone; NEJM October 29, 2014DOI: 10.1056/NEJMoa1411680
- ↑ FDA: Ebola – Emergency Use Authorizations and Approvals, abgerufen am 18.05.2026
- ↑ 10,0 10,1 Mulangu S et al.: A Randomized, Controlled Trial of Ebola Virus Disease Therapeutics. N Engl J Med. 2019;381(24):2293–2303.
- ↑ Corti D et al.: Protective monotherapy against lethal Ebola virus infection by a potently neutralizing antibody. Science. 2016;351(6279):1339–1342. doi:10.1126/science.aad5224
- ↑ PREVAIL II Writing Group: A Randomized, Controlled Trial of ZMapp for Ebola Virus Infection. N Engl J Med. 2016;375(15):1448–1456. doi:10.1056/NEJMoa1604330
- ↑ Dunning J, Sahr F et al.: Experimental Treatment of Ebola Virus Disease with TKM-130803: A Single-Arm Phase 2 Clinical Trial. PLoS Med. 2016;13(4):e1001997. doi:10.1371/journal.pmed.1001997
- ↑ Sissoko D et al.: Experimental Treatment with Favipiravir for Ebola Virus Disease (the JIKI Trial). PLoS Med. 2016;13(3):e1001967. doi:10.1371/journal.pmed.1001967
- ↑ Mentré F et al.: Favipiravir pharmacokinetics in Ebola-Infected patients of the JIKI trial reveals concentrations lower than targeted. PLoS Negl Trop Dis. 2017;11(2):e0005389. doi:10.1371/journal.pntd.0005389
- ↑ Henao-Restrepo AM et al.: Efficacy and effectiveness of an rVSV-vectored vaccine expressing Ebola surface glycoprotein: interim results from the Guinea ring vaccination cluster-randomised trial. Lancet. 2015;386(9996):857–66. doi:10.1016/S0140-6736(15)61117-5
- ↑ RKI – Hinweise zum beispielhaften An- und Ablegen von PSA für Fachpersonal, abgerufen am 18.05.2026
- ↑ Deen GF et al.: Ebola RNA Persistence in Semen of Ebola Virus Disease Survivors - Final Report N Engl J Med. 2017 Oct 12;377(15):1428-1437. doi: 10.1056/NEJMoa1511410
Bildquelle
- Bildquelle für Flexikon-Quiz: © Andrea Piacquadio / Pexels