Adenosinrezeptor
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonyme: A-Rezeptor, P1-Rezeptor, P1-Purinozeptor
Englisch: adenosine receptor, P1 receptor
Definition
Als Adenosinrezeptoren wird eine Familie von G-Protein-gekoppelten Rezeptoren bezeichnet, an die Adenosin als Ligand bindet. Sie sind eine Untergruppe der Purinozeptoren.
Biochemie
Struktur
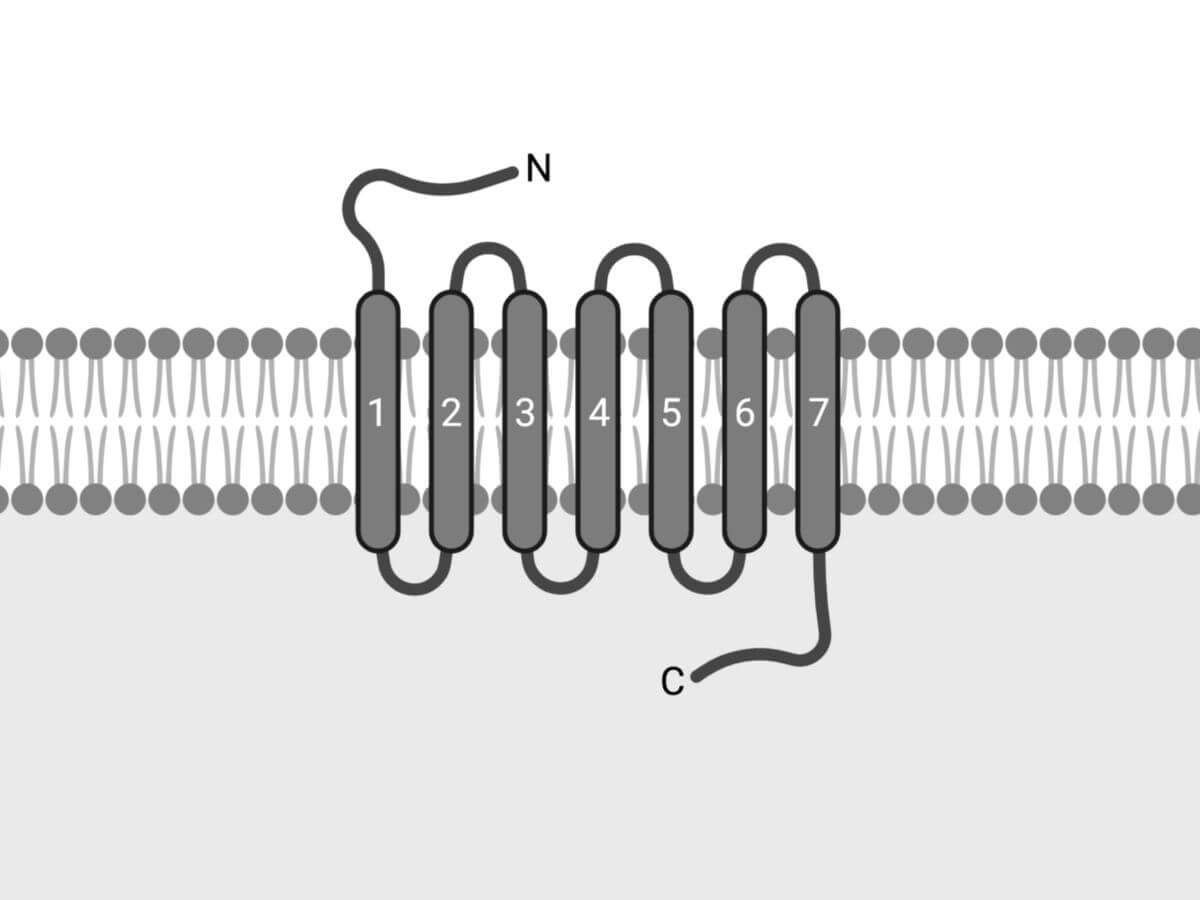
Adenosinrezeptoren bestehen aus sieben Transmembrandomänen, die durch drei extra- und drei intrazelluläre Schleifen miteinander verbunden sind. Dabei liegt der N-Terminus außerhalb und der C-Terminus innerhalb der Zelle.
Einteilung
Man unterscheidet vier verschiedene Adenosinrezeptoren:
- A1-Adenosinrezeptor: kodiert durch ADORA1-Gen auf Chromosom 1 (Genlokus 1q32.1)
- A2A-Adenosinrezeptor: kodiert durch ADORA2A-Gen auf Chromosom 22 (Genlokus 22q11.23)
- A2B-Adenosinrezeptor: kodiert durch ADORA2B-Gen auf Chromosom 17 (Genlokus 17p12)
- A3-Adenosinrezeptor: kodiert durch ADORA3-Gen auf Chromosom 1 (Genlokus 1p13.2)
Wirkmechanismus
Die A2A- und A2B-Adenosinrezeptoren vermitteln ihre Wirkung über ein stimulatorisches G-Protein (Gs), das die Adenylatcyclase (AC) aktiviert und einen Anstieg der intrazellulären cAMP-Konzentration auslöst. Dies führt zur Aktivierung der Proteinkinase A (PKA). Die Subtypen A1 und A3 hemmen die AC und somit die PKA über das inhibitorische G-Protein (Gi). Außerdem bewirken sie eine Stimulation der Phospholipase C (PLC) und damit der Proteinkinase C (PKC).
Des Weiteren können alle Subtypen an die Signalwege der MAPK gekoppelt sein, die eine große Rolle bei der Regulation der Proliferation, der Differenzierung und der Apoptose spielt.
Die vielseitigen Effekte von Adenosin hängen nicht nur von der Expressionsdichte der einzelnen Subtypen in verschiedenen Geweben ab, sondern auch von der extrazellulären Adenosinkonzentration. Während A1-, A3- und A2A-Rezeptoren schon auf Adenosinkonzentrationen im nanomolaren Bereich reagieren, ist für die Stimulation von A2B-Rezeptoren eine höhere Konzentration notwendig.
Jeder Rezeptortyp hat unterschiedliche Funktionen, die sich z.T. überlappen. Im Vordergrund steht – als eine der wichtigsten Aufgaben des Adenosins – der Schutz von Zellen und Geweben vor Schäden durch Hypoxie, Traumata, Hypertension und Anfallsleiden.
A1-Rezeptoren
Der A1-Rezeptor ist am stärksten im zentralen Nervensystem (ZNS) exprimiert. Es reduziert die Ausschüttung von exzitatorischen Neurotransmittern (z.B. Glutamat) und reguliert die neuronale Aktivität auf prä- und postsynaptischer Ebene. Eine überschießende Ausschüttung von Neurotransmittern (z.B. bei Stress, Traumata, Krampfanfällen) wird somit verhindert. Die Aktivierung des Rezeptors führt zu sedativen, anxiolytischen und antikonvulsiven Effekten sowie einer Minderung der Schmerzwahrnehmung. Durch Hemmung von cholinergen Neuronen im basalen Frontalhirn und Aktivierung des Nucleus praeopticus ventrolateralis im Hypothalamus wirkt es schlaffördernd.
Weiterhin schützt der A1-Rezeptor das Herz und andere Organe über eine PKC-vermittelte Aktivitätssteigerung der ATP-abhängigen Kaliumkanäle der Mitochondrien vor kurzzeitigen hypoxischen Zuständen. Am Herzen wirkt Adenosin negativ-inotrop, -dromotrop und -chronotrop und hemmt die Ausschüttung von Katecholaminen.
In der Niere ist der A1-Rezeptor für eine Vasokonstriktion der afferenten Arteriolen verantwortlich. Die Rezeptoraktivierung verringert somit die glomeruläre Filtrationsrate (GFR) und den renalen Blutfluss.
In Fettzellen bewirkt der A1-Rezeptor eine Reduktion der Lipolyse. Außerdem führen A1-Rezeptoren zu einer Bronchokonstriktion. Des Weiteren stimulieren A1-Rezeptoren die Differenzierung von Osteoklasten. Sie spielen damit eine wichtige Rolle in der Regulation der Knochenhomöostase.
A2A-Rezeptoren
A2A-Rezeptoren können Heteromere mit anderen Rezeptor-Untereinheiten ausbilden, z.B. mit A1-, D3- oder CB1-Rezeptoren.
A2A-Rezeptoren finden sich v.a. in den Basalganglien und in Immunzellen. Im Gehirn bewirken sie eine Steigerung der Freisetzung von Acetylcholin, Noradrenalin und Glutamat. In den Basalganglien steigern sie die Freisetzung von GABA und hemmen somit indirekt die Ausschüttung von Dopamin. A2A-Rezeptoren stimulieren zudem die Schmerzwahrnehmung.
Des Weiteren bewirken A2A-Rezeptoren eine Vasodilatation (z.B. der Koronararterien oder der Meningealgefäße) und eine verminderte Thrombozytenaggregation. Im Fall eines ischämischen Insults verringert Adenosin über eine Aktivierung von A2A-Rezeptoren die Entzündungsreaktion nach Reperfusion. Außerdem wird die Wundheilung und die Angiogenese angeregt.
Adenosin vermittelt seine immunsuppressive, antiinflammatorische Wirkung, insbesondere über den A2A-Rezeptor. Dieser vermindert die Ausschüttung von proinflammatorischen Zytokinen (z.B. TNF-alpha und Interleukin-2). Die Aktivierung und Reifung von T-Zellen, Makrophagen und NK-Zellen wird gehemmt.
Im Pankreas vermittelt es eine vermehrte Ausschüttung von Glukagon. Im Knochen hemmt der Rezeptor die Differenzierung von Osteoklasten und stimulieren die Aktivität von Osteoblasten.
A2B-Rezeptoren
A2B-Rezeptoren kommen ubiquitär im Körper vor. In kardialen Fibroblasten führt der Rezeptor zu einer Hemmung des Zellproliferation und der Kollagensynthese. Die Expression in Endothelzellen fördert ihre Proliferation und somit die Angiogenese. In Mesenterial-, Lungen- und Koronararterien wirkt Adenosin vasodilatatorisch.
Auf Immunzellen (z.B. Mastzellen) fördert es die Produktion und Degranulation von inflammatorischen Zytokinen. Weiterhin beeinflusst es die Aktivität von CFTR im Darm- und Bronchialepithel. Im Knochen stimulieren A2B-Rezeptoren die Differenzierung von Osteoblasten.
A3-Rezeptoren
A3-Rezeptoren sind ebenfalls in den meisten Geweben vorhanden. Im Gehirn vermitteln sie neuroprotektive Effekte. Ihre Aktivierung stabilisiert in kurzen ischämischen Phasen das Zytoskelett und verhindert die Einleitung der Apoptose. Bei längerer Ischämie steigert Adenosin hingegen die Apoptose.
Außerdem spielt der A3-Rezeptor wie der A2A-Rezeptor eine Rolle bei Entzündungs- und Immunreaktionen. Beispielsweise hemmt Adenosin die Ausschüttung von TNF-α aus neutrophilen Granulozyten sowie die Chemotaxis von eosinophilen Granulozyten.
Klinik
Adenosinrezeptoren spielen eine wichtige pathophysiologische Rolle bei einer Vielzahl an Erkrankungen, z.B.:
- A2B-Rezeptoren: bei Asthma bronchiale und COPD
- A2A-Rezeptoren: bei rheumatoider Arthritis und Morbus Parkinson
Pathologisch erhöhte Adenosinkonzentrationen in Malignomen können zu einer lokalen, tumorinduzierten Immunsuppression führen. Daher können die Adenosinrezeptoren als Immuncheckpoint angesehen werden, der ein potentieller Ansatz in der onkologischen Immuntherapie ist.
Pharmakologie
Agonisten
Bei rascher intravenöser Bolusinjektion blockiert Adenosin über Aktivierung des A1-Rezeptors die AV-Überleitung. Daher wird es bei supraventrikulären Tachyarrhythmien verwendet. Außerdem wird es bei Herzkatheteruntersuchungen verabreicht, um eine Hyperämie auszulösen und die fraktionelle Flussreserve zu bestimmen.
Weitere Agonisten sind z.B. Regadenoson (A2A), Cannabidiol (A2A) und Baldrian (A1).
Antagonisten
Als Antagonisten wirken:
- Coffein (A1, A2A)
- Theophyllin (A1, A2A, A2B, A3): Einsatz bei postspinalem Kopfschmerz und bei Asthma bronchiale
- Theobromin
- Istradefyllin (A2A): Verwendung bei Morbus Parkinson im Rahmen von klinischen Studien
Merkhilfe
Mit der Eselsbrücke "ISI" (gesprochen "EASY") kann man sich die G-Proteine merken, die mit den unterschiedlichen Adenosinrezeptoren gekoppelt sind:
- A1 → I (Gi-Protein)
- A2 → S (Gs-Protein)
- A3 → I (Gi-Protein)
Literatur
- Kurzlehrbuch Pharmakologie und Toxikologie; Georg Thieme Verlag; Stuttgart, New York