Rheumatoide Arthritis
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonyme: chronische Polyarthritis (CP), primär chronische Polyarthritis (PCP)
Laienbegriff: Rheuma
Englisch: Rheumatoid arthritis
Definition
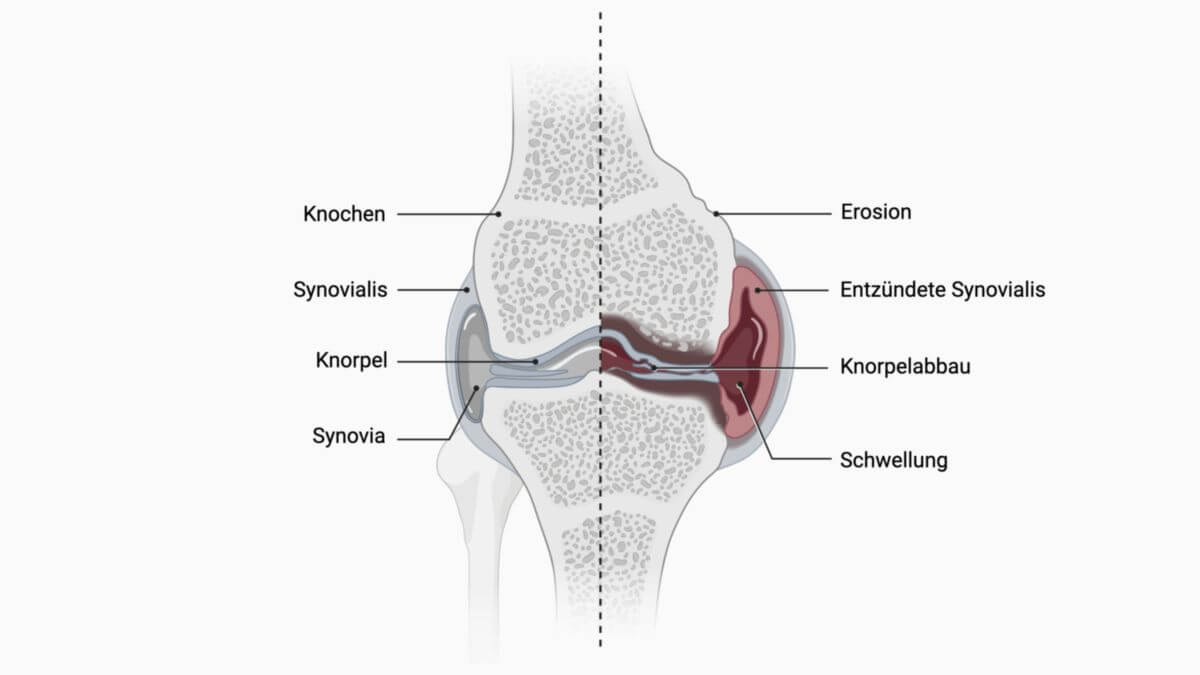
Die rheumatoide Arthritis, kurz RA, ist eine chronisch-entzündliche Systemerkrankung, welche die Innenhaut (Synovialis) der Gelenke befällt und dadurch das klinische Bild einer Polyarthritis hervorruft. Fakultativ können auch andere Organe betroffen sein. Die Erkrankung zeigt einen schubweisen, progredienten Verlauf, der ohne adäquate Behandlung zur Zerstörung der Gelenke und zu schwerwiegenden Behinderungen bis zur Invalidität führen kann.
ICD10-Codes
- M05: Seropositive chronische Polyarthritis
- M06: Sonstige chronische Polyarthritis
Epidemiologie
Die rheumatoide Arthritis hat eine weltweite Prävalenz von ungefähr 0,5 bis 1,0 %.[1] Die jährliche Inzidenz variiert zwischen 12 und 1.200 Fällen pro 100.000 Personen pro Jahr, abhängig vom Geschlecht und von der ethnischen Herkunft.[2] Nach der aktivierten Arthrose ist sie die häufigste inflammatorische Gelenkerkrankung. Frauen sind etwa dreimal so häufig betroffen wie Männer. Der Manifestationsgipfel liegt ungefähr zwischen dem 45. und 65. Lebensjahr. Familiäre Häufungen sind zu beobachten.
Ätiologie
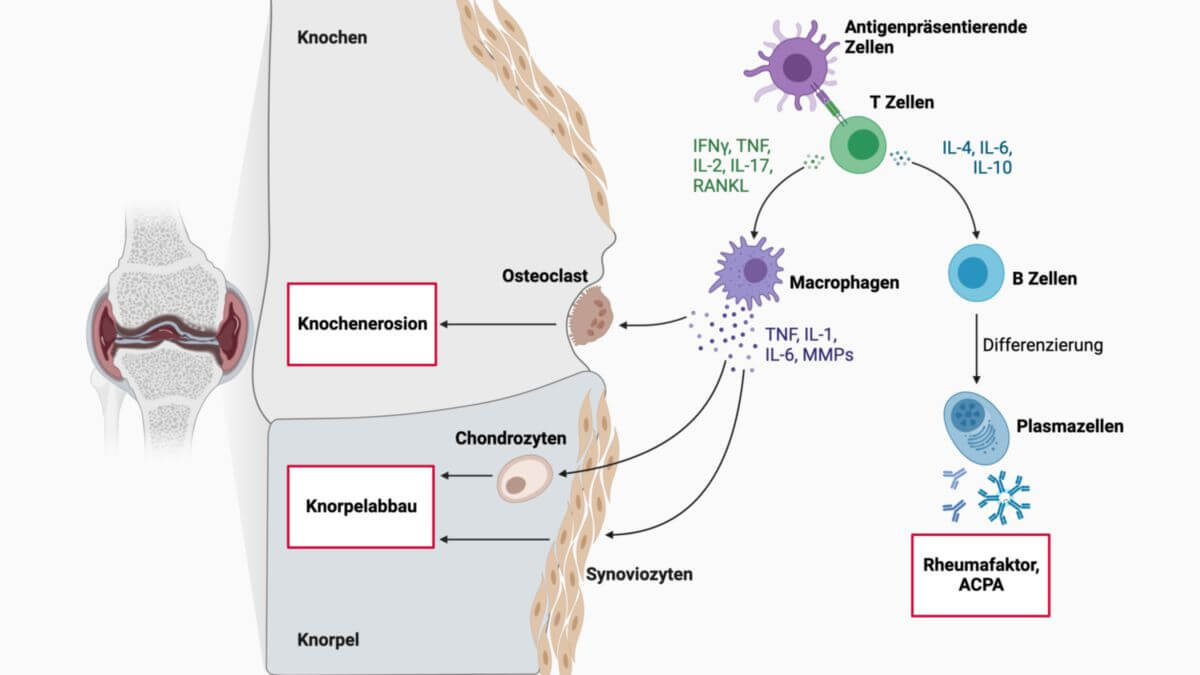
Die genauen Ursachen der rheumatoiden Arthritis sind derzeit (2026) zum größten Teil ungeklärt. Es handelt sich um eine Autoimmunerkrankung, bei der bestimmte körpereigene Gewebe (z.B. Gelenkknorpel) und Bindegewebe vom Immunsystem, nämlich von Antikörpern und Phagozyten angegriffen werden. Es wird vermutet, dass Viren und Bakterien pathogenetisch mitbeteiligt sind.
Für die Erkrankung besteht eine genetische Disposition: Die rheumatoide Arthritis tritt familiär gehäuft auf und ist mit bestimmten MHC- bzw. HLA-Merkmalen assoziiert. Die Mehrheit der Patienten teilt ein kurzes Sequenzmotiv ("Shared Epitope"), das von mehreren HLA-DRB1-Allelen kodiert wird. In der kaukasischen, nordeuropäischen und nordamerikanischen Bevölkerung handelt es sich häufig um die Aminosäuresequenz-Variante "QKRAA", die hauptsächlich vom HLA-DRB1*04:01-Allel (HLA-DR4) kodiert wird. Darüber hinaus sind zwei weitere Sequenzvarianten bekannt, die u.a. von den HLA-DRB1-Allelen *01:01, *04:04, *04:05, *04:08 und *14:02 kodiert werden. Das Vorhandensein eines Shared Epitopes erhöht das Risiko für eine RA und für einen schwereren Krankheitsverlauf.[3]
Klinik
Initialphase
In der Initialphase zeigen sich Allgemeinsymptome:
- Abgeschlagenheit
- Subfebrile Temperaturen
- Nachtschweiß
- Myalgien
Arthritis
Im weiteren Verlauf kommt es schließlich zu den typischen Manifestationen am Bewegungsapparat:
- Periphere Arthritis v.a. an kleinen Gelenken der Hände und Füße (außer DIP) mit typischerweise polyartikulärem symmetrischen Verteilsmuster
- Morgensteifigkeit der Gelenke von mindestens 60 Minuten Dauer
- Rheumaknoten (v.a. subkutan und an Sehnen)
- Karpaltunnelsyndrom
- Sulcus-ulnaris-Syndrom
- Baker-Zyste
- Ulnardeviation der Langfinger
Extraartikuläre Manifestationen
Extraartikulär manifestiert sich die Erkrankung vor allem an:
- Herz: Perikarditis, Perikarderguss, granulomatöse Myokarditis, Klappenveränderungen
- Lunge (siehe Hauptartikel: CTD-ILD)
- interstitielle Lungenerkrankung bei 5 bis 10 % d.F; meist mit UIP-Muster.
- kleine Atemwege: follikuläre Bronchiolitis, Bronchiolitis obliterans
- große Atemwege: Bronchiektasie
- nekrobiotische pulmonale Rheumaknoten
- Pleura: Pleuritis, Pleuraerguss
- Leber: erhöhte Leberenzyme
- Niere: selten Glomerulonephritis
- Auge: Keratokonjunktivitis sicca, Skleritis, Epikleritis
- Gefäße: rheumatoide Vaskulitis, selten und oft nach langjährigem und schwerem Verlauf; sehr variable Klinik, äußert sich primär an der Haut oder als Polyneuropathie
Komplikationen
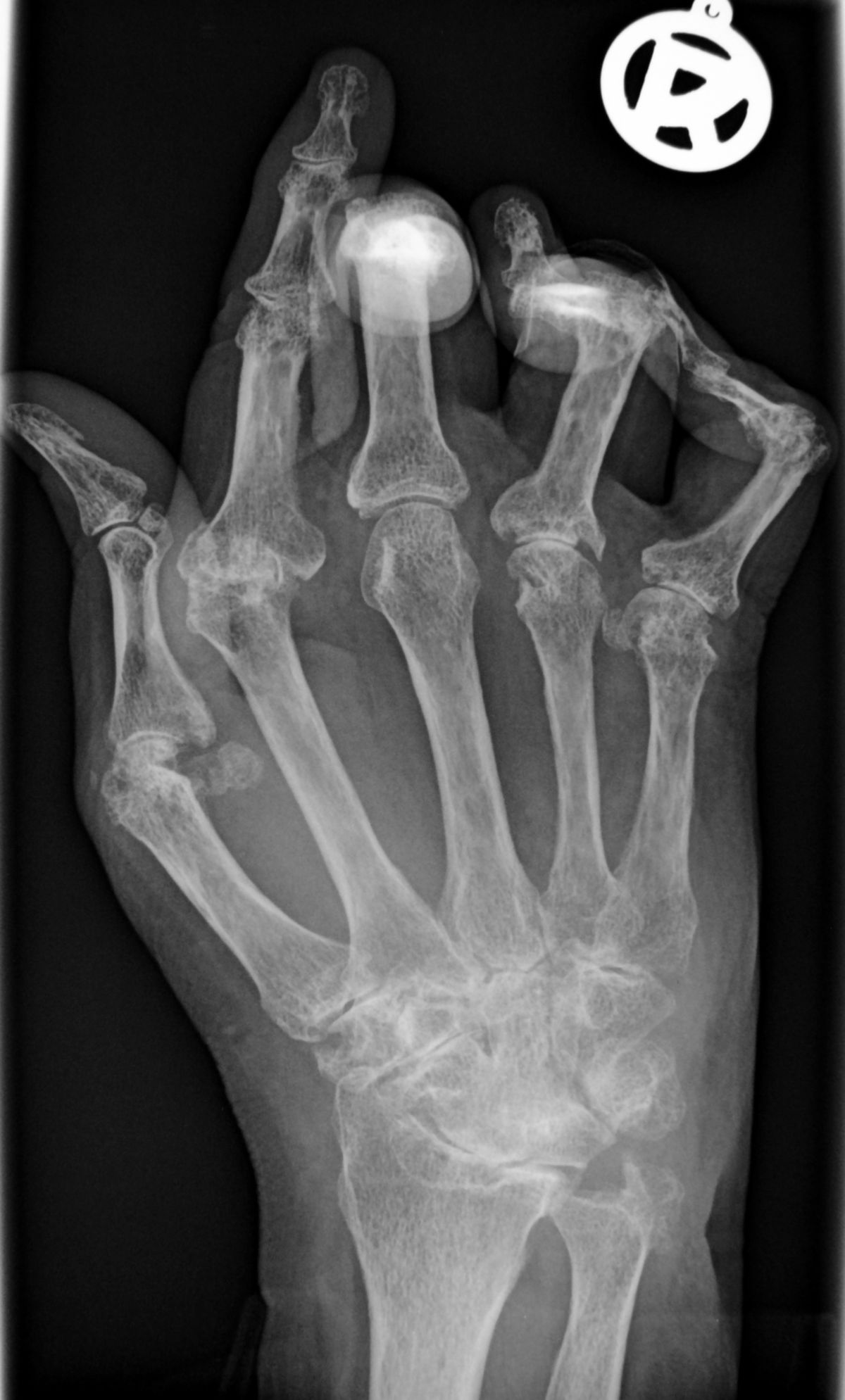
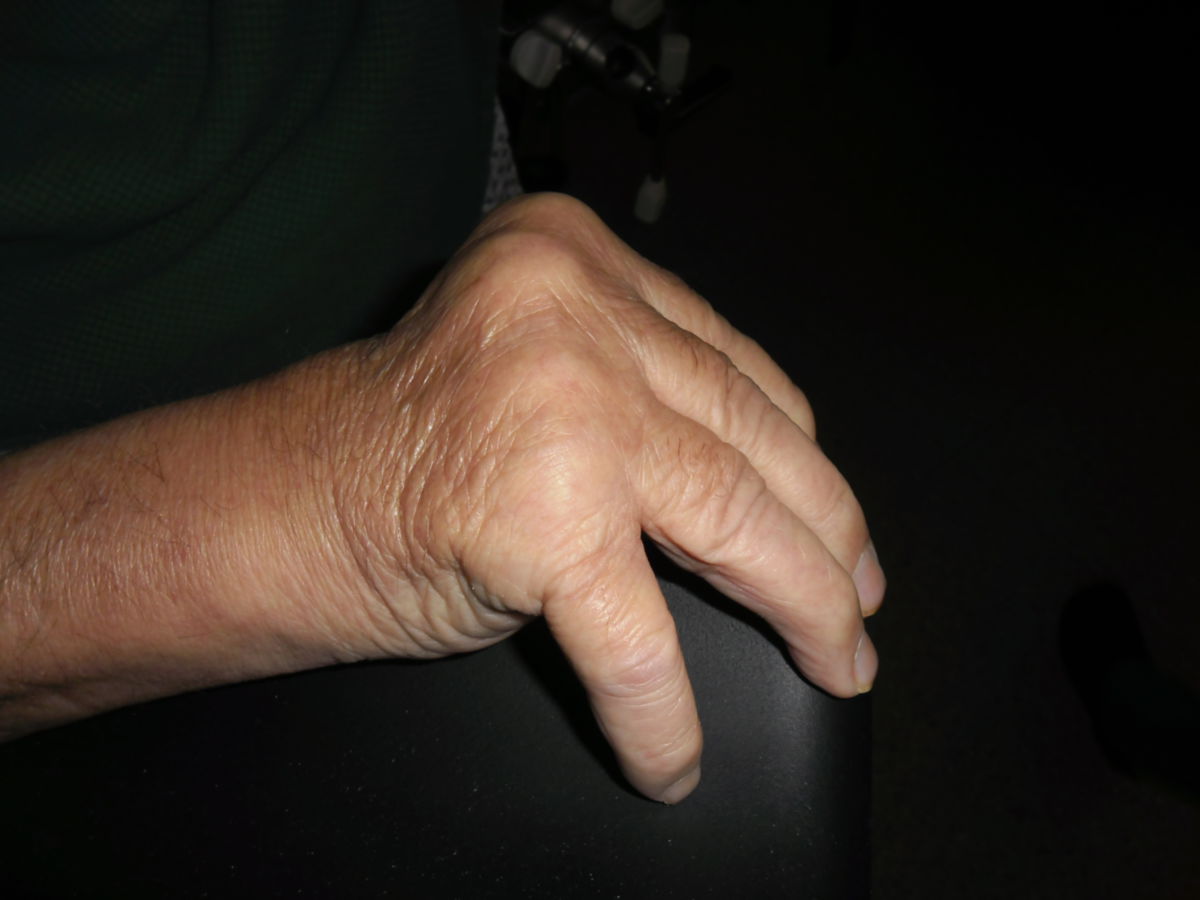
Bei besonders schweren Verläufen oder in unbehandeltem Zustand kommt es zu einer zunehmenden Destruktion der Gelenke mit typischen Deformitäten und großen Einschränkungen der Beweglichkeit sowie der Mobilität.
Charakteristische Deformitäten der Hand werden als rheumatische Hand bezeichnet. Dazu gehören:
- Deviation der Finger nach ulnar
- Knopflochdeformität (PIP gebeugt, DIP überstreckt)
- Schwanenhalsdeformität (PIP überstreckt, DIP gebeugt)
- 90-90-Deformität (Daumengrundgelenk gebeugt, Endgelenk überstreckt)
- Atrophie der Musculi interossei
- Verkürzung der Handwurzel
- Rheumaknoten
- Nagelfalz-Vaskulitis
An den Füßen können ebenfalls Deformitäten auftreten, dazu gehören:
Zudem können die Organbeteiligungen zu zahlreichen Organkomplikationen führen.
Sonderformen
- Caplan-Syndrom: RA + Silikose
- Felty-Syndrom: schwere Form der RA mit Neutropenie und Splenomegalie
- verschiedene Formen der juvenilen idiopathischen Arthritis (JIA)
Diagnostik
Die Basisdiagnostik bildet die klinische Untersuchung der betroffenen Körperpartien. Darüber hinaus stehen die Bildgebung und Laboruntersuchungen im Vordergrund.
Klinische Untersuchung
- Inspektion und Palpation: Druckschmerz, prallelastische Schwellung, Überwärmung, Krepitation, Sehnenknoten
- Funktionsprüfung: aktive und passive Beweglichkeit (Neutral-Null-Methode), Bandstabilität, Muskelkraft
- Querdruckschmerz im Bereich der Finger- und Zehengrundgelenke (Gaenslen-Zeichen)
Bildgebung
- Gelenksonographie: Nachweis von Synovialitis, Tendinitis, Bursitis und Zysten
- MRT: Knochenmarksödem erkennbar (Frühzeichen), Inflammation, Erosionen
- Skelettszintigrafie: Nachweis der Synovialitis bzw. Arthritis in den Frühaufnahmen
- Röntgen: Hände und Handgelenke, Vorfuß, Dens axis
siehe Hauptartikel: Rheumatoide Arthritis (Radiologie)
Labor
Primärdiagnostik
- Erythrozytensedimentationsrate (BSG)
- C-reaktives Protein (CRP)
- Rheumafaktor (RF)
- Blutbild
- Ferritin als Akute-Phase-Protein
- CCP-Antikörper
- Synoviaanalyse
CCP-Antikörper sind Antikörper gegen citrullinierte Peptide. Sie werden auch als ACPA (Anti citrullinated peptide/protein antibodies) bezeichnet und sind weitaus spezifischer als der Rheumafaktor. Dadurch verbessern sie den serologischen Nachweis bedeutend. Insbesondere das CCP-Assay und die ACPA-MCV-ELISA weisen eine Sensitivität von 80 % und eine Spezifität von nahezu 98 % auf.
Die rheumatoide Arthritis unterscheidet sich von anderen ("seronegativen") Arthritiden durch den Nachweis von Rheumafaktoren oder CCP-Antikörpern. Daher wird sie auch als seropositive chronische Polyarthritis bezeichnet. Der Nachweis von CCP-Antikörpern und RF in Kombination hat einen sehr hohen positiven Vorhersagewert für eine rheumatoide Arthritis.
Verlaufskontrolle
BSG und CRP korrelieren mit der entzündlichen Aktivität der Erkrankung und einem progressiv destruierenden Verlauf. Ein Rückgang der Werte unter Therapie weist auf einen guten therapeutischen Effekt hin und ist daher ein Surrogatparameter für die Unterdrückung der entzündlichen Gelenkdestruktion. Rheumafaktoren und die Höhe der CCP-Antikörper eignen sich dagegen nicht als Verlaufsparameter der entzündlichen Krankheitsaktivität.
Diagnostische Kriterien
ACR/EULAR-Kriterien
Das American College of Rheumatology (ACR) hat 2010 gemeinsam mit der European League Against Rheumatism (EULAR) die sogenannten ACR/EULAR-Klassifikationskriterien definiert, anhand derer die Diagnose "Rheumatoide Arthritis" mithilfe eines Punktsystems gestellt werden kann:
| Punkte | Gelenkbeteiligung | Serologie | Entzündungsparameter | Symptomdauer |
|---|---|---|---|---|
| 0 | ≤ 1 großes Gelenk | RF + ACPA neg. | CRP + BSG normal | < 6 Wochen |
| 1 | 2 - 10 große Gelenke | CRP + BSG ↑ | ≥ 6 Wochen | |
| 2 | 1 - 3 kleine Gelenke | RF + ACPA ↑ | ||
| 3 | 4 - 10 kleine Gelenke | RF + ACPA ↑↑ | ||
| 5 | > 10 Gelenke, davon ≥ 1 kleines Gelenk |
Die Interphalangealgelenke, Metacarpophalangealgelenke, Metatarsophalangealgelenke und Handgelenke werden dabei als kleine Gelenke, Schultergelenk, Ellenbogengelenk, Hüftgelenk, Kniegelenk und Sprunggelenk als große Gelenke gewertet. In jeder Spalte wird dann der höchste erreichbare Punktwert vergeben. Eine RA liegt vor, wenn sich ein Punktwert ≥ 6 ergibt und gleichzeitig eine gesicherte Gelenkentzündung an typischer Stelle ohne andere erkennbare Ursache (z.B. Trauma, Arthrose) vorliegt.
Ältere ACR-Kriterien
Die älteren, nicht mehr gültigen ACR-Kriterien von 1987 legten die Diagnosekriterien wie folgt fest:
- Morgensteifigkeit von mindestens 60 Minuten Dauer
- Gelenkschwellungen oder Gelenkerguss an mindestens 3 Gelenkregionen
- Arthritis der Hand- und/oder Fingergelenke
- Symmetrischer Befall derselben Gelenke beider Körperhälften
- Vorliegen von Rheumaknoten
- Positiver Rheumafaktor und/oder ACPA im Serum
- Gelenknahe Osteoporose oder Erosionen im Röntgen
Eine rheumatoide Arthritis lag demnach vor, wenn ein Patient mindestens 4 von 7 Kriterien erfüllte. Die ersten 4 Kriterien mussten über einen Zeitraum von mindestens 4 bis 6 Wochen bestehen.
Therapie
Pharmakotherapie
Wirkstoffe
Die medikamentöse Therapie der RA kann mit folgenden Wirkstoffen erfolgen:
- Glukokortikoide
- Analgetika
- NSAIDs
- Unselektive Cyclooxygenase-Hemmer (Ibuprofen, Diclofenac, Naproxen)
- Selektive COX-2-Hemmer (Coxibe z.B. Etoricoxib)
- Basistherapeutika (Disease modifying antirheumatic drugs, DMARDs)
- Konventionelle synthetische Wirkstoffe ("csDMARDs")
- Methotrexat (MTX)
- Azathioprin
- Ciclosporin A (CIA)
- Leflunomid (LEF)
- Sulfasalazin (SSZ)
- Penicillamin
- Cyclophosphamid
- Hydroxychloroquin (HCQ)
- Goldpräparate (Auranofin)
- Gezielte synthetische Wirkstoffe ("tsDMARDs")
- Biologika ("bDMARDs")
- Anti-TNF-α-Therapeutika: Adalimumab, Infliximab, Etanercept, Golimumab, Certolizumab
- Interleukin-Blocker: Anakinra, Tocilizumab
- Rituximab
- Abatacept
- Konventionelle synthetische Wirkstoffe ("csDMARDs")
Vorgehen
Im akuten Schub wird die RA symptomatisch mit NSAIDs oder Coxiben behandelt. Zusätzlich erfolgt die systemische Gabe von Glukokortikoiden, um die Entzündungsaktivität zu reduzieren. Bei sehr starker Symptomatik können Glukokortikoide auch intraartikulär injiziert werden.
Die langfristige Therapie basiert auf der Gabe von DMARDs. Ihr Wirkeintritt dauert einige Wochen, so dass diese Zeit mit NSAID und/oder Glukokortikoiden überbrückt werden muss. Das Mittel der Wahl bei mittelschwerer bis schwerer RA ist Methotrexat (initial: 15 mg/Woche). Alternativ kommen u.a. Leflunomid und Sulfasalazin in Frage. Wenn unter dieser Therapie nach 4 bis 6 Wochen keine Besserung erzielt wird, werden Kombinationen verschiedener DMARDs eingesetzt (z.B. MTX + LEF oder MTX + SSZ + HCQ). Als weitere Eskalationsstufe kommt nach weiteren 3 Monaten der Einsatz von Biologika in Betracht.[4]
Es besteht eine hohe Evidenz, dass durch einen frühen Therapiebeginn mit dem Ziel einer vollständigen Krankheitsremission ("treat to target") die Prognose der Erkrankung deutlich verbessert wird. Daraus ergibt sich die Forderung nach einer frühen Diagnosestellung und Behandlung möglichst innerhalb der ersten drei bis sechs Monate nach Beschwerdebeginn.
Wechselwirkungen
Die richtige Koordination der verwendeten Arzneistoffe spielt eine wichtige Rolle. Zum Beispiel hat Methotrexat zahlreiche Wechselwirkungen, die beachtet werden müssen. Die Elimination von Methotrexat wird durch die gleichzeitige Einnahme nicht-steroidaler Entzündungshemmer (z.B. Ibuprofen) gehemmt, wodurch die toxische Wirkung verstärkt werden kann.
Weitere konservative Maßnahmen
Physiotherapie
Ergotherapie
- Verbesserung der Beweglichkeit, Kraft und Geschicklichkeit
- Erhalt der Selbstständigkeit im Alltag
Physikalische Therapie
Hilfsmittelversorgung
- Hilfsmittel (z.B. AUD-Schiene)
- Orthopädische Schuhversorgung
Invasive Therapiemaßnahmen
In der Frühphase kann eine Synovektomie den Krankheitsbeginn günstig beeinflussen. Eine weitere Therapieoption ist die Durchführung einer Radiosynoviorthese (RSO) – vor allem bei therapieresistenten Beschwerden oder länger bestehenden Monarthritiden.
Bei Versagen aller anderen Maßnahmen sind chirurgische Rekonstruktionen (z.B. Arthrodese, Arthroplastik) eine Alternative.
Verlaufskontrolle
Das Ziel einer frühen und effektiven Behandlung erfordert eine regelmäßige Erfassung und Dokumentation der Krankheitsaktivität und des Verlaufs. Dazu hat sich in der Praxis als Standard der Disease Activity Score (DAS28) bewährt, in dem verschiedene Parameter der Krankheitsaktivität eingehen. Es handelt sich um einen zusammengesetzten Score aus der Anzahl druckschmerzhafter und geschwollener Gelenke von insgesamt 28 beurteilten Gelenken, der Einschätzung der Krankheitsaktivität in den letzten 7 Tagen durch den Patienten selbst anhand einer visuellen Analogskala und der Erfassung der serologischen Entzündungszeichen (BSG in mm/h, CRP in mg/l). Werte < 2,6 sprechen für eine gut kontrollierte Erkrankung im Sinne einer Remission. Werte > 3,2 deuten auf eine nicht ausreichende Kontrolle der Krankheitsaktivität hin, die in der Regel eine Änderung der Therapie erfordert.
Weitere Scores zur Überprüfung der Krankheitsaktivität sind der Simplified Disease Activity Index (SDAI) und der Clinical Disease Activity Index (CDAI).
Darüber hinaus werden zur Verlaufskontrolle auch standardisierte Fragebögen zum Gesundheitszustand (Health Assessment Questionnaire (HAQ)) und zu krankheitsbedingten Funktionsstörungen (z.B. Funktionsfragebogen Hannover) eingesetzt.
Zur Dokumentation der radiologischen Progression sollte bei deutlich aktiver Erkrankung nach sechs und zwölf Monaten eine Nativaufnahme erfolgen. Danach wird eine jährliche Kontrolle empfohlen.
Prognose
Bei Patienten mit einer RA ist nach längerer Erkrankung ein hoher Grad an Erwerbsunfähigkeit sowie eine Verkürzung der Lebenszeit um drei bis zwölf Jahren beschrieben. Eine rechtzeitige und adäquate Therapie kann dem jedoch entgegenwirken.
Fortbildung
Quiz
Bildquelle
- Bildquelle für Flexikon-Quiz: © SHVETS production / Pexels
Quellen
- ↑ Silman AJ, Pearson JE Epidemiology and genetics of rheumatoid arthritis, Arthritis Res. 2002; 4(Suppl 3): S265–S272, abgerufen am 08.07.2019
- ↑ Gabriel SE The epidemiology of rheumatoid arthritis, Rheum Dis Clin North Am. 2001 May;27(2):269-81, abgerufen am 08.07.2019
- ↑ De Almeida et al., New Insights into the Functional Role of the Rheumatoid Arthritis Shared Epitope. FEBS Letters, 2012.
- ↑ Fiehn, C et al. S2e-Leitlinie: Therapie der rheumatoiden Arthritis mit krankheitsmodifizierenden Medikamenten Z Rheumatol 2018, 77 (Suppl 2):S35–S53, abgerufen am 16.07.2019