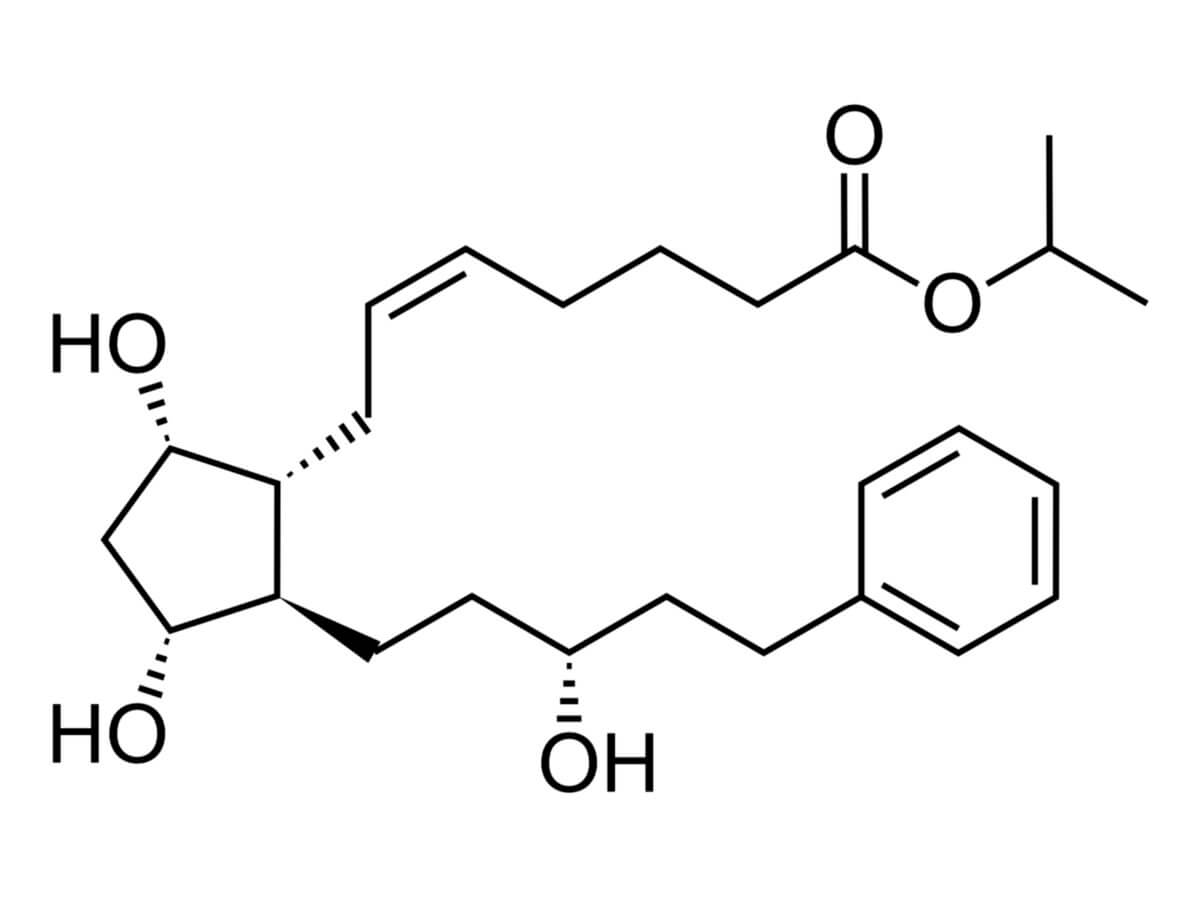
Latanoprost
Handelsnamen: Arulatan®, Monoprost®, Xalatan®
Synonyme: Latanoprostum, PhXA41
Englisch: latanoprost
Definition
Latanoprost ist ein Arzneistoff zur Senkung des erhöhten Augeninnendrucks (IOD).[1]
Chemie
Latanoprost ist ein Analogon von Prostaglandin-F2α. Die Summenformel ist C26H40O5. Chemische Namen sind:
- Propan-2-yl (Z)-7-[(1R,2R,3R,5S)-3,5-dihydroxy-2-[(3R)-3-hydroxy-5-phenylpentyl]cyclopentyl]hept-5-enoat (IUPAC)
- Isopropyl-(5Z,15R)-9α,11α,15-trihydroxy-17-phenyl-18,19,20-trinor-prost-5-en-1-oat (INN)
Die molare Masse beträgt 432,60 g/mol, der Oktanol-Wasser-Koeffizient (logP) 4,16. Die CAS-Nummer lautet 130209-82-4.
Die Substanz liegt bei Raumtemperatur als leicht gelbliche, ölige Flüssigkeit vor. In Wasser ist der Arzneistoff praktisch unlöslich (0,0129 mg/mL), in DMSO und Ethanol hingegen löslich.
Wirkmechanismus
Der uveosklerale Transport von Kammerwasser über Gefäße von Ziliarkörper und Iris hat bei jüngeren Menschen einen Anteil von bis zu 30 % am Kammerwassertransport. Dieser Anteil sinkt mit steigendem Alter, wodurch sich die Glaukomanfälligkeit erhöht. Latanoprost verbessert den uveoskleralen Kammerwasserabfluss.
Als Wirkmechanismus wird der Agonismus an Prostaglandin-F2α-Rezeptoren angegeben. In der Folge steigt die Expression von Metalloproteasen im Musculus ciliaris und das Remodeling der extrazellulären Matrix wird angeregt. Dadurch soll das Gewebe durchgängiger für das Kammerwasser werden. Der gewünschte Effekt ist eine Senkung des Augeninnendrucks.
Experimentelle Studien deuten darauf hin, dass Latanoprost möglicherweise auch direkte neuroprotektive Eigenschaften besitzt. So konnte die Überlebensrate von retinalen Ganglienzellen erhöht und die Expression neuroprotektiver Faktoren wie BDNF (Brain-Derived Neurotrophic Factor) in der Netzhaut stimulieren werden.[2]
Pharmakokinetik
Latanoprost ist ein Prodrug, in dem der Wirkstoff als Ester mit lipophilen Eigenschaften vorliegt.[1] In der veresterten Form ist der Wirkstoff besser bioverfügbar und wird zudem als Depot in der Hornhaut (Kornea) gespeichert, sodass eine einmal tägliche Applikation ausreichend ist.
Das Prodrug wird in der Hornhaut von Esterasen durch Hydrolyse des Isopropyl-Esters zu aktiver Latanoprostsäure und Isopropanol gespalten. Die Wirkung tritt etwa 3 bis 4 h nach topischer Applikation ein, das Wirkungsmaximum wird 8 bis 12 h nach topischer Applikation erreicht. Dabei werden Spitzenkonzentration im Kammerwasser nach etwa 2 h erreicht. Die Wirkungsdauer beträgt mehr als 24 h. Das Verteilungsvolumen wird mit 0,16 ± 0,02 L/kgKG angegeben.
Metabolisierung
Der Wirkstoff wird in der Leber durch Fettsäure-β-Oxidation zu unwirksamen Metaboliten (1,2-Dinor- und 1,2,3,4-Tetranorlatanoprostsäure) umgewandelt. Die biologische Halbwertszeit liegt bei 17 min nach topischer Applikation.
Elimination
Die systemische Clearance beträgt 7 mL/min/kgKG. Die Exkretion der Metaboliten erfolgt überwiegend über die Niere (88 % der Dosis nach topischer, 98 % nach i.v.-Applikation).
Indikationen
Die Anwendung von Latanoprost ist bei folgenden Erkrankungen indiziert:[3]
- Offenwinkelglaukom (Weitwinkelglaukom)
- Okuläre Hypertonie
- Erhöhter Augeninnendruck/Glaukome in der Pädiatrie
Darreichungsform
Latanoprost steht in Form von Augentropfen mit einer Wirkstoffkonzentration von 50 µg/mL in Tropfflaschen und in Einzeldosisbehältnissen zur Verfügung.
Dosierung
Die empfohlene Dosierung beträgt einmal täglich abends 1 Tropfen (1,5 µg) in jedes Auge. Kontaktlinsen sollten vor der Verabreichung entfernt und erst 15 Minuten später wieder eingesetzt werden.
Bei der Anwendung kann die systemische Resorption verringert werden, wenn der Tränensack unter dem inneren Augenwinkel nach jeder Instillation eines Tropfens für eine Minute komprimiert wird.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Nebenwirkungen
Die häufigsten unerwünschten Wirkungen von Latanoprost sind:[1]
- Reizwirkung: Brennen, Kratzen, Jucken, Stechen, Fremdkörpergefühl
- Konjunktivale Hyperämie, meist innerhalb von 2 bis 3 Tagen nach der ersten Anwendung beginnend, innerhalb eines Monats nachlassend
- Hyperpigmentation der Iris – irreversible Farbänderung durch erhöhten Melaningehalt von Melanozyten
- Konjunktivitis
- Hornhautödem
- Reaktivierung einer Keratitis herpetica
- Keratitis superficialis punctata
- Iritis
- Makulaödem
- Exanthem
- Lidrandentzündung
Bei dauerhafter Anwendung von Latanoprost kann es zu einer Hypertrichosis der Wimpern kommen. Dabei nehmen Länge, Dicke, Pigmentierung und Anzahl der Wimpern zu. Die Nebenwirkung führte zur Entwicklung von Bimatoprost, das durch die FDA auch zur Förderung des Wimpernwachstums zugelassen wurde.
Nach einer Änderung der Zusammensetzung traten vermehrt Fälle von starker Augenreizung auf, daher wurde Latanoprost von der EMA mit einem Sicherheitssignal versehen.[4]
Therapiekontrolle
Aufgrund der Nebenwirkungen sollten während der gesamten Anwendungsdauer das Auftreten folgender Symptome regelmäßig kontrolliert werden:[1]
- intraokulare Entzündungszeichen
- Veränderungen der Pigmentierung
- Veränderungen der Makula
Eine Augeninnendruckmessung sollte alle 2 bis 4 Wochen erfolgen, bis die gewünschte Drucksenkung erreicht ist, danach nur alle 6 Monate.
Wechselwirkungen
Bei gleichzeitiger Anwendung anderer Antiglaukomatosa kann es zu einer Wirkungsverstärkung kommen. Die gleichzeitige Anwendung von zwei Prostaglandinanaloga am Auge kann paradoxerweise zu einer Erhöhung des IOD führen. Es besteht eine Inkompatibilität mit Thiomersal.
Kontraindikationen
- Überempfindlichkeit gegen den Wirkstoff und sonstige Bestandteile des Arzneimittels
Schwangerschaft und Stillzeit
Bisher gibt es nur geringe Erfahrungen zur Anwendung von Latanoprost in der Schwangerschaft. Die verfügbaren Studienergebnisse sind unzureichend.[5]
1. Trimenon
Bisher (2025) gibt es keine Hinweise auf eine teratogene Wirkung. Systematische Untersuchungen fehlen.
2. und 3. Trimenon
Eine systemische Wirkung von lokal angewendeten Augentropfen ist prinzipiell möglich und kann zur Zunahme des Uterustonus, zur Minderperfusion des Fetus und zum Abort führen.[6]
Zur Zeit (2025) gibt es keine Hinweise auf ein fetotoxisches Risiko bei ordnungsgemäßer topischer Anwendung von prostaglandinhaltigen Augentropfen. Die systemische Resorption kann wie unter "Dosierung" beschrieben verringert werden. Als besser geeignete Alternative wird die Anwendung von Timolol empfohlen.[5]
Stillzeit
Systematische Untersuchungen zur Anwendung in der Stillzeit liegen nicht vor. Über Symptome bei gestillten Säuglingen wurde bisher nicht berichtet. Indikationsgerechte Anwendung wie oben beschrieben.[5]
Toxizität
Es gibt bisher keine Hinweise auf kanzerogene, mutagene oder reproduktionstoxische Wirkungen. In vitro lassen sich Chromosomenaberrationen an menschlichen Lymphozyten nachweisen.[1]
Die i.v.-Infusion von 3 µg/kgKG, bei der 200-fach höhere Plasmaspiegel als bei topischer Applikation auftreten, löste bei gesunden Probanden keine Nebenwirkungen aus. Nach i.v.-Infusion von 5,5 bis 10 µg/kgKG traten Müdigkeit, Schwitzen, Schwindel, Übelkeit und Bauchschmerzen auf.[1]
Es besteht zur Zeit (2025) keine Evidenz für einen Zusammenhang zwischen der Verabreichung von Latanoprost und Aderhautmelanomen oder Melanomen der Haut.[7]
Labormedizin
Es gibt keine Hinweise auf die Beeinflussung von Laboruntersuchungen durch Latanoprost.
Verschreibungspflicht
Alle Präparate, die Latanoprost enthalten, sind verschreibungspflichtig.
Zulassung
Latanoprost wurde in den 1980er Jahren entwickelt und 1993 patentiert.[8] Es ist seit 1996 in der EU zugelassen.
ATC-Codes
- S01EE01 - Prostaglandinanaloga; Glaukommittel und Miotika
- S01ED61 - Timolol und Latanoprost
- S01EE51 - Latanoprost und Netarsudil
Quellen
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 Tripathy und Geetha, Latanoprost, StatPearls 2022
- ↑ Song W, et al. Neuroprotective therapies for glaucoma. Drug Des Devil Ther 2015;9:1469-79.
- ↑ Diestelhorst, Glaukomtherapie mit Prostaglandin-F2 alpha-Derivaten, Ophthalmologe 1997
- ↑ EMA - PRAC recommendations on signals, abgerufen am 23.05.2023
- ↑ 5,0 5,1 5,2 embryotox.de - Latanoprost, abgerufen am 21.01.2023
- ↑ Sakai et al., Pregnancy Loss Signal from Prostaglandin Eye Drop Use in Pregnancy: A Disproportionality Analysis Using Japanese and US Spontaneous Reporting Databases, Drugs Real World Outcomes. 2022
- ↑ Tressler et al., Lack of evidence for a link between latanoprost use and malignant melanoma: an analysis of safety databases and a review of the literature, Br J Ophthalmol. 2011
- ↑ Stjernschantz, From PGF(2alpha)-isopropyl ester to latanoprost: a review of the development of xalatan: the Proctor Lecture, Invest Ophthalmol Vis Sci. 2001
Literatur
- Mutschler et al., Mutschler Arzneimittelwirkungen: Lehrbuch der Pharmakologie und Toxikologie, Wissenschaftliche Verlagsgesellschaft, 9. Auflage, 2008.
Weblinks
- Latanoprost. Drugbank
- Latanoprost. PharmaWiki
- Latanoprost. Pharmazeutische Zeitung Arzneistoffe
- PubChem: 5311221
- MeSH: D000077338