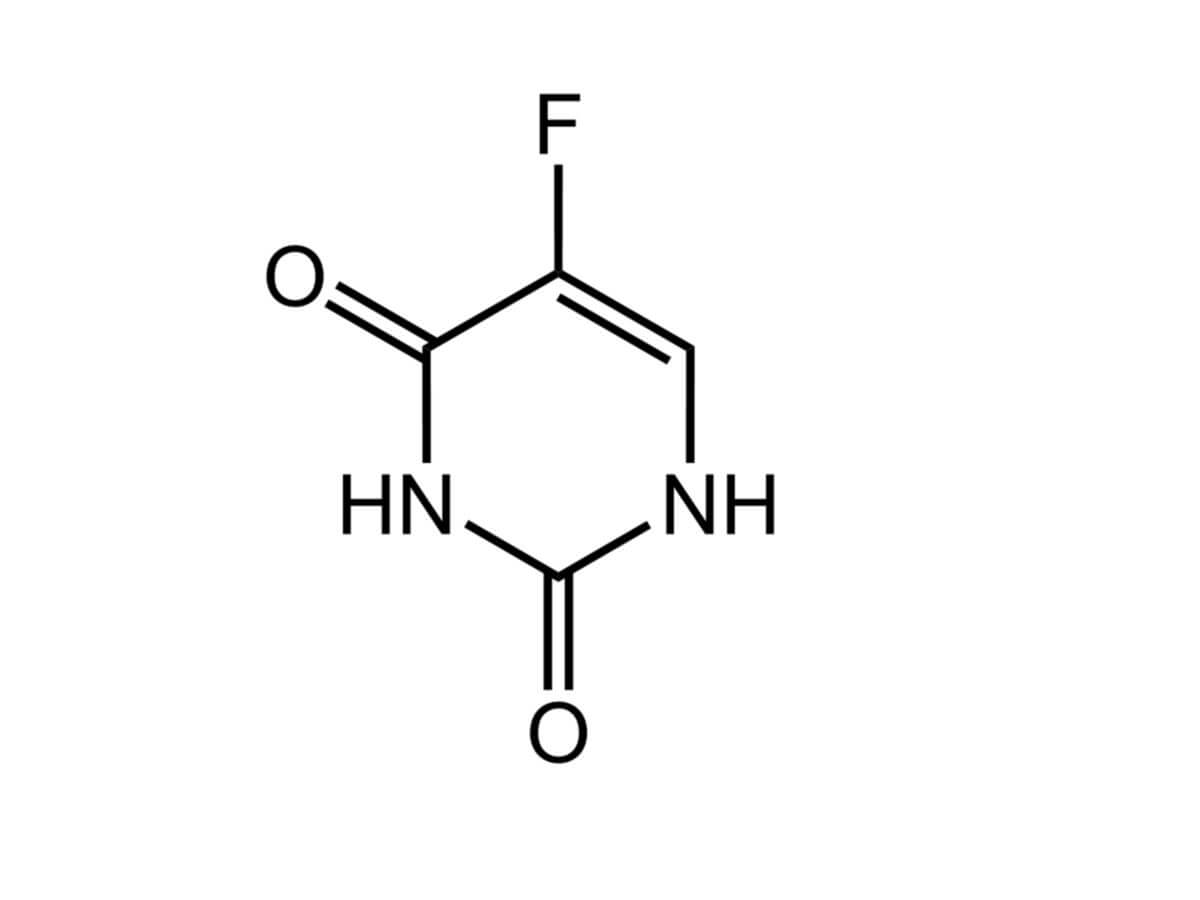
5-Fluorouracil
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsnamen: Actikerall®, Efudix®, Tolak®, Verrucutan®, Verrumal® u.v.a.
Synonyme: Fluorouracilum, 5-FU, 5-Fluoruracil
Englisch: fluorouracil
Definition
5-Fluorouracil, kurz 5-FU, ist ein Arzneistoff aus der Gruppe der Antimetabolite, der vor allem bei der Chemotherapie verschiedener maligner Tumoren eingesetzt wird.
Chemie
5-FU ist ein Pyrimidinanalogon von Thymin (5-Methyluracil). Es handelt sich um ein an Position 5 fluoriertes Uracil und zählt deshalb zu den Fluoropyrimidinen. Die Summenformel ist C4H3FN2O2. Der IUPAC-Name ist
- 5-Fluoro-1H-pyrimidin-2,4-dion
Die molare Masse beträgt 130,1 g/mol, der Oktanol-Wasser-Koeffizient (logP) -0,58. Die CAS-Nummer lautet 51-21-8. Die Substanz liegt bei Raumtemperatur als weißes, kristallines Pulver vor, das in Wasser wenig löslich ist.
Wirkmechanismus
5-FU zählt als Pyrimidinanalogon zur Gruppe der Antimetabolite. Die Wirkform 5-F-UTP wird aufgrund ihrer strukturellen Ähnlichkeit anstelle der Pyrimidinbase Uracil in die RNA eingebaut. Dadurch kommt es zu einer Störung der Transkription und in der Folge zum Abbruch der Proteinsynthese, was zum Zelltod führt.
Für die antiproliferative Wirkung von 5-FU ist darüber hinaus die Hemmung der Thymidylat-Synthase durch 5-F-dUMP von entscheidender Bedeutung. Dadurch wird die Umwandlung von Desoxyuridinmonophosphat (dUMP) in den DNA-Baustein Desoxythymidinmonophosphat (dTMP) blockiert, was zur Störung der DNA-Replikation führt und damit vor allem die Zellteilung von Zellen mit hoher Replikationsrate blockiert.
Folinsäure (Leucovorin) verstärkt als Co-Substrat die Hemmung der Thymidilat-Synthase, sodass bei gleichzeitiger Anwendung die zytotoxische Wirkung von 5-FU verstärkt wird (z.B. im FOLFOX- oder FOLFIRI-Schema).[1]
Cave: Während Natriumfolinat zusammen mit 5-FU infundiert werden kann, müssen Calciumfolinat und 5-FU getrennt verabreicht werden, um eine intravasale Präzipitation von Calciumcarbonat zu vermeiden.
Pharmakokinetik
5-FU wird nach oraler Aufnahme sehr variabel resorbiert. Aufgrund eines First-Pass-Effekts, der durch die hepatische Aktivität der Dihydropyrimidin-Dehydrogenase (DPD) bestimmt wird, schwankt die orale Bioverfügbarkeit zwischen 0 und 80 %. Nach dermaler Applikation werden ca. 6 % resorbiert. Um eine sichere Dosierung zu gewährleisten, wird 5-FU als intravenöser Bolus verabreicht. Die Plasmaproteinbindung beträgt 8 - 12 %. Die Verteilung erfolgt in alle Gewebe und Organe des Körpers.
Die Aufnahme von 5-FU in die Zellen erfolgt über den Transporter für Uracil. Intrazellulär wird 5-FU durch die Uracil-Phosphoribosyl-Transferase (UPRTase) zu 5-Fluor-Uridinmonophosphat (5-F-UMP) umgewandelt. Im nächsten Schritt konvertiert die Ribonukleotidreduktase 5-F-UMP in 5-Fluor-Desoxyuridinmonophosphat (5-F-dUMP). Außerdem werden auch 5-Fluor-Uridintriphosphat (5-F-UTP) und 5-Fluor-Deoxyuridintriphosphat (5-F-dUTP) gebildet. 5-FU wird zu 80 % durch DPD zum inaktiven Dihydrofluorouracil (DHFU) biotransformiert, das renal eliminiert wird. Nur 5 bis 20 % der Dosis werden innerhalb von 6 Stunden unverändert mit dem Urin ausgeschieden, davon über 90 % innerhalb der ersten Stunde. Die Eliminationshalbwertszeit beträgt initial 10 bis 20 Minuten, terminal 20 Stunden.[1]
Indikationen
5-FU wird allein oder in Kombination mit anderen Wirkstoffen bei einer Vielzahl von Tumorerkrankungen eingesetzt, u.a. bei:
- malignen Tumoren des Magen-Darm-Trakts
- malignen Tumoren des Kopf- und Halsbereichs
- Mammakarzinom
Neben diesen Indikationen wird 5-FU – oft in Kombination mit Salicylsäure – zur Behandlung von Warzen und aktinischen Keratosen sowie bei bestimmten Formen des Basalzellkarzinoms eingesetzt.
Darreichungsform
5-FU ist als Injektionslösung zur intravenösen Anwendung sowie als Lösung oder Creme zur dermalen Applikation erhältlich.
Dosierung
Die intravenöse Anwendung erfolgt als Mono- oder Kombinationstherapie in Dosierungen von 300 bis 600 mg/m² KOF pro Tag unverdünnt als langsame Bolusinjektion oder verdünnt als Dauerinfusion über 24 Stunden. Die Tageshöchstdosis sollte 1.000 mg nicht überschreiten. In Kombination mit Folinsäure wird die Dosierung reduziert.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Zur dermalen Anwendung werden 0,5 bis 5 %ige Zubereitungen appliziert.
Nebenwirkungen
Wie bei anderen Zytostatika kommt es auch unter der Therapie mit 5-FU zu teilweise erheblichen Nebenwirkungen, die dosislimitierend sein können. Hierzu zählen u.a.:
- Gastrointestinale Nebenwirkungen
- Blutbildendes System
- Hand-Fuß-Syndrom
Das Ausmaß der Nebenwirkungen (Toxizität) von 5-FU hängt unter anderem von der DPD-Aktivität ab. Bei einer Dihydropyrimidin-Dehydrogenase-Defizienz (DPD-Insuffizienz) ist die Toxizität deutlich erhöht.
Wechselwirkungen
Bei der Gabe von 5-FU kann es zu Wechselwirkungen mit anderen Arzneimitteln kommen. Schwere Nebenwirkungen sind bei gleichzeitiger Einnahme des Virostatikums Brivudin (Zostex®) bekannt. Diese Wechselwirkung betrifft auch die 5-FU-Prodrugs Capecitabin und Tegafur. Brivudin bewirkt eine irreversible Hemmung der DPD, sodass 5-Fluoropyrimidine nicht mehr abgebaut werden können. Daher muss nach der Therapie mit Brivudin ein Sicherheitsabstand von 4 Wochen eingehalten werden, bevor 5-Fluoropyrimidine eingesetzt werden dürfen. Außerdem wird die Bestimmung der Enzymaktivität der DPD vor Beginn der Behandlung empfohlen.[2]
Kontraindikationen
- Überempfindlichkeit gegen 5-FU oder einen der sonstigen Bestandteile des Arzneimittels
- Myelosuppression
- schwere Blutbildveränderungen
- schwere Leberfunktionsstörungen
- schwere Infektionen
- gleichzeitige Anwendung von Brivudin
- Schwangerschaft und Stillzeit
- vollständiger DPD-Mangel
Labormedizin
Aufgrund von Mutationen im kodierenden Gen haben bis zu 9 % der kaukasischen Bevölkerung eine niedrige DPD-Aktivität. Bei bis zu 0,5 % fehlt die Enzymaktivität vollständig, sodass die Gefahr lebensbedrohlicher und tödlicher Nebenwirkungen besteht. Die Therapie-assoziierte Letalität liegt bei 0,2-1,0 %.[3]
Es wird empfohlen, vor Beginn einer Behandlung mit 5-Fluoropyrimidinen den Phänotyp und/oder Genotyp zu bestimmen. Bei niedriger DPD-Aktivität sollte die initiale Dosis auf mindestens 50 % reduziert werden. Patienten, die keine DPD-Aktivität aufweisen, dürfen nicht mit 5-FU oder anderen Fluoropyrimidinen behandelt werden.[4]
Die Untersuchung der DPD-Aktivität im Zusammenhang mit der Verabreichung von 5-Fluoropyrimidin-haltigen Arzneimitteln ist seit dem 01.10.2020 als Kassenleistung über eine EBM-Ziffer abrechenbar.
Bestimmung des DPD-Phänotyps
Folgende Untersuchungen können zur Identifizierung des Phänotyps von Patienten mit einem DPD-Mangel eingesetzt werden:[3]
- Bestimmung von Uracil im Plasma
Ein Uracil-Blutspiegel ≥ 16 ng/ml und < 150 ng/ml weist auf einen partiellen DPD-Mangel hin. Ein Uracil-Blutspiegel ≥ 150 ng/ml gilt als Indikator für einen vollständigen Mangel an DPD-Aktivität.[4]
Bei Patienten mit mittelschwerer oder schwerer Nierenfunktionsstörung können erhöhte Uracil-Spiegel auftreten, ohne dass ein DPD-Mangel vorliegt. Eine Fehlinterpretation des Messergebnisses kann zur Unterdosierung führen.[5]
Weitere Testmöglichkeiten sind:[3]
- Bestimmung der DPD- und der TS-Aktivität in mononukleären Zellen
- Bestimmung des physiologischen Verhältnisses von Dihydrouracil/Uracil (UH2/U) in Blut, Urin oder Speichel
- Bestimmung von UH2/U nach Verabreichung einer Testdosis Uracil
Bestimmung des DPD-Genotyps
Das Enzym wird durch das Dihydropyrimidin-Dehydrogenase-Gen (DPYD-Gen) kodiert. Es existieren mehrere Genotypen, deren Expression für Unterschiede in der DPD-Enzymaktivität verantwortlich ist und mit einem erhöhten Risiko für schwere toxische Wirkungen in Verbindung gebracht wird. Bei der Genotypisierung werden die 4 wichtigsten DPYD-Varianten (c.1905+1G>A oder Exon 14-Skipping-Mutation [DPYD*2A], c.1679T>G [DPYD*13], c.1236G>A bzw. c.1129-5923C>G [HapB3] und c.2846A>T im Exon 22) mittels PCR und Kapillarelektrophorese untersucht.[3]
ATC-Code
- L01BC02 - Antineoplastische und immunmodulierende Mittel - Antineoplastische Mittel - Antimetabolite - Pyrimidin-Analoga
- D11AF05 - Andere Dermatika - Warzenmittel und Keratolytika
Quellen
- ↑ 1,0 1,1 Freissmuth M, Offermanns S, Böhm S. Pharmakologie und Toxikologie. 3. Aufl., Berlin, Germany : Springer 2020
- ↑ Wechselwirkungen zwischen Brivudin und 5-Fluoropyrimidinen. Rote Hand Brief 27.08.2012, abgerufen am 24.10.2024
- ↑ 3,0 3,1 3,2 3,3 Dihydropyrimidin-Dehydrogenase (DPD) -Testung vor Einsatz von 5-Fluorouracil, Capecitabin und Tegafur. Positionspapier der Deutschen Gesellschaft für Hämatologie und Medizinische Onkologie, Stand Juni 2020, abgerufen am 24.10.2024
- ↑ 4,0 4,1 5-Fluorouracil - Tests vor Behandlungsbeginn. Rote Hand Brief 04.06.2020, abgerufen am 24.10.2024
- ↑ 5-Fluorouracil bei Patienten mit mittelschwerer oder schwerer Nierenfunktionsstörung. Rote Hand Brief 24.10.2024, abgerufen 24.10.2024
Weblinks
- Drugbank - Fluorouracil, abgerufen am 24.10.2024
- Gelbe Liste Wirkstoffe - Fluorouracil, abgerufen am 24.10.2024
- PharmaWiki - 5-Fluorouracil, abgerufen am 24.10.2024
- PubChem 3385
- MeSH 68005472