Herpesviridae
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: Herpesviren
Englisch: herpes viruses
Definition
Als Herpesviridae bzw. Herpesviren wird eine mehr als 130 Arten umfassende Familie von DNA-Viren in der Ordnung Herpesvirales bezeichnet. Trotz enger struktureller Gemeinsamkeiten rufen sie äußerst unterschiedliche Erkrankungen hervor.
Taxonomie
- Bereich: Duplodnaviria
- Reich: Heunggongvirae
- Stamm: Peploviricota
- Klasse: Herviviricetes
- Ordnung: Herpesvirales
- Familie: Herpesviridae
- Ordnung: Herpesvirales
- Klasse: Herviviricetes
- Stamm: Peploviricota
- Reich: Heunggongvirae
Die Familie Herpesviridae umfasst derzeit (2021) drei Unterfamilien mit jeweils mehreren human- sowie tierpathogenen Gattungen.
| Unterfamilie | Gattung | Art |
|---|---|---|
| Alphaherpesvirinae | Simplexvirus |
|
| Varicellovirus |
| |
| Betaherpesvirinae | Cytomegalovirus |
|
| Roseolovirus |
| |
| Gammaherpesvirinae | Lymphocryptovirus |
|
| Rhadinovirus |
|
siehe Hauptartikel: Virustaxonomie
Eigenschaften
Morphologie
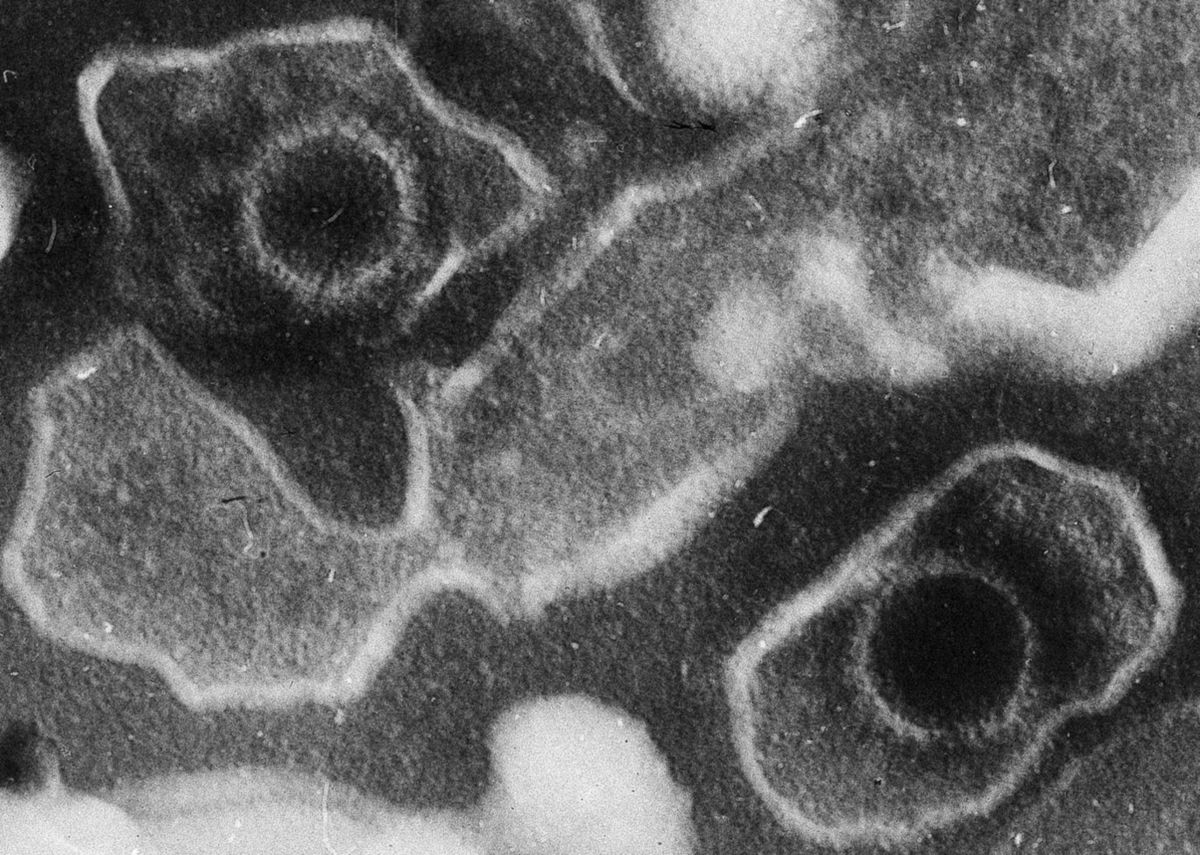
Herpesviren haben ein Durchmesser von etwa 120 bis 200 nm. Unter dem Elektronenmikroskop sieht man meist eine unregelmäßige, eingedellte Virushülle, die als Artefakt durch die Präparation auftritt. Das ca. 100 nm große Kapsid ist ikosaedrisch geformt. Zwischen Virushülle und Kapsid befindet sich ein relativ großer Matrixraum (Tegument), der mit zahlreichen Strukturproteinen angefüllt ist.
Genom
Die lineare Doppelstrang-DNA der Herpesviren ist mit ca. 125 bis 235 kbp sehr groß. In der Latenzphase werden nur wenige Gene exprimiert. Während der lytischen Phase unterscheidet man Sofortproteine, Frühproteine und Spätproteine.
Lebenszyklus
Eine Infektion mit Herpesviren beginnt mit der Interaktion des Viruspartikels mit spezifischen Rezeptormolekülen auf der Zelloberfläche der Wirtszelle. Nach der Bindung der Glykoproteine der Virushülle an seine Membranrezeptoren wird das Virion internalisiert und das Kapsid im Zytoplasma aufgelöst. Die freigesetzte DNA wird in den Zellkern verlagert.
Alle Herpesviren vermehren sich im Zellkern. Die virale DNA wird dort repliziert und in mRNA umgeschrieben, welche die Produktion neuer Viren durch die Proteinmaschinerie der Zelle in Gang setzt.
Im Rahmen symptomatischer Infektionen vermehren sich rasch neue Viruspartikel in den infizierten Zellen, die schließlich unter Einwirkung lytischer Virusenzyme die Zelle auflösen und die Viren freisetzen. In anderen Zellen werden stattdessen Virusgene produziert, die man als Latency-Associated Transcript (LAT bzw. HHV LAT) bezeichnet. Sie führen zu einer latenten, symptomfreien Infektion, die es dem Virus ermöglicht, nahezu unbegrenzt in der Zelle zu persistieren.
Die Reaktivierung dieser latenten Infektion ist z.B. für den Herpes zoster verantwortlich, der Jahre bis Jahrzehnte nach einer HHV-3-Primärinfektion ausbrechen kann.
Resistenz
Herpesviren sind relativ stabil, reagieren jedoch empfindlich gegen Lipidlösungsmittel.
Klinik
Alphaherpesviren
Alphaherpesviren zeichnen sich durch ein breites Wirtszellpektrum und eine schnelle Replikation aus. Sie persistieren in Ganglienzellen und verursachen folgende Krankheitsbilder:
- HHV-1, HHV-2 (HSV-1, -2):
- HHV-3 (VZV):
- Windpocken
- Gürtelrose
- Pneumonien
- Embryofetopathien (konnatales Varizellensyndrom)
- Suides Herpesvirus 1: Aujeszky-Krankheit beim Schwein
Betaherpesvirinae
Betaherpesviren haben ein enges Wirtszellspektrum und replizieren langsam. Sie führen zur Bildung von Riesenzellen.
- HHV-5 (CMV):
- mononukleoseähnliches Syndrom
- Embryofetopathien (konnatale CMV-Infektion)
- bei Immunsuppression auch Hepatitis, Pneumonie, Meningoenzephalitis, Ösophagitis, Retinitis
- HHV-6 und HHV-7:
- Dreitagefieber (Exanthema subitum)
- mononukleoseähnliche Krankheitsbilder
- selten Pneumonie, Hepatitis, Meningoenzephalitis etc.
- evtl. Pityriasis rosea
Gammaherpesvirinae
Gammaherpesviren haben ein sehr enges Wirtszellspektrum. Ihre Replikation verläuft langsam. Sie persistieren in B-Lymphozyten und sind potentielle Onkoviren.
- HHV-4 (EBV):
- HHV-8 (KSHV):
- Kaposi-Sarkom
- KSHV-assoziierte Lymphome
Literatur
- Susanne Modrow, Dietrich Falke, Uwe Truyen, Hermann Schätzl (2010): Molekulare Virologie. 3. Auflage, Spektrum