Schistosoma mansoni
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
Loslegennach dem schottischen Arzt Sir Patrick Manson (1844-1922)
von griechisch: σχιστος ("schistos") - gespalten und σῶμα ("soma") - Körper
Synonym: Pärchenegel
Englisch: Schistosoma mansoni
Definition
Schistosoma mansoni ist ein klinisch bedeutsamer, zu den Schistosomen gehörender Parasit aus der Klasse der Saugwürmer, der die Darmbilharziose verursacht. Der ursprüngliche Name der Gattung (Bilharzia), ist heutzutage nur wenig gebräuchlich.
Morphologie
Schistosoma mansoni gehört zu den getrennt-geschlechtlichen Trematoden. Je ein Männchen und ein Weibchen leben ständig zusammen, wobei das Männchen durch Zusammenrollen seines blattartigen Körpers eine Röhre bildet, in der das Weibchen liegt (Pärchenegel). Schistosomen sind 6 - 22 mm lang und ihre Lebensspanne beträgt bis zu 30 Jahre. Ihre Eier besitzen einen kleinen, lateralen Stachel.
siehe auch: Schistosoma - Morphologie
Vorkommen
Schistosoma mansoni ist in Teilen von Afrika und Südamerika sowie in Arabien und Westindien zu finden.
Genetik
Schistosoma mansoni besitzt 8 Chromosomenpaare, die sich aus 7 Autosomen und einem Geschlechtschromosom zusammensetzen. Weibliche Schistosomen sind heterogametisch (ZW), männliche Schistosomen homogametisch (ZZ).
Das Genom umfasst etwa 270 Megabasenpaare, wobei es sich zu etwa 30% um repetitive DNA handelt. Grob geschätzt werden 15.000-20.000 Gene exprimiert.
Pathogenese
Die adulten Würmer (Männchen und Weibchen) leben paarweise in der Blutbahn ihres Endwirtes Mensch. Es werden täglich Hunderte bis Tausende von Eiern in den jeweiligen Blutgefäßen, insbesondere den Mesenterialvenen, abgelegt. Von der in der Eihülle liegenden Larve wird ein Enzym ausgeschieden, das den Eiern die Penetration durch die Gefäßwand in das Blasen- oder Darmlumen ermöglicht.
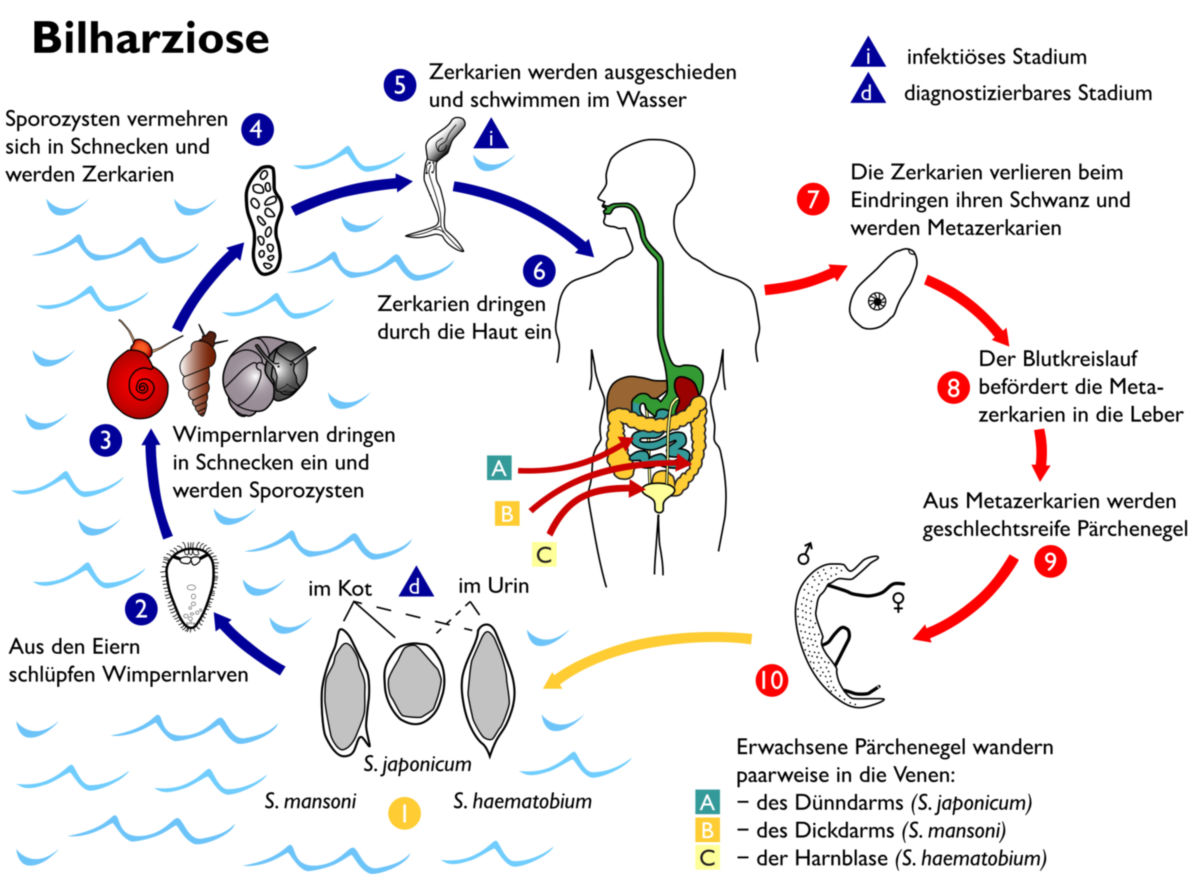
Mit dem Stuhl oder Urin gelangen die Eier schließlich in die freie Natur. In Süßwasser schlüpfen die Larven (Mirazidien), die dann aktiv mithilfe von zahlreichen Zilien ihre Zwischenwirte, bestimmte Wasserschnecken, aufsuchen und in sie eindringen. In der Schnecke reifen die Larven zu Zerkarien heran und verlassen diese wieder durch die Atemöffnung. Im Süßwasser bohren sich die Zerkarien durch die Haut des Endwirtes Mensch und gelangen über die Hautvenen in den Körperkreislauf und schließlich in das Pfortadersystem, wo sie sich an der Gefäßwand festsaugen, heranwachsen und sich als Paar etablieren. Erst nach der geschlechtlichen Paarung wandern die Weibchen in die Mesenterial- bzw. Blasengefäße, um ihre Eier abzulegen. Die Krankheitserscheinungen entstehen durch entzündliche Reaktionen auf die Eier.
Lebenszyklus
Endwirt Mensch: adulter Wurm → Ei → Süßwasser: Mirazidium → Zwischenwirt Wasserschnecke: Zerkarien → Endwirt Mensch: adulter Wurm
Immunevasion
Schistosoma mansoni besitzt mehrere Mechanismen, um der Immunantwort des Wirts zu entgehen (Immunevasion):
- Tegument: Das Tegument umhüllt den Wurm und bildet eine physikalische Barriere gegenüber Antikörpern und dem Komplementsystem.
- Antioxidative Proteine: Schistosoma mansoni produziert verschiedene Superoxiddismutasen, um das vom Wirt gebildete Wasserstoffsuperoxid zu neutralisieren. Diese Superoxiddismutasen sind ein möglicher Angriffspunkt für eine pharmakologische Therapie.
- Verteidigung gegen den Membranangriffskomplex (MAK): Der Erreger hat Mechansimen entwickelt, um das Komplementsystem zu blockieren. Auf dem Tegument befindet sich u.a. ein Homolog des menschlichen Oberflächenantigens CD59, das den MAK hemmt.
Klinik
Zerkariendermatitis
Die ersten klinischen Erscheinungen entstehen beim Eindringen der Zerkarien in die Haut. Symptome sind Juckreiz, Hautrötung und Pusteln.
Eine Schistosomatiden-Dermatitis kann auch durch normalerweise nicht humanpathogene Larven der Gattung Trichobilharzia ausgelöst werden. Er tritt vor allem in subtropischen Gebieten als unangenehmer Ausschlag auf.
Katayama-Syndrom
Die Etablierung der adulten Würmer ist anfangs mit akuten Entzündungserscheinungen verbunden: nach einer Inkubationszeit von 2 - 10 Wochen kann ein Katayama-Syndrom auftreten mit Symptomen wie Fieber, generalisierter Urtikaria, Hepatosplenomegalie sowie Eosinophilie.
Darmbilharziose
Die Symptome der eigentlichen Darmbilharziose werden nach einer Inkubationszeit von mehr als 2 Monaten vor allem durch die in der Darmwand oder in der Leber liegenden Eier hervorgerufen. Die Eier induzieren einen intensiven granulomartigen Gewebsumbau in ihrer Umgebung. In der Folge kommt es zu fibrotischen Veränderungen wie Pseudopolypen der Darmschleimhaut und Leberzirrhose.
Diagnostik
Direkter Nachweis
Bei Verdacht auf einen Befall mit Schistosoma mansoni ist der Nachweis der Eier im Stuhl oder Urin des Patienten beweisend. Die Eier haben eine Größe von 130 x 60 μm und einen seitlichen Stachel. Zusätzlich kann ein Mirazidien-Schlüpfversuch im Stuhlsediment durchgeführt werden.
Indirekter Nachweis
Bei fortgeschrittenen Erkrankungen können auch serologische Verfahren eingesetzt werden. Dazu wird 1 ml Serum benötigt.
Referenzbereich
| Testverfahren | Referenzwert |
|---|---|
| Schistosoma-mansoni-IgG-ELISA | negativ |
| Indirekte Immunfluoreszenz | negativ |
| Indirekter Hämagglutinationstest (IHT) | ≤ 1:16 |
| Allergenspezifische IgE-Antikörper | 0,00 bis 0,34 kU/l |
Weitere Laborparameter
Im Rahmen eines Schistosoma-Befalls lassen sich im Blutbild eine Eosinophilie sowie eine Erhöhung des Gesamt-IgE nachweisen. In 50% der Fälle ist das Alpha-1-Fetoprotein ebenfalls erhöht.
Therapie
Zur Therapie wird Praziquantel angewandt.
Prophylaxe
Als effektive Prophylaxe dient die strikte Trinkwasserhygiene sowie das Vermeiden von direktem Hautkontakt mit Gewässern in den betroffenen Gebieten.
Literatur
- Herbert Hof und Rüdiger Dörries et al.: Duale Reihe Medizinische Mikrobiologie, Thieme
- Uwe Groß: Kurzlehrbuch Medizinische Mikrobiologie und Infektiologie, Thieme, 2. Auflage
- Laborlexikon.de; abgerufen am 28.04.2021