Ketonkörper
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: Ketokörper
Englisch: ketone bodies
Definition
Zu den so genannten Ketonkörpern gehören die chemischen Verbindungen Acetoacetat, Aceton und Beta-Hydroxybutyrat. Letzteres wird zu den Ketonkörpern gerechnet, obwohl es chemisch gesehen eine Hydroxycarbonsäure ist.
Physiologie
Ketonkörper entstehen bei absolutem oder relativem Kohlenhydratmangel als Nebenprodukt der Fettverbrennung in den Mitochondrien der Leberzellen (Hepatozyten) - zum Beispiel bei Hungerzuständen. Für den Gehirnstoffwechsel ist die Bildung von Ketonkörpern dabei essentiell, da sie neben Glucose und Laktat die einzige Energiequelle darstellen.
Ein weiterer Grund ist eine verminderte Aufnahme von Glucose im Rahmen eines Diabetes mellitus. Der Glukosespiegel im Blut ist dabei nicht unbedingt vermindert. Bei Insulinmangel ist die Glucosekonzentration hoch, das Kohlenhydrat kann aber nicht in die Zellen aufgenommen und verwertet werden ("relativer Glucosemangel").
Im Rahmen einer ketogenen Diät wird durch kohlenhydratarme Ernährung gezielt die Bildung von Ketonkörpern induziert.
Synthese (Ketogenese)
Die Synthese von Ketonkörpern bezeichnet man als Ketogenese. Bei Kohlenhydratmangel werden vermehrt Fettsäuren über die beta-Oxidation zu Acetyl-CoA abgebaut. Gleichzeitig entsteht ein Mangel an Oxalacetat, an das Acetyl-CoA normalerweise im Citratzyklus gebunden wird. In der Folge akkumuliert Acetyl-CoA in den Hepatozyten. Dieses dient als Substrat für die Synthese von Ketonkörpern, die im Matrixraum von Mitochondrien abläuft.
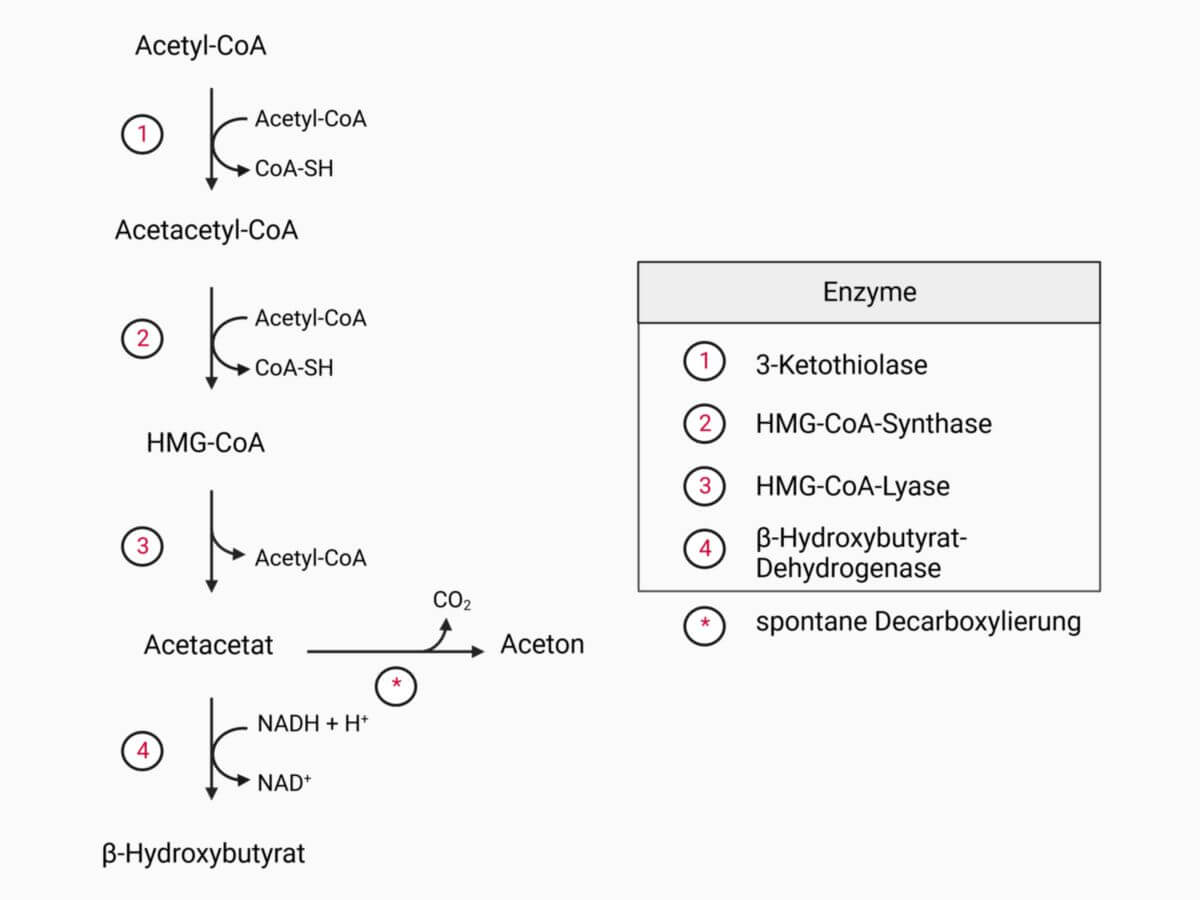
- Zunächst werden durch die 3-Ketothiolase zwei Moleküle Acetyl-CoA zu Acetoacetyl-CoA kondensiert.
- Es folgt die Anlagerung eines weiteren Acetyl-CoA durch das Enzym HMG-CoA-Synthase, wobei beta-Hydroxy-beta-Methylglutaryl-CoA (HMG-CoA) entsteht.
- HMG-CoA wird dann durch die HMG-CoA-Lyase zu Acetyl-CoA und Acetoacetat gespalten.
- In Summe entstehen somit aus 2 Molekülen Acetyl-CoA 1 Molekül Acetoacetat.
- Aus Acetoacetat entstehen schließlich die übrigen beiden Ketonkörper. Zunächst kann es mit NADH durch die beta-Hydroxybutyrat-Dehydrogenase zu beta-Hydroxybutyrat reduziert werden. Bei länger andauernder Nahrungskarenz oder beim Coma diabeticum erfolgt ebenfalls in großem Maße die spontane Decarboxylierung des Acetoacetats zu Aceton. Dies kann gelegentlich in der Ausatemluft nachgewiesen werden.
Regulation der Synthese
Die Synthese wird durch drei Enzyme reguliert.
Hormonsensitive Lipase
Durch die phosphorylierte hormonsensitive Lipase (HSL) werden Triacylglycerine zu Fettsäuren hydrolysiert und diese anschließend in der beta-Oxidation abgebaut. Dies führt zu einer erhöhten Konzentration an Acetyl-CoA. Die HSL wird maßgeblich von Adrenalin und Insulin reguliert. Adrenalin aktiviert die HSL im Rahmen der Lipolyse. Durch Insulin kommt es zu einer Dephosphorylierung und damit Inaktivierung des Enzyms.
Acetyl-CoA-Carboxylase
Durch die Acetyl-CoA-Carboxylase wird Acetyl-CoA in Malonyl-CoA umgewandelt. Dieses bewirkt, dass weniger Acyl-CoA, das Substrat der beta-Oxidation, in die Mitochondrien transportiert wird. Insulin stimuliert dieses Enzym.
HMG-CoA-Synthase
Insulin hemmt das Enzym, während es durch Nahrungskarenz und sehr fettreiche Nahrung aktiviert wird.
Abbau von Ketonkörpern
Die Leber gibt Ketonkörper an das Blut ab, da sie diese nicht metabolisieren kann. Sie dienen zahlreichen extrahepatischen Geweben (insbesondere dem ZNS) als Energielieferant. Um in den oxidativen Stoffwechsel eingeschleust zu werden, müssen sie jedoch zunächst aktiviert werden:
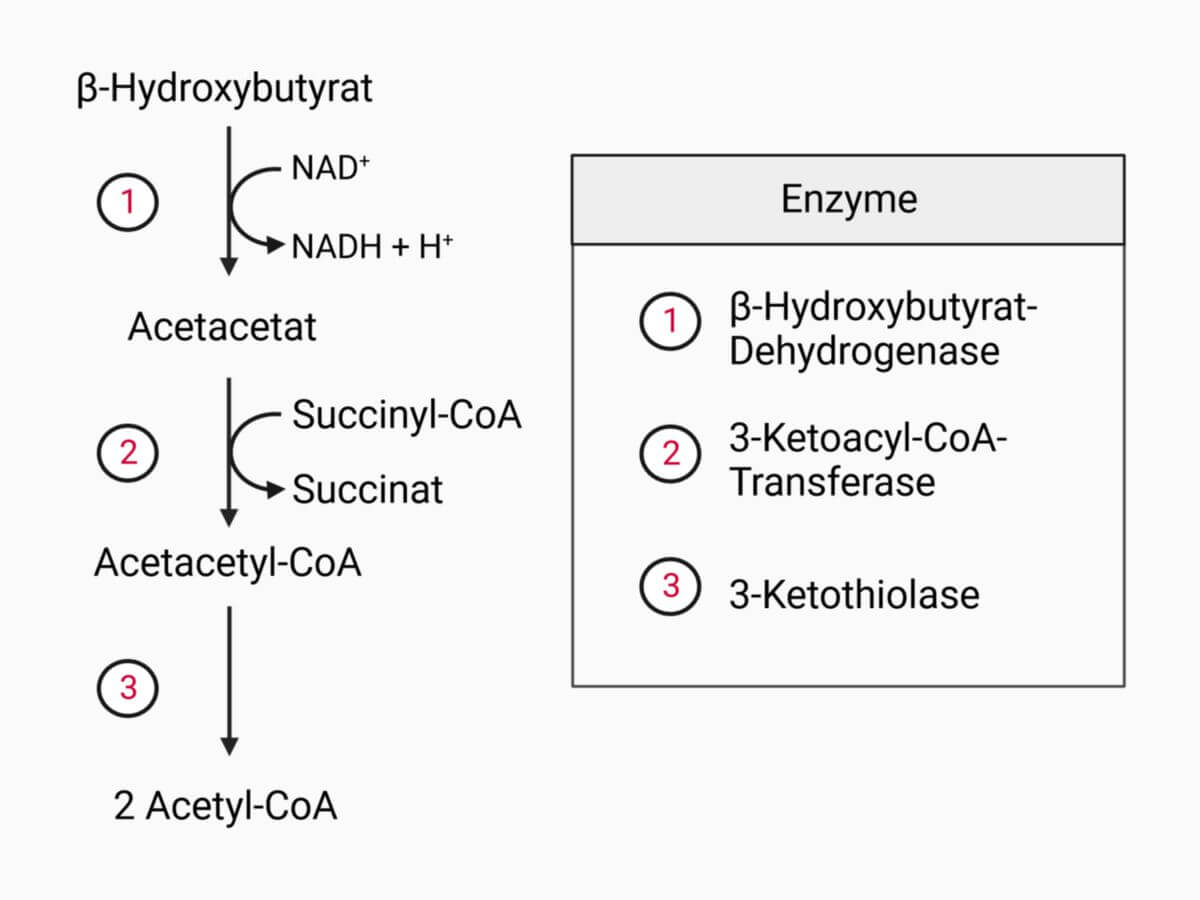
- Zu Beginn wird beta-Hydroxybutyrat zu Acetoacetat oxidiert.
- Es folgt die Reaktion von Acetoacetat mit Succinyl-CoA, wobei Acetoacetyl-CoA und Succinat entstehen.
- Nachdem das Acetoacetyl-CoA durch die 3-Ketothiolase zu Acetyl-CoA gespalten worden ist, kann es als Acetyl-CoA in den Citratzyklus eingeschleust werden.
Diabetische Ketoazidose
Die diabetische Ketoazidose tritt vor allem bei Patienten mit Diabetes mellitus Typ 1 auf und resultiert aus einem ausgeprägten Insulinmangel sowie erhöhten Konzentrationen an Glucagon, Cortisol und Katecholaminen.
Dies bewirkt u.a. eine Aktivierung der hormonsensitiven Lipase und damit eine Hydrolyse von Triacylglycerinen, die wiederum die Konzentrationen an freien Fettsäuren erhöht. Dies führt schließlich zu einer erhöhten Konzentration an Acetyl-CoA, aus dem vermehrt Ketonkörper synthetisiert werden. Es kommt zu einer Senkung des pH-Wertes des Blutes (metabolische Azidose), da Acetoacetat und beta-Hydroxybutyrat dissoziieren. Aceton wird dagegen über die Lunge abgeatmet.
Nachweismethoden
Höhere Spiegel an Ketonkörpern fallen durch den charakteristischen Aceton-Geruch der abgeatmeten Atemluft auf. Laborchemisch können Ketonkörper mit Teststreifen semiquantitativ in Blut und Urin (Ketonurie) nachgewiesen werden (Legal'sche Probe, Nitroprussid-Methode). Diese reagieren nur mit Acetoacetat und Aceton, aber nicht mit beta-Hydroxybutyrat.
Blutzuckermessgeräte, die im Rahmen der patientennahen Sofortdiagnostik (POCT) eingesetzt werden, bieten teilweise auch die Möglichkeit, mit speziellen Sensoren Ketone zu messen.