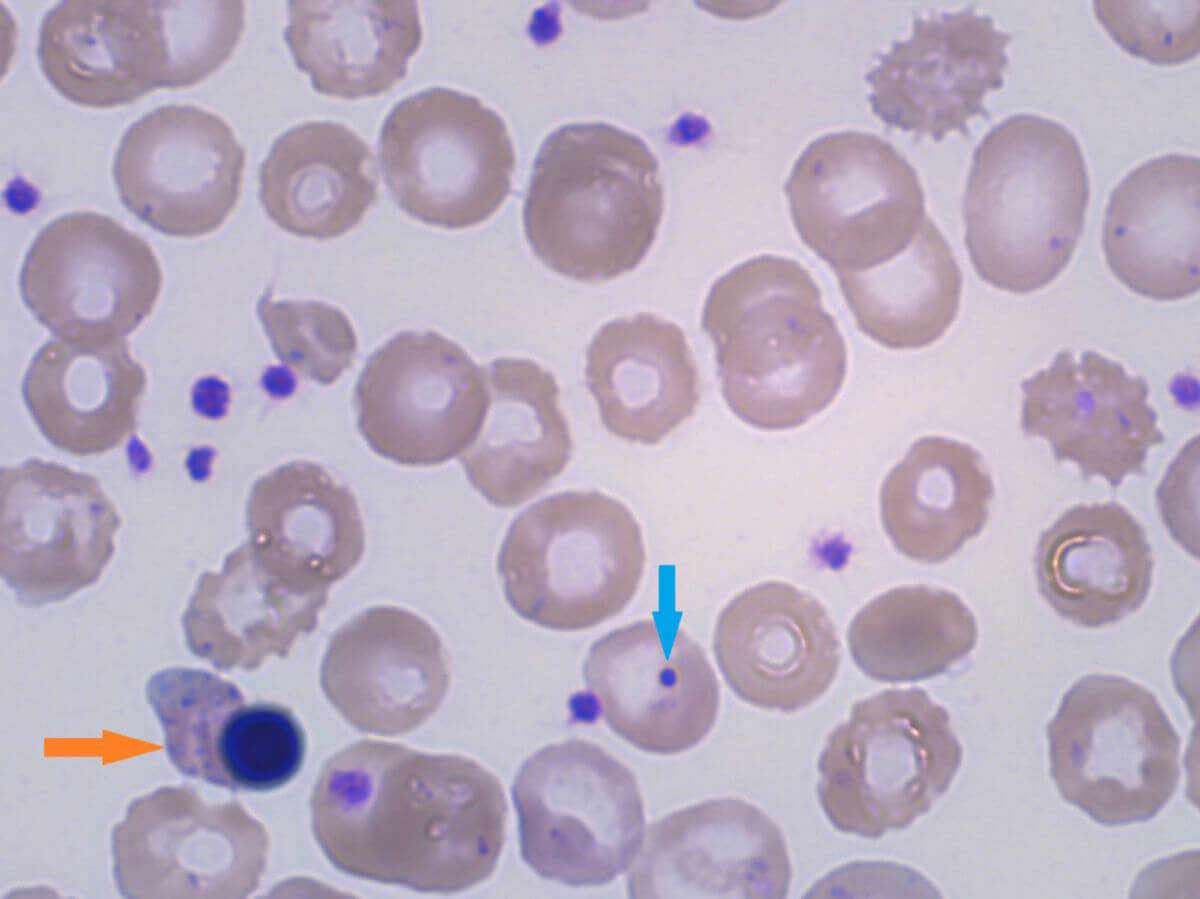
Pyruvatkinase-Mangel
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonyme: PK-Mangel, Pyruvatkinasemangel
Englisch: pyruvate kinase deficiency, PKD
Definition
Der Pyruvatkinase-Mangel ist eine autosomal-rezessiv vererbte Stoffwechselstörung der Glykolyse, die insbesondere den Energiestoffwechsel der Erythrozyten beeinträchtigt und zu einer chronischen hämolytischen Anämie führen kann.
Epidemiologie
Der Pyruvatkinasemangel ist mit einer geschätzten Prävalenz von 1/10.000 Einwohnern eine seltene Erkrankung, jedoch der häufigste Defekt des Glykolysestoffwechsels.[1] In einigen afrikanischen Populationen liegt die polymorphe PKLR-Mutation E277K mit einer Heterozygotenfrequenz von 1 bis 7 % vor. Dabei handelt es sich vermutlich um einen Selektionsvorteil aufgrund einer damit einhergehenden relativen Malaria-Resistenz. Eine erhöhte Erkrankungshäufigkeit findet sich darüber hinaus in Sub-Sahara-Afrika sowie im Mittleren Osten, vermutlich begünstigt durch Gründereffekte in isolierten Populationen.[1]
Ätiologie
Der Pyruvatkinase-Mangel entsteht durch Mutationen im PKLR-Gen auf Chromosom 1 (Genlokus 1q22). Die von dem Gen kodierte Pyruvatkinase katalysiert den letzten Schritt der Glykolyse, die Übertragung eines Phosphatrestes von Phosphoenolpyruvat auf ADP. Bislang (2026) sind über 350 pathogene Varianten bekannt, überwiegend Missense-Mutationen. Seltener finden sich disruptive Varianten wie Frameshift-Mutationen, vorzeitige Stopp-Codons oder größere Deletionen. Sie sind in der Regel mit einem schwereren Phänotyp assoziiert.[2]
Pathophysiologie
Die Funktion der Pyruvatkinase ist für die Erythrozyten essenziell, da sie keine Mitochondrien besitzen und zur Bereitstellung von ATP auf die anaerobe Glykolyse angewiesen sind. ATP wird vom Erythrozyten unter anderem zur Aufrechterhaltung des Natriumgradienten an der Zellmembran via Natrium-Kalium-ATPase benötigt. Je nach Ausprägung des Pyruvatkinasemangels ist die Membranstabilität der Erythrozyten stark eingeschränkt. Dann kommt es zu vermehrter Hämolyse.
Durch Blockade der Glykolyse häufen sich Metaboliten an, insbesondere 1,3-Bisphosphoglycerat, das im Gleichgewicht mit 2,3-Bisphosphoglycerat steht. Dieser Metabolit senkt die Sauerstoffaffinität des Hämoglobins und fördert die Sauerstoffabgabe in das Gewebe. Aus diesem Grund können Patienten mit Pyruvatkinasemangel niedrigere Hämoglobinwerte tolerieren als Patienten mit anderen Anämieformen.
Klinik
Das klinische Spektrum des Pyruvatkinasemangels ist heterogen. Bei homozygoten oder compound-heterozygoten Betroffenen zeigt sich das klassische Bild einer hämolytischen Anämie, meist sogar in Form eines Neugeborenenikterus. Schwere Verläufe können sich bereits intrauterin manifestieren und zu Wachstumsretardierung, Hydrops fetalis oder Frühgeburtlichkeit führen. Der Schweregrad der Anämie ist variabel , bei manchen Patienten kann eine Transfusionspflichtigkeit bestehen. In anderen Fällen entsteht eine kompensierte Hämolyse ohne Anämie, die erst im Rahmen von Infektionen oder während der Schwangerschaft zu hämolytischen Krisen führt.[2]
Weitere mögliche Manifestationen sind Splenomegalie, Ikterus, Cholelithiasis sowie Wachstumsverzögerungen bei schweren Verläufen. Aplastische Krisen treten seltener auf, meist ausgelöst durch Parvovirus-B19-Infektionen. Langzeitkomplikationen umfassen Osteopenie und Osteoporose, die bereits im Jugend- oder frühen Erwachsenenalter auftreten können. Selten kommt es zu extramedullärer Hämatopoese, Beinulzera und pulmonaler Hypertonie.
Diagnostik
Diagnostisch wegweisend ist die hämolytische, hyperregeneratorische Anämie mit typischen Hämolyseparametern. Dazu zählen:
- erhöhtes indirektes Bilirubin
- erhöhtes LDH
- erniedrigtes Haptoglobin und
- Retikulozytose.
Im peripheren Blutausstrich können unspezifische Erythrozytenveränderungen, wie Poikilozytose, Echinozyten oder kontrahierte Erythrozyten, auftreten. Sie sind beim Pyruvatkinase-Mangel typisch, jedoch nicht pathognomonisch.
Die Diagnose wird heute (2026) in der Regel molekulargenetisch gesichert, meist durch Sequenzierung des PKLR-Gens oder im Rahmen eines Genpanels für hereditäre hämolytische Anämien. Die molekulargenetische Diagnostik ist insbesondere bei unklaren enzymatischen Befunden, nach Erythrozytentransfusionen oder bei atypischer Klinik von zentraler Bedeutung.
In Speziallaboren kann zur Differentialdiagnostik eine verminderte Aktivität der Pyruvatkinase in Erythrozyten nachgewiesen werden. Dabei ist zu beachten, dass die Enzymaktivität bei ausgeprägter Retikulozytose oder nach Erythrozytentransfusionen falsch normal bzw. schwer interpretierbar sein kann. Wichtige Differentialdiagnosen sind andere hereditäre hämolytische Anämien, insbesondere die hereditäre Sphärozytose, der Glucose-6-Phosphat-Dehydrogenase-Mangel sowie weitere seltene Enzymdefekte des Erythrozytenstoffwechsels.
Therapie
Die Therapie erfolgt überwiegend supportiv, obwohl in einem Fallbericht eine kurative allogene Stammzelltransplantation gelungen ist. Dennoch ist eine allogene Stammzelltransplantation keine Standardtherapie und bleibt Einzelfällen vorbehalten. Aufgrund des erhöhten Zellumsatzes sollte regelmäßig Folsäure oral substituiert werden. Falls regelmäßig Erythrozytentransfusionen notwendig sind, sollte eine Eisenüberladung mittels Eisenchelatoren verhindert werden. Das Monitoring der Eisenüberladung erfolgt heute (2026) standardisiert mittels Ferritinbestimmung und bildgebender Verfahren (z.B. MRT der Leber).
Seit Februar 2022 ist in den USA zur Behandlung der hämolytischen Anämie bei Pyruvatkinase-Mangel der Pyruvatkinase-Aktivator Mitapivat zugelassen. Mitapivat wurde ebenfalls im November 2022 in der EU zugelassen und ist bei erwachsenen Patienten eine krankheitsspezifische Therapieoption, die den Hämoglobinwert verbessern und den Transfusionsbedarf reduzieren kann.
Bei schweren Krankheitsverläufen kann eine Splenektomie, insbesondere bei überwiegend extravaskulärer Hämolyse, zur Reduktion des Ausmaßes der chronischen hämolytischen Anämie sowie der Häufigkeit hämolytischer Schübe beitragen. Die Indikation wird aufgrund des Risikos für Infektionen (insbesondere OPSI-Syndrom) und Thrombosen heute (2026) zurückhaltend gestellt und individuell abgewogen. Der Nutzen ist variabel und nicht bei allen Patienten gegeben. Eine Szintigraphie mit radioaktiv markierten Erythrozyten kann die Milzbeteiligung darstellen, wird jedoch nicht routinemäßig eingesetzt.
Neue Therapieansätze, wie gentherapeutische Verfahren, befinden sich in klinischer Entwicklung.
Prognose
Die Prognose des Pyruvatkinase‑Mangels ist heterogen und wird neben der Restaktivität der Pyruvatkinase wesentlich durch den Schweregrad der Hämolyse, den Transfusionsbedarf, das Ausmaß der Eisenüberladung sowie durch Langzeitkomplikationen bestimmt. Chronische Fatigue und Einschränkungen der Lebensqualität sind häufige prognoserelevante Faktoren. Ein erhöhtes Thromboserisiko, insbesondere nach Splenektomie, sowie seltene Komplikationen, wie pulmonale Hypertonie, können den Langzeitverlauf ungünstig beeinflussen. Die Einführung krankheitsspezifischer Therapien wie Mitapivat hat bei ausgewählten erwachsenen Patienten das Potenzial, Hämoglobinwerte, Transfusionsbedarf und Lebensqualität nachhaltig zu verbessern.
Quellen
- Orphanet: Pyruvate kinase deficiency, abgerufen am 28.04.2026
- UpToDate: Pyruvate kinase deficiency, abgerufen am 28.04.2026
- Al-Samkari et al., Diagnosis and management of pyruvate kinase deficiency: international expert guidelines, Lancet Haematology, 2024
- Grace et al., Clinical spectrum of pyruvate kinase deficiency: data from the Pyruvate Kinase Deficiency Natural History Study, Blood, 2018
Literatur
- ↑ 1,0 1,1 Rachmilewitz EA et al. Updates and advances in pyruvate kinase deficiency. Trends Mol Med. 2023;29(5):378-392.
- ↑ 2,0 2,1 Bianchi P et al. Pyruvate Kinase Deficiency: Current Challenges and Future Prospects. J Blood Med. 2022;13:691-706.