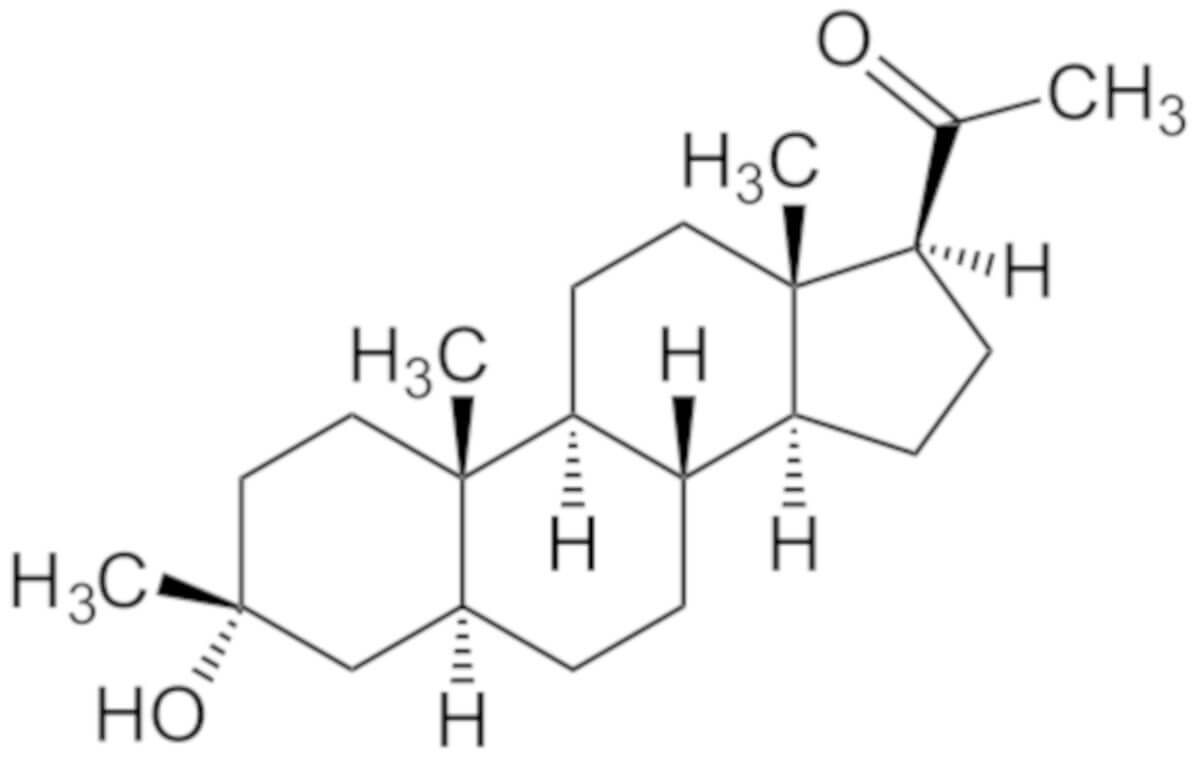
Ganaxolon
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsname: Ztalmy®
Synonym: CCD-1042
Englisch: ganaxolone
Definition
Ganaxolon ist ein Arzneistoff aus der Gruppe der Neurosteroide, der zur Behandlung von Krampfanfällen beim CDKL5-Mangel-Syndrom angewendet wird.
Chemie
Ganaxolon ist ein Methylanalogon des endogenen Neurosteroids Allopregnanolon. Die Summenformel von Galoxon ist C22H36O2. Der chemische Name ist
- 1-[(3R,5S,8R,9S,10S,13S,14S,17S)-3-Hydroxy-3,10,13-trimethyl-1,2,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydrocyclopenta[a]phenanthren-17-yl]ethanon (IUPAC)
Die molare Masse beträgt 332,53 g/mol, der Oktanol-Wasser-Koeffizient (logP) 4.37. Die CAS-Nummer lautet 38398-32-2. Die Substanz liegt bei Raumtemperatur als weißes bis fast weißes kristallines Pulver vor und zeigt nur eine geringe Löslichkeit in Wasser.[1]
Wirkmechanismus
Der genaue Wirkmechanismus von Ganaxolon ist unbekannt. Möglicherweise moduliert der Wirkstoff im ZNS synaptische und extrasynaptische GABA-A-Rezeptoren und normalisiert durch Hyperpolarisation die Erregbarkeit bestimmter Neurone.[1]
Pharmakokinetik
Ganaxolon wird nach oraler Aufnahme rasch resorbiert. Maximale Plasmaspiegel werden nach 2 bis 3 Stunden erreicht. Die Plasmaproteinbindung beträgt 99 %, das Verteilungsvolumen 580 Liter (ca. 8 l/kgKG. Die Biotransformation in der Leber erfolgt über die Cytochrom-P450-Isoenzyme CYP3A4 und CYP3A5 sowie CYP2B6, CYP2C19 und CYP2D6. Anschließend findet eine Glucuronidierung dieser Metaboliten statt, die pharmakologisch nicht aktiv sind. Die Elimination erfolgt zu 55 % mit der Fäzes (nur 2 % unverändert) und zu 18 % mit dem Urin. Die Eliminationshalbwertszeit beträgt in Steady state 8 bis 10 Stunden, terminal 34 Stunden. Die Metaboliten können eine bis zu 230 Stunden längere Halbwertszeit als Ganaxolon haben.[1][2]
Indikation
Ganaxolon ist indiziert als Zusatzbehandlung von epileptischen Anfällen im Zusammenhang mit einer CDKL5-Mangelerkrankung (CDD) bei Patienten im Alter von 2 bis 17 Jahren.[3] Bei Jugendlichen, bei denen ein eindeutiger Nutzen der Behandlung nachgewiesen wurde, kann die Behandlung bis ins Erwachsenenalter fortgesetzt werden. Die Wirksamkeit und Sicherheit des Behandlungsbeginns bei Patienten über 17 Jahren ist derzeit (2023) noch nicht erwiesen. Ein Behandlungsbeginn bei Erwachsenen wird nicht empfohlen.[2]
Darreichungsform
Ganaxolon wird oral in Form einer Suspension verabreicht. Das Medikament muss mit der Nahrung eingenommen werden.
Dosis
Das genaue Dosierungsschema ist abhängig vom Körpergewicht des Patienten; die Dosisanpassung erfolgt in wöchentlichen Abständen:[2]
- Körpergewicht ≤ 28kg: Anfangsdosis dreimal täglich 6 mg/kgKG (1. Woche) bis 21 mg/kgKG (ab 4. Woche)
- Körpergewicht ≥ 28 kg: Anfangsdosis dreimal täglich 150 mg (1. Woche) bis 600 mg (ab 4. Woche)
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Bei einem Abbruch der Behandlung sollte die Dosis schrittweise verringert werden:[2]
- Körpergewicht ≤ 28kg: Gesamttagesdosis alle vier Tage um 15 mg/kg verringern
- Körpergewicht ≥ 28 kg: Gesamttagesdosis alle vier Tage um 450 mg verringern.
Das abrupte Absetzen ist mit dem Risiko einer erhöhten Anfallsfrequenz und eines Status epilepticus verbunden.
Nebenwirkungen
Die häufigsten unerwünschten Wirkungen von Ganaxolon sind:[1][2][4]
- Somnolenz
- Pyrexie
- Hypersalivation
- Allergie durch den Hilfsstoff Benzylalkohol
Aufgrund der sedierenden Wirkung sind Patienten anzuweisen, kein Fahrzeug zu führen und keine Maschinen zu bedienen.
Bei der Anwendung bei Kleinkindern kann ein Gasping-Syndrom ausgelöst werden, bei dem es durch die Anhäufung der aus Benzylalkohol entstehenden Benzoesäure zur metabolischen Azidose mit Anionenlücke, zu neurologischen Störungen mit Krampfanfällen, intraventrikulären Blutungen, schweren Atemstörungen, zum kardiovaskulärem Schock und Nierenversagen kommen kann.[5]
Wechselwirkungen
Die gleichzeitige Anwendung von starken CYP3A4-Induktoren führt zur Wirkungsverminderung, von starken CYP3A4-Inhibitoren zur Wirkungssteigerung. Bei gleichzeitiger Verabreichung von UGT-Inhibitoren (z.B. Valproat) muss eine Dosisanpassung erfolgen.
Wirkstoffe, die das zentrale Nervensystem (ZNS) dämpfen (z.B. Hypnotika, Antiepileptika, Opioide, Antidepressiva) und Alkohol können die sedierenden Nebenwirkungen von Ganaxolon verstärken.[2]
Kontraindikation
- Überempfindlichkeit gegen Ganaxolon oder einen der sonstigen Bestandteile des Arzneimittels.
Missbrauch
Ganaxolon besitzt Missbrauchspotenzial, da in tierexperimentellen Studien bei abruptem Absetzen von Ganaxolon Entzugserscheinungen aufgetreten sind.[2]
Schwangerschaft und Stillzeit
Da keine ausreichenden Daten zur Beurteilung der Reproduktionstoxizität vorliegen, wird die Anwendung von Ganaxolon während der Schwangerschaft und bei Frauen im gebärfähigen Alter nicht empfohlen.
Ganaxolon und seine Metaboliten treten in die Muttermilch über, wobei 4-mal höhere Konzentrationen als im mütterlichen Plasma gemessen wurden. Es ist nicht bekannt, ob Ganaxolon Auswirkungen auf gestillte Neugeborene hat. Ob das Stillen zu unterbrechen ist oder auf die Behandlung während der Stillzeit verzichtet werden soll, ist im Einzelfall zu entscheiden.[2]
Toxizität
Es liegen aktuell (2023) keine Erfahrungen zur Symptomatik einer Überdosierung oder Vergiftung mit Ganaxolon vor. Aufgrund der bekannten Nebenwirkungen ist davon auszugehen, dass es zu komatösen Zuständen mit Krampfanfällen kommen kann. Eine primäre Giftentfernung durch Verabreichung von Aktivkohle kann innerhalb einer Stunde nach der Ingestion unter Intubationsschutz (wegen der Aspirationsgefahr) erfolgen. Die weitere Behandlung erfolgt in jedem Fall symptomatisch. Ein spezifisches Antidot steht bisher (2023) nicht zur Verfügung. Aufgrund seiner pharmakokinetischen Eigenschaften (hohe Plasmaproteinbindung; großes Verteilungsvolumen) ist eine sekundäre Giftentfernung durch Hämodialyse nicht effektiv.
Zulassung
ATC-Code
- N03AX27 - Antiepileptika
Quellen
- ↑ 1,0 1,1 1,2 1,3 Full Prescribing Information Ztalmy, FDA, abgerufen am 08.06.2023
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 2,7 2,8 Zusammenfassung der Merkmale des Arzneimittels Ztalmy, EMA. Abgerufen am 15.08.2023
- ↑ Hoy SM. Ganaxolone: A Review in Epileptic Seizures Associated with Cyclin-Dependent Kinase-Like 5 Deficiency Disorder. Paediatr Drugs. 2025
- ↑ Knight EMP et al. Safety and efficacy of ganaxolone in patients with CDKL5 deficiency disorder: results from the double-blind phase of a randomised, placebo-controlled, phase 3 trial. Lancet Neurol. 2022
- ↑ Gershanik J et al. The gasping syndrome and benzyl alcohol poisoning. N Engl J Med. 1982
Bildquelle
- Strukturformel Ganaxolon CC0 1.0 Universal Public Domain Dedication, by Benff
Weblinks
- Drugs.com - Ganaxolone. Abgerufen am 15.08.2023
- Drugbank - Ganaxolone. Abgerufen am 15.08.2023
- PubChem: 6918305
- MeSH: 67105051