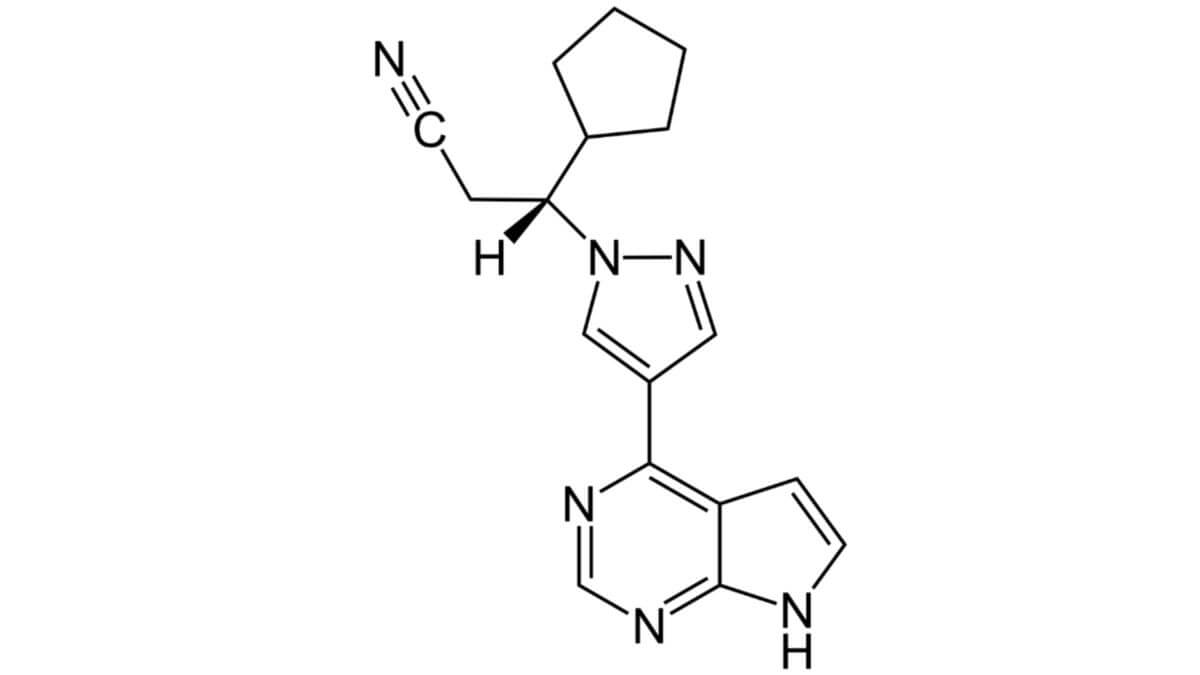
Ruxolitinib
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsname: Jakavi®, Opzelura®
Synonyme: Ruxolitinibum, INC424
Englisch: ruxolitinib
Definition
Ruxolitinib ist ein Arzneistoff aus der Gruppe der Tyrosinkinasehemmer bzw. JAK-Inhibitoren, dessen Anwendungsgebiet die pharmakologische Therapie von Myelofibrosen darstellt. Der Wirkstoff ist seit dem Jahr 2012 auf dem europäischen Arzneimittelmarkt zugelassen. Im Jahr 2023 wurde eine topische Formulierung zur Behandlung der nichtsegmentalen Vitiligo eingeführt.
Chemie
Die Summenformel der Verbindung lautet C17H18N6. Nach der offiziellen IUPAC-Nomenklatur wird Ruxolitinib als (3R)-3-cyclopentyl-3-[4-(7H-pyrrolo[2,3-d]pyrimidin-4-yl)pyrazol-1-yl]propannitril bezeichnet. Es handelt sich um ein aromatisches Kohlenwasserstoffmolekül, das bei Zimmertemperatur in Form eines weißen Pulvers vorliegt. Ruxolitinib ist ein Pyrrolopyrimidinpyrazol-Derivat mit guter Wasserlöslichkeit. Es ist leicht basisch und weist die für Tyrosinkinasehemmer typische Pyrrolo[2,3-d]pyrimidin-Struktur auf, über welche es an das aktive Zentrum des Enzyms bindet. Die molare Masse beträgt 306,37 g/mol.
Pharmakokinetik
Das Verteilungsvolumen liegt bei 75 Litern, die Plasmaproteinbindung bei 97 %. Die Verstoffwechselung erfolgt weitestgehend über CYP3A4 und zu geringeren Anteilen über CYP2C9. Die Eliminationshalbwertszeit beträgt 3 Stunden.
Es handelt sich bei Ruxolitinib um einen Arzneistoff der BCS Klasse 1 (gut löslich, gut membranpermeabel).
Wirkungsmechanismus
Ruxolitinib hemmt die Januskinasen JAK1 und JAK2. Direkte Folge ist eine Unterbrechnung bzw. Deaktivierung des JAK-STAT-Signalweges. Die Aktivität einer ektopen Blutbildung in Leber und Milz wird herabgesetzt. Beide Organe verlieren dadurch an Größe.
Die Wirkung bei Vitiligo wird dadurch erklärt, dass T-Lymphozyten, die für die Zerstörung der Melanozyten verantwortlich gemacht werden, in ihrer Aktivität herabgesetzt werden.
Indikationen
Ruxolitinib ist zur Behandlung folgender Erkrankungen zugelassen:[1]
- Krankheitsbedingte Splenomegalie oder Symptome bei Erwachsenen mit primärer Myelofibrose (auch bekannt als chronische idiopathische Myelofibrose), Post-Polycythaemia-vera-Myelofibrose oder Post-ET-Myelofibrose
- Polycythaemia vera, die resistent oder intolerant gegenüber Hydroxycarbamid ist
- Graft-versus-Host-Erkrankung (GvHD), die unzureichend auf Kortikosteroide oder andere systemische Therapien anspricht
Darüber hinaus ist Ruxolitinib bei topischer Anwendung zur Behandlung der nichtsegmentalen Vitiligo mit Beteiligung des Gesichts zugelassen.[2][3]
Darreichungsform
Dosierung
Systemische Therapie
Die Anfangsdosis zur Behandlung der Myelofibrose ist von der Thrombozytenzahl abhängig und variiert zwischen 5 und 20 mg zweimal täglich. Bei den anderen Indikationen wird die Therapie mit 10 mg zweimal täglich begonnen. Je nach Ansprechen kann die Dosis auf bis zu 25 mg zweimal täglich angehoben werden; treten schwere Nebenwirkungen auf, muss die Dosis reduziert werden. Bei gleichzeitiger Therapie mit starken CYP3A4-Inhibitoren wird nur die Hälfte der Dosis gegeben. Weitere Details sind in der Fachinformation zu finden.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Topische Therapie
Ruxolitinib Creme wird zweimal täglich dünn auf die betroffene Stellen aufgetragen. Zwischen den Anwendungen sollen 8 Stunden liegen und es sollen maximal 10% der gesamten Körperoberfläche auf einmal behandelt werden. Bis eine Repigmentierung eintritt, kann es über 24 Wochen dauern. Sind nach 52 Wochen weniger als 25% der behandelten Hautfläche repigmentiert, kann die Therapie abgebrochen werden. Der Wirkstoff wirkt aus der Creme lediglich lokal und wird kaum systemisch resorbiert. Nach dem Auftragen der Creme sollte der Patient seine Hände waschen.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Nebenwirkungen
- Myelosuppression mit nachfolgender Anämie, Thrombozytopenie und Leukopenie. Die Thrombozyto- und Neutropenie ist reversibel und normalisiert sich nach Dosisanpassung häufig.
- Blutungen: Blutergüsse, gastrointestinale und kranielle Blutungen
- Hypercholesterinämie, Hypertriglyceridämie, Gewichtszunahme
- erhöhte Infektneigung (Harnwegsinfekte, Herpes zoster, Pneumonie, Sepsis)
- Kopfschmerzen, Schwindel
- Obstipation, Flatulenz, erhöhte Lipasewerte
- Anstieg von Leberenzymen: ALAT, AST
- Hypertonie
- Absetzreaktion: Wird Ruxolitinib abgesetzt, können innerhalb einer Woche Symptome der Myelofibrose auftreten. Um dies vorzubeugen, sollte die Dosis langsam ausgeschlichen werden.
Bei der topischen Anwendung wurde lediglich Akne an der Applikationsstelle als Nebenwirkung beschrieben.
Wechselwirkungen
- Ruxolitinib wird durch CYP3A4 metabolisiert, weshalb es zu Wechselwirkungen mit CYP3A4-Inhibitoren (Erhöhung der Ruxolitinib-Konzentration und vermehrte Nebenwirkungen) und CYP3A4-Induktoren (erniedrigte Ruxolitinib-Konzentrationen und verminderte Wirkung) kommen kann.
- Ruxolitinib ist ein Inhibitor von P-gp und BCRP und erhöht somit die Plasmaspiegel von Substanzen, die Substrate dieser Transporter sind.
Bei der topischen Anwendung sind wegen der geringen systemischen Bioverfügbarkeit keine Wechselwirkungen mit anderen Medikamentenn zu erwarten. Bevor eine andere Creme aufgetragen wird, sollte jedoch mindestens zwei Stunden gewartet werden.
Kontraindikationen
- Überempfindlichkeit gegenüber dem Wirkstoff
- Schwangerschaft und Stillzeit
Literatur
- Neubauer, A., Wiesmann, T., Vogelmeier, C.F. et al. Ruxolitinib for the treatment of SARS-CoV-2 induced acute respiratory distress syndrome (ARDS). Leukemia 34, 2276–2278 (2020). https://doi.org/10.1038/s41375-020-0907-9
- ↑ Zusammenfassung der Merkmale des Arzneimittels Jakavi, EMA, abgerufen am 17.07.2024
- ↑ Zusammenfassung der Merkmale des Arzneimittels Opzelura, EMA, abgerufen am 17.06.2024
- ↑ 3,0 3,1 Kang C. Ruxolitinib Cream 1.5%: A Review in Non-Segmental Vitiligo. Drugs. 2024