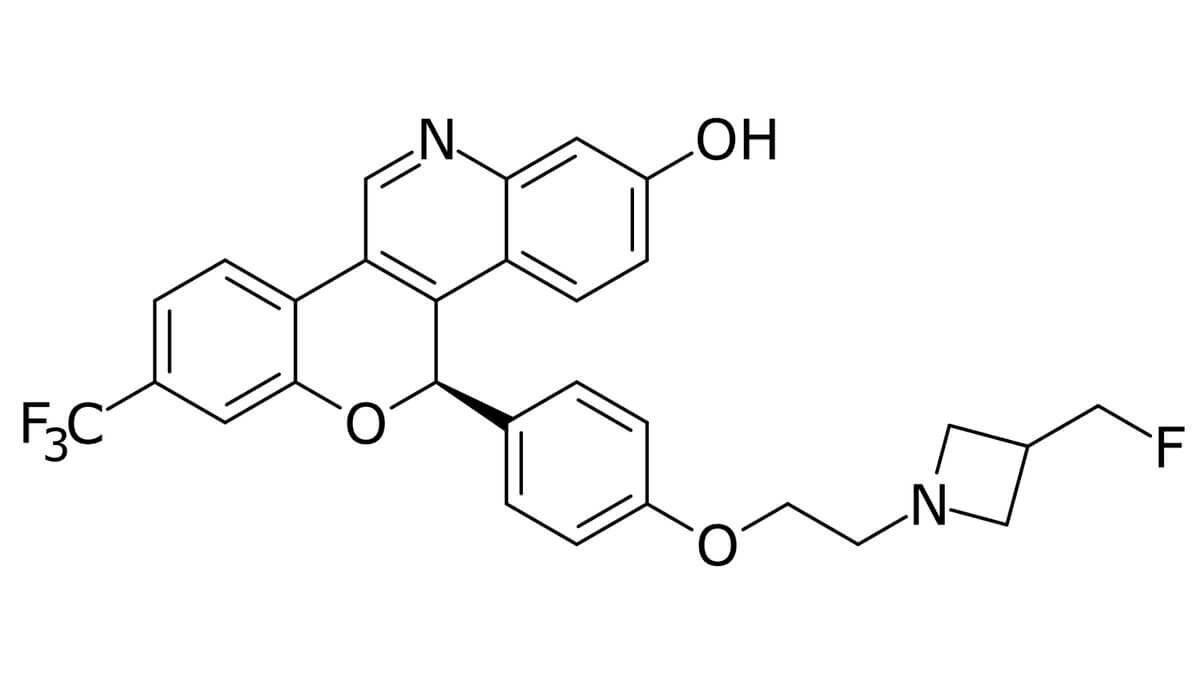
Imlunestrant
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsname: Inluriyo®
Englisch: imlunestrant
Definition
Imlunestrant ist ein oral verfügbarer selektiver Östrogenrezeptor-Degrader (SERD) mit antiöstrogener Wirkung. Der Arzneistoff wird als Monotherapie zur Behandlung von Erwachsenen mit Östrogenrezeptor(ER)-positivem, HER2-negativem, lokal fortgeschrittenem oder metastasiertem Mammakarzinom mit aktivierender ESR1-Mutation eingesetzt, wenn nach einer vorausgegangenen endokrinen Therapie eine Krankheitsprogression eingetreten ist.[1][2]
Chemie
Imlunestrant wird arzneilich als Imlunestranttosylat eingesetzt. Eine Filmtablette enthält Imlunestranttosylat entsprechend 200 mg Imlunestrant.[1] Die Summenformel lautet C29H24F4N2O3. und die molare Masse beträgt 524,51 g/mol.
Wirkmechanismus
Imlunestrant ist ein Antagonist des Wildtyp- und mutierten Östrogenrezeptors α (ERα), der zugleich den Abbau des Rezeptors induziert. Dadurch werden die östrogenrezeptorabhängige Gentranskription und die Proliferation ER-positiver Tumorzellen gehemmt.[1]
Pharmakokinetik
Nach oraler Gabe von 400 mg beträgt die absolute Bioverfügbarkeit im Mittel 10,5 %, die mediane Zeit bis zum Erreichen der maximalen Plasmakonzentration (Cmax) etwa 4 Stunden.[1] Im Steady State werden bei 400 mg einmal täglich mittlere Cmax-Werte von 141 ng/ml und eine AUC0-24h von 2.400 ng*h/ml erreicht.[1] Die Einnahme mit Nahrung erhöht die Exposition deutlich. Nach einer fettarmen Mahlzeit stiegen Cmax und AUC gegenüber der Nüchterneinnahme auf das 3,55-Fache bzw. 2,04-Fache an. Daher soll Imlunestrant nüchtern eingenommen werden.[1]
Das Verteilungsvolumen beträgt 4.310 l, die Proteinbindung liegt bei 99,93 bis 99,96 %. Der Abbau erfolgt durch Sulfatierung, CYP3A4-vermittelte oxidative Prozesse und direkte Glucuronidierung. Die Eliminationshalbwertszeit beträgt etwa 30 Stunden. Nach einer radioaktiv markierten Einzeldosis wurden 97,3 % im Fäzes und 0,278 % im Urin wiedergefunden.[1]
Indikationen
Imlunestrant ist in der EU als Monotherapie indiziert bei Erwachsenen mit ER-positivem, HER2-negativem, lokal fortgeschrittenem oder metastasiertem Mammakarzinom mit aktivierender ESR1-Mutation nach Progress unter mindestens einer endokrinen Therapie.[1][2] Bei prä- oder perimenopausalen Frauen sowie bei Männern ist die Behandlung mit einem LHRH-Agonisten zu kombinieren.[1]
Darreichungsform
Imlunestrant ist als Filmtablette mit 200 mg Wirkstoff zur oralen Anwendung verfügbar.[1]
Dosierung
Die empfohlene Dosis beträgt 400 mg einmal täglich, entsprechend 2 Filmtabletten zu 200 mg.[1][3] Die Einnahme soll möglichst täglich zur gleichen Zeit erfolgen, mindestens 2 Stunden vor dem Essen oder 1 Stunde nach dem Essen. Die Tabletten sollen unzerkaut geschluckt und nicht geteilt, zerdrückt oder gekaut werden.[1] Dosisanpassungen können bei Nebenwirkungen, bei gleichzeitiger Gabe starker CYP3A-Inhibitoren bzw. -Induktoren und bei Leberfunktionsstörungen erforderlich sein.[1]
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Nebenwirkungen
Die häufigsten klinisch relevanten Nebenwirkungen sind erhöhte Transaminasen, Fatigue, Diarrhoe, Übelkeit und Erbrechen.[1]
Weitere häufige bzw. klinisch relevante unerwünschte Wirkungen sind unter anderem:[3][1]
Wechselwirkungen
Imlunestrant wird unter Beteiligung von CYP3A4 metabolisiert. Starke CYP3A4-Induktoren vermindern, starke CYP3A4-Inhibitoren erhöhen die Exposition und sollten möglichst vermieden werden. Falls dies nicht möglich ist, muss die Dosis angepasst werden.[1] Außerdem kann Imlunestrant die Exposition bestimmter Begleitmedikationen erhöhen. Klinisch relevant ist dies insbesondere bei:
- CYP2D6-Substraten
- P-Glykoprotein-Substraten
- BCRP-Substraten[1]
Für Protonenpumpenhemmer wie Omeprazol wurde kein klinisch relevanter Einfluss auf die Pharmakokinetik von Imlunestrant gezeigt.[1]
Kontraindikationen
Kontraindikationen sind:
- Stillzeit
- Überempfindlichkeit gegen Imlunestrant oder einen der sonstigen Bestandteile[1]
Während der Behandlung soll eine Schwangerschaft ausgeschlossen sein. Aufgrund des Wirkmechanismus und tierexperimenteller Daten kann Imlunestrant den Fetus schädigen. Frauen im gebärfähigen Alter und zeugungsfähige Männer sollen während der Therapie und mindestens 1 Woche nach der letzten Dosis eine hochwirksame Kontrazeption anwenden.[1]
Zulassung
Imlunestrant wurde im September 2025 in den USA und im Januar 2026 in der EU zugelassen.[4] Die Zulassung basiert im Wesentlichen auf der randomisierten Phase-3-Studie EMBER-3. In der Population mit ESR1-mutierten Tumoren betrug das mediane progressionsfreie Überleben unter Imlunestrant 5,5 Monate gegenüber 3,8 Monaten unter Standardtherapie (Fulvestrant oder Exemestan). Die Hazard Ratio lag bei 0,62.[3][5]
Quellen
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 1,13 1,14 1,15 1,16 1,17 1,18 1,19 EMA-Fachinformation Inluriyo, zuletzt abgerufen am 17.03.2026
- ↑ 2,0 2,1 EMA: Inluriyo, zuetzt abgerufen am 17.03.2026
- ↑ 3,0 3,1 3,2 U.S. Food & Drug Administration (FDA): FDA approves imlunestrant for ER-positive, HER2-negative, ESR1-mutated advanced or metastatic breast cancer, zuletzt abgerufen am 17.03.2026
- ↑ Gelbe Liste: Neueinführung Inluriyo: Neue SERD-Monotherapie bei ESR1-mutiertem Mammakarzinom, zuletzt abgerufen am 17.03.2026
- ↑ ClinicalTrials.gov: A Study of Imlunestrant, Investigator's Choice of Endocrine Therapy, and Imlunestrant Plus Abemaciclib in Participants With ER+, HER2- Advanced Breast Cancer (EMBER-3), zuletzt abgerufen am 17.03.2026