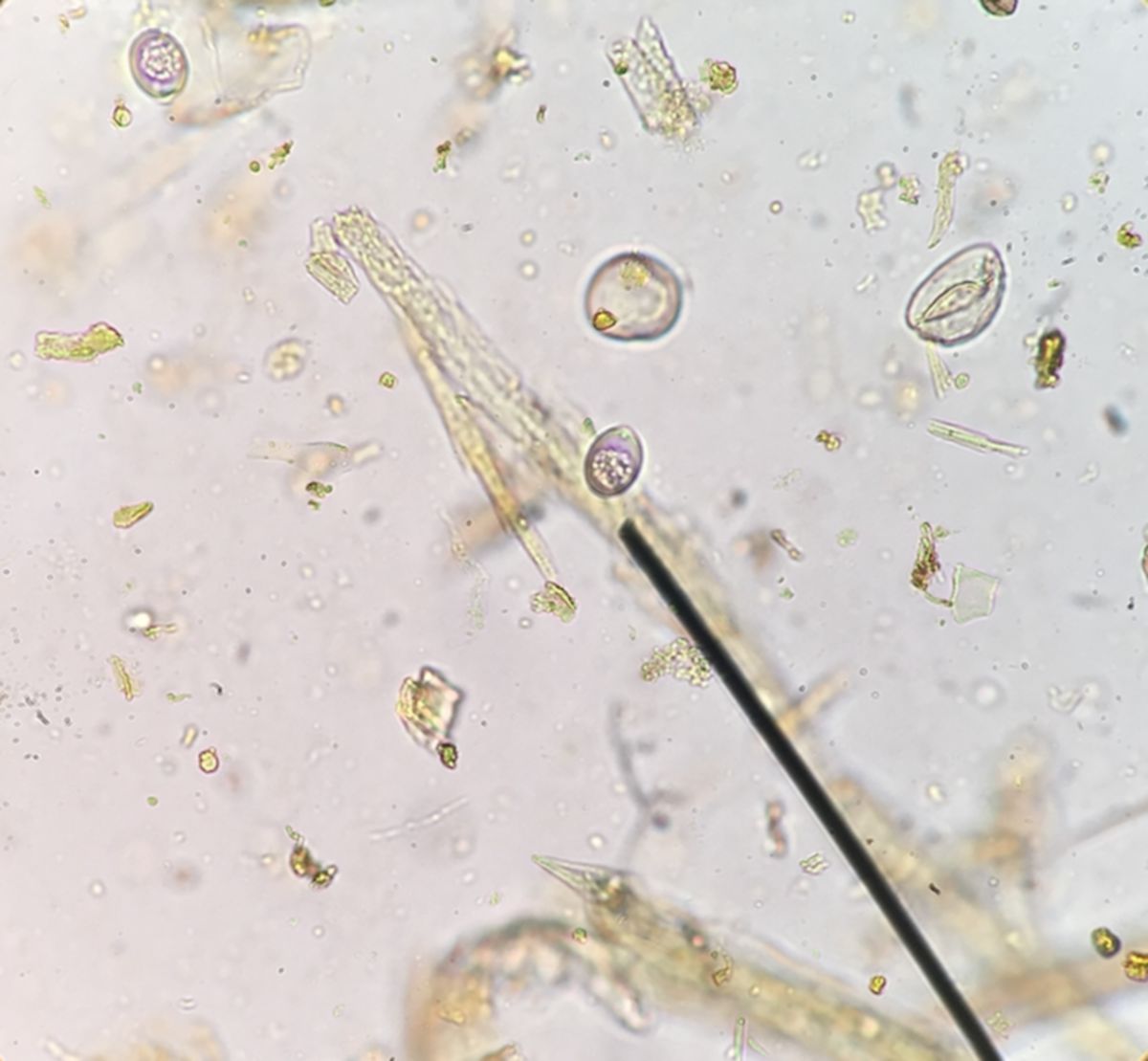
Eimeriose (Rind)
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: Eimeria-Infektion beim Rind
Definition
Als Eimeriose des Rindes bezeichnet man eine parasitär bedingte Erkrankung des Rindes durch Eimeria-Arten.
Erreger
Folgende Tabelle zeigt die zehn wichtigsten Eimeria-Arten des Rindes:
| Eimeria-Art | Größe Oozyste (μm) |
Größe Sporozyste (μm) |
Präpatenz (Tage) |
|---|---|---|---|
| E. bovis | 26 - 32 x 18 - 21 | 14 - 17 x 6 - 8 | 18 - 21 |
| E. zuernii | 16 - 20 x 15 - 18 | 8 - 10 x 4 - 6 | 15 - 17 |
| E. ellipsoidalis | 18 - 26 x 13 - 18 | 12 - 16 x 5 - 6 | 8 - 13 |
| E. aubumensis | 36 - 46 x 19 - 26 | 16 - 21 x 8 - 1 | 16 - 24 |
| E. wyomingensis | 36 - 45 x 26 - 30 | 19 x 18 | 14 - 15 |
| E. pellita | 32 - 42 x 22 - 27 | 17 - 20 x 7 - 8 | * |
| E. cylindrica | 16 - 27 x 12 - 15 | * | 10 |
| E. brasiliensis | 33 - 42 x 23 - 30 | 17 - 21 x 8 - 10 | * |
| E. alabamensis | 33 - 42 x 23 - 30 | 10 - 12 x 4 - 6 | 6 - 8 |
| E. subspherica | 10 - 13 x 9 - 12 | 7 - 8 x 3 - 5 | 7 - 18 |
| * = unbekannt | |||
Vorkommen
Weltweit sind beim Rind 21 Eimeria-Arten bekannt. In Mitteleuropa sind bisher 13 Arten verbreitet. Je nach Haltungsform und Weideverhältnissen schwanken die Befallsraten zwischen 12 und 100 %. Der durch Eimerien verursachte wirtschaftliche Schaden richtet sich nach der Virulenz der vorliegenden Eimeria-Art und dem Befallsgrad.
Der weltweit bei Rindern durch Kokzidien verursachte Schaden wird auf rund 700 Millionen Dollar pro Jahr geschätzt.
Entwicklung
Die Oozysten sporulieren in der Umwelt, wobei dieser Prozess durch höhere Temperaturen und Feuchtigkeit gefördert wird. Die sporulierten Oozysten sind deutlich widerstandsfähiger als unsporulierte und bleiben unter mitteleuropäischen Bedingungen auf der Weide bis zu einem Jahr lebensfähig. Eine Infektion erfolgt durch orale Aufnahme sporulierter Oozysten. Die endogenen Entwicklungsstadien sitzen - je nach Eimeria-Art - in unterschiedlichen Darmabschnitten sowie Schichten der Darmwand. Die endogene Entwicklung ist nur bei wenigen Arten erforscht.
Eimeria bovis
Bei einem pH-Wert von 7,5 bis 8,5 und unter Einfluss von Trypsin und Galle werden die Sporozoiten freigesetzt. Diese dringen in die Schleimhaut der hinteren Dünndarmhälfte ein, um dort in den Endothelzellen der zentralen Lymphkapillaren bis zu 300 μm großen und bereits makroskopisch als weiße Pünktchen erkennbare Makromeronten heranzuwachsen.
Innerhalb von 14 bis 18 Tagen entwickeln sich in ihnen die etwa 12 μm langen Merozoiten, die in die Epithelzellen von Caecum und Dickdarm eindringen. In den Zellen bilden sie innerhalb von 2 Tagen die zweite Merontengeneration mit je 30 bis 36 Merozoiten. Aus ihnen bilden sich dann Makro- und Mikrogamonten, die im Wesentlichen die Schädigung und die klinischen Symptome der Eimeriose hervorrufen.
Die Präpatenz beträgt zwischen 18 und 21 Tagen, die Patenz 5 bis 15 Tage.
Eimeria zuernii
Die erste Merogonie (ungeschlechtliche Zellteilung) von Eimeria zuernii läuft in der Lamina propria des Ileums ab. Anschließend kommt es zur Bildung von Makromeronten. Die zweite Merogonie läuft in den Epithelzellen des Caecums ab und die Gamogonie im Caecum und im Dickdarm.
Die Präpatenz beträgt 15 bis 17 Tage und die Patenz ca. 11 Tage.
Epidemiologie
Typisch für Eimeriosen ist, dass die meisten Rinder mit Eimeria-Arten befallen sind, jedoch nur in einigen Betrieben und bei meist relativ wenigen Tieren klinische Erkrankungen auftreten. In Einzelfällen beträgt die Morbidität jedoch 100 %.
Unter den meisten Rindergruppen besteht enzootische Stabilität. Darunter versteht man, dass ständige Infektionen mit subklinischen Mengen von Oozysten eine Immunität aufrecht hält. So kommt es bei begrenzter Oozystenausscheidung nicht zu einem krankheitsverursachenden Infektionsrisiko. Als Infektionsquellen gelten kotverschmutzte Medien wie Futter, Wasser, Einstreu, Tränkeplätze, Wände und das Haarkleid der Tiere. Ebenso kann Heu von kontaminierten Weiden eine Infektionsquelle darstellen.
Die Oozysten in der Umwelt stammen primär aus Kälbern. Im Gegensatz dazu können auch ältere Tiere oft noch Oozysten im Kot ausscheiden. Kühe weisen peripartal einen deutlichen Anstieg der Oozystenausscheidung auf.
Erkrankungen treten meist dann auf, wenn nicht immune Tiere aller Altersgruppen in eine kontaminierte Umgebung gebracht werden, z.B. 3 Wochen nach dem Umsetzen der Kälber aus Einzel- in Gruppenboxen (v.a. Eimeria bovis, Eimeria zuernii) oder in den ersten 2 Wochen nach dem Austrieb der Kälber auf kontaminierte Weiden (v.a. Eimeria alabamensis).
Pathogenese
Entsprechend den verschiedenen Entwicklungsorten einzelner Eimeria-Arten treten auch unterschiedliche Veränderungen auf. Die meisten Eimeria-Arten führen zu epithelialen Dünndarmschäden, wohingegen beim Befall mit Eimeria bovis und Eimeria zuernii Dickdarmläsionen (mit Beteiligung tieferer Gewebeschichten) zu beobachten sind.
Eimeria bovis und Eimeria zuernii (die virulentesten Arten) führen zu geringen Reaktionen im distalen Bereich des Dünndarmes - verursacht durch Makromeronten in Endothelzellen der zentralen Lymphgefäße von Darmzotten. Die zweiten Meronten und Gamonten führen hingegen zu schweren Veränderungen - insbesondere im Caecum - aber auch in den distalen zwei Metern des Dünndarmes und im proximalen Dickdarm. So sind in der 2. Woche p.i. fast alle Epithelzellen an der Basis der Drüsen mit zwei Meronten und Gamonten besetzt. Die Drüsen sind dabei erweitert, subepithelial zellulär infiltriert, im Bereich der Lamina propria und Submukosa ödematös und mit erweiterten Lymph- und Blutgefäßen ausgestattet.
In den darauf folgenden Tagen heben sich die Epithelien großflächig von ihrer Unterlage ab. Auf der darunter liegenden nackten Lamina propria befinden sich diphteroide Membranen aus Blut, Fibrin, Granulozyten, Bakterien, Oozysten und Zellresten. Die Kapillaren erscheinen deutlich erweitert, thrombosiert und aufgerissen. Ab der 3. Woche p.i. sind dichte, flache Lagen von Granulationsgewebe ersichtlich, die die Mukosa ersetzen (oft bis zur Lamina muscularis mucosae reichend). Infolge einer totalen Zerstörung der Drüsenzellen sind nur noch Epithelinseln sichtbar. Alle darunter liegenden (tiefen) Gewebeschichten werden ödematös, stark zellig infiltriert und hyperämisch.
Durch Veränderungen im Dickdarm entstehen Resorptionsstörungen, die sich durch Wasserverlust mit dem Kot und verminderte Plasmakonzentrationen von Na+- und Cl--Ionen bemerkbar machen. Die Folge ist eine Dehydrierung. Die Todesursache von Kälbern in der Anfangsphase der Erkrankung ist auf Exsikkose infolge des Verlustes von Plasmaproteinen und Mineralstoffen zurückzuführen. Ein später eintretender Tod beruht meist auf einer Anämie infolge eines Erythrozytenverlustes.
Die restlichen Eimeria-Arten führen meist nur zu Epithelschäden und vermehrter Schleimbildung sowie einer katarrhalischen Enteritis.
Immunität
Subklinische Infektionen induzieren bereits eine Immunität, die je nach Eimeria-Art und in Abhängigkeit von der Immunisierungsdosis mehr oder weniger stark ausgeprägt ist. Kreuzimmunitäten zwischen den einzelnen Arten gibt es nicht.
Die im Serum infizierter Tiere nachweisbaren Antikörper weisen keinen schützenden Effekt auf. Die Immunität wird ausschließlich durch T-Lymphozyten vermittelt.
Klinik
Eine Infektion mit Eimeria bovis oder Eimeria zuernii führt anfangs bei erhaltenem Appetit und normaler Körpertemperatur zu Koterweichung. Am nächsten Tag folgt Diarrhö mit grünlich-braunen, schleimig-stinkenden Kot, der in dünnflüssigen und blutigen Kot übergehen kann. Im Kot können Schleimhautfetzen oder diphtheroide Membranen beigemengt sein, wobei der Kotabsatz unter hohem Druck in kleinen Portionen explosionsartig entleert wird. Dabei wird oftmals der Schwanz verschmutzt und der Kot läuft an den Hinterbeinen herab. Diese Phase ist oftmals mit Körpertemperaturen um 40 °C und abnehmender Fresslust begleitet, wohingegen das Trinkbedürfnis steigt. Die Tiere zeigen einen aufgeschürzten Leib mit eingefallenen Flanken. Sie schlagen mit den Beinen sowie dem Kopf nach dem Bauch, knirschen mit den Zähnen und werden zunehmend schwächer.
Um den 4. Tag der Erkrankung verändert sich der Kotabsatz: der wässrig-rote Kot (dem Blutkoagula in Form langer Darmausgüsse beigemengt sind) wird unter starkem Pressen in kleinsten Portionen bei abgehobenem Schwanz und aufgekrümmten Rücken abgegeben ("Rote Ruhr"). Der Tenesmus verstärkt sich bei stark verdickter und in Längsfalten gelegter Rektalschleimhaut so sehr, dass infolge von Sphinkterlähmung die Analschleimhaut sichtbar wird oder gar ein Mastdarmvorfall eintritt.
Zusätzliche Symptome sind: Dehydrierung mit eingesunkenen Augäpfeln, verminderter Hautturgor mit lederartiger Hautbeschaffenheit, blasse Schleimhäute und erhöhte Herzfrequenz (Hinweis auf Anämie). Die Pansentätigkeit ruht weitgehend, sodass nach Absinken der Körpertemperatur auf subnormale Werte in dieser Krankheitsphase meist mit Todesfällen zu rechnen ist.
Eine Genesung kann etwa vom 6. Krankheitstag an einsetzen (bei nicht-hämorrhagischer Enteritis jedoch früher). Dabei verschwinden die Blutbeimengungen im Kot, wobei Diarrhö und Tenesmus noch mehrere Tage andauern können. Obwohl der Appetit stetig zunimmt, bleiben allgemeine Schwäche, Abmagerung und struppiges Haar oftmals noch wochenlang bestehen.
Die durch Toxine verursachte besondere Form der Eimeria-zuernii- und Eimeria-bovis-Kokzidiose ist mit zerebralen Symptomen, wie etwa tetanischen Krämpfen, Überempfindlichkeit, Nystagmus, Opisthotonus, Radfahrergang und hoher Letalität vergesellschaftet.
Diagnose
Eine Diagnose wird anhand der Anamnese und der klinischen Symptome gestellt. Durch wiederholte Kotuntersuchungen mit Flotationsverfahren kann die Erkrankung gesichert werden. Klinische Symptome können schon bereits während der Inkubationszeit auftreten - noch lange bevor Oozysten ausgeschieden werden (Präpatenz). In dieser Phase können rektal entnommene Schleimhautabstriche eine Diagnosestellung sichern.
Therapie
Da die verfügbaren Medikamente nur gegen die Meronten wirken - die klinischen Erscheinungen aber durch die erst später auftretenden Gamonten verursacht werden - ist eine echte kausale Therapie bei einem Befall mit Eimeria bovis bzw. Eimeria zuernii nicht möglich. Da in den meisten Fällen die Tiere in einer Gruppe nacheinander erkranken, ist eine Gruppenbehandlung beim ersten Auftreten einer Eimeriose sinnvoll.
Eine Befall mit Eimeria alabamensis ist weniger problematisch. Hier kann eine Therapie mit Sulfadimidin-Na (50 bis 100 mg/kgKG täglich bis zur Besserung) oder Toltrazuril (20 mg/kgKG täglich über 2 Tage) angestrebt werden. In kritischen Fällen kann auch eine Behandlung mit Sulfonamiden i.v. (langsame Injektion) erfolgen. Begleitend sollte der Elektrolythaushalt aufrechterhalten und auf eine Trockenfütterung umgestellt werden.
Prophylaxe
Ställe sollten möglichst hygienisch betrieben werden, um Eimeriosen zu verhindern. Als geeignetste Prophylaxe hat sich Trockenheit und Sauberkeit erwiesen.
Literatur
- Boch, Josef, Supperer, Rudolf. Veterinärmedizinische Parasitologie. 6. vollständig überarbeitete und erweiterte Auflage. Parey Verlag, 2005