Taenia solium
Synonym: Schweinebandwurm
Definition
Taxonomie
- Phylum: Plathelminthes
- Subphylum: Neodermata
Vorkommen
Merkmale
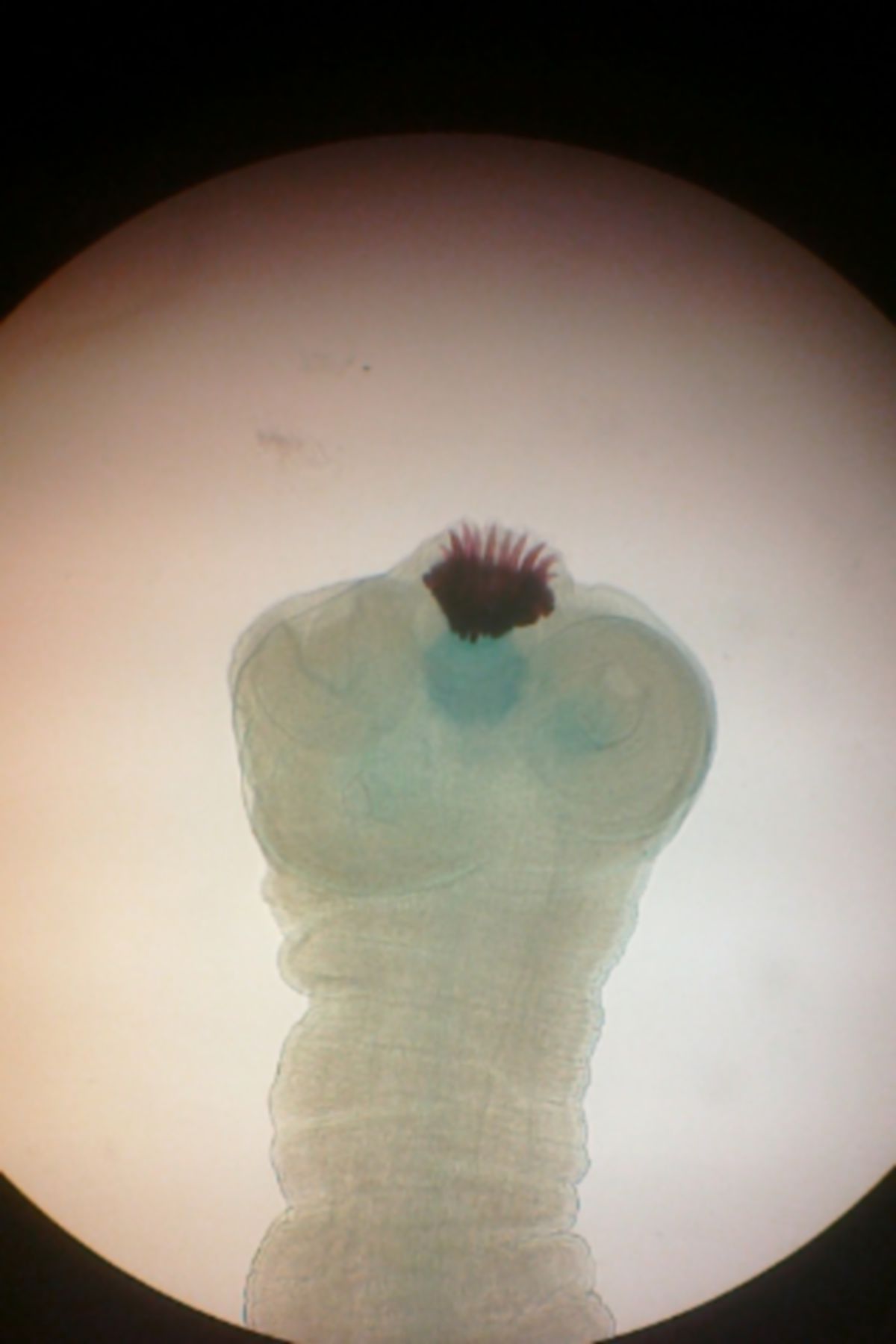
Der Wurm lebt als Parasit im oberen Jejunum des Menschen, der den einzigen Endwirt darstellt. Sein Scolex haftet mittels Saugnäpfen und zwei Hakenreihen an der Darmwand an. Dort kann der adulte Wurm über Jahre leben.
Taenia solium ist durchschnittlich 3 Meter lang und besitzt bis zu 1.000 Proglottiden, von denen jede bis zu 50.000 infektiöse Eier produzieren kann. Diese werden mit dem Stuhl ausgeschieden. Morphologisch unterscheidet sich Taenia solium vom Rinderbandwurm (Taenia saginata) durch Proglottiden mit nur 7-13 Uterusseitenästen, im Gegensatz zu 15-20 bei Taenia saginata. Der Schweinebandwurm hat einen Hakenkranz am Scolex, der beim Rinderbandwurm fehlt.
Lebenszyklus
Nach Aufnahme der Eier in den Zwischenwirt (Schwein und z.T. andere Tiere) schlüpfen die Embryos aus den Eiern, durchdringen die Darmwand und gelangen in verschiedene Gewebe, v.a. in die quergestreifte Muskulatur des Halses, der Zunge und des Rumpfes. Innerhalb von 60-90 Tagen entwickelt sich die Larve innerhalb der Zyste. Diese Zystizerken können über Monate bis Jahre überleben. Das Finnenstadium wird als Zystizerkose (Cysticercus cellulosus) des Schweines bezeichnet.
Eine Infektion des Menschen erfolgt nach Verzehr von ungenügend gekochtem Fleisch, das Zystizerken oder Finnen enthält. Im Darm des Menschen entwickeln sich dann die reifen Bandwürmer, die bis zu 20 Jahre überleben können.
Gelegentlich kann es aber passieren, dass auch der Mensch versehentlich zum Zwischenwirt ("Fehlzwischenwirt") wird. Diese Zystizerkose des Menschens entsteht nach der Ingestion von Eiern, die z.B. unter den Fingernägeln von Bandwurmträgern zu finden sind. Entsprechend erfordert die Übertragung einen engen Kontakt mit einer infizierten Person. Weiterhin kann es zu einer Autoinfektion kommen, wenn ein Bandwurmträger Eier aus dem eigenen Stuhl aufnimmt.
Klinik
Taeniasis
Die intestinale Infektion mit Taenia solium (Taeniasis) verläuft häufig symptomlos, wobei der Abgang von Proglottiden mit dem Kot gelegentlich bemerkt wird.
Zystizerkose
Die Manifestation der Zystizerkose variiert je nach Anzahl und Lokalisation der Zystizerken sowie in Abhängigkeit vom Ausmaß der begleitenden Entzündungsreaktion. Die Zystizerken können überall im Körper verteilt sein, am häufigsten im Gehirn, im Liquor, im Skelettmuskel, im subkutanen Gewebe sowie im Auge. Am häufigsten finden sich neurologische Symptome. Die entzündliche Reaktion im Hirnparenchym kann zu zerebralen Krampfanfällen führen. Eine Liquorabflussbehinderung durch Zystizerken, entzündliche Reaktionen oder Arachnoiditis führen zu einem Hydrozephalus. Dabei finden sich oft Zeichen eines erhöhten Hirndrucks (Kopfschmerzen, Übelkeit, Erbrechen, Sehstörungen, Schwindel, Ataxie, Verwirrtheit). Weiterhin können ein Papillenödem oder kognitive Defizite auftreten. Zystizerken an der Hirnbasis oder im Subarachnoidalraum führen zu einer chronischen Meningitis, Arachnoiditis, Blutungen oder Schlaganfällen.
Bei Muskel- und Hautbefall kann es zu rheumatoiden Beschwerden kommen. Die Finnen sterben nach einigen Jahren ab. Radiologisch zeigen sich dann oft sichtbare Verkalkungen.
Diagnostik
Taeniasis
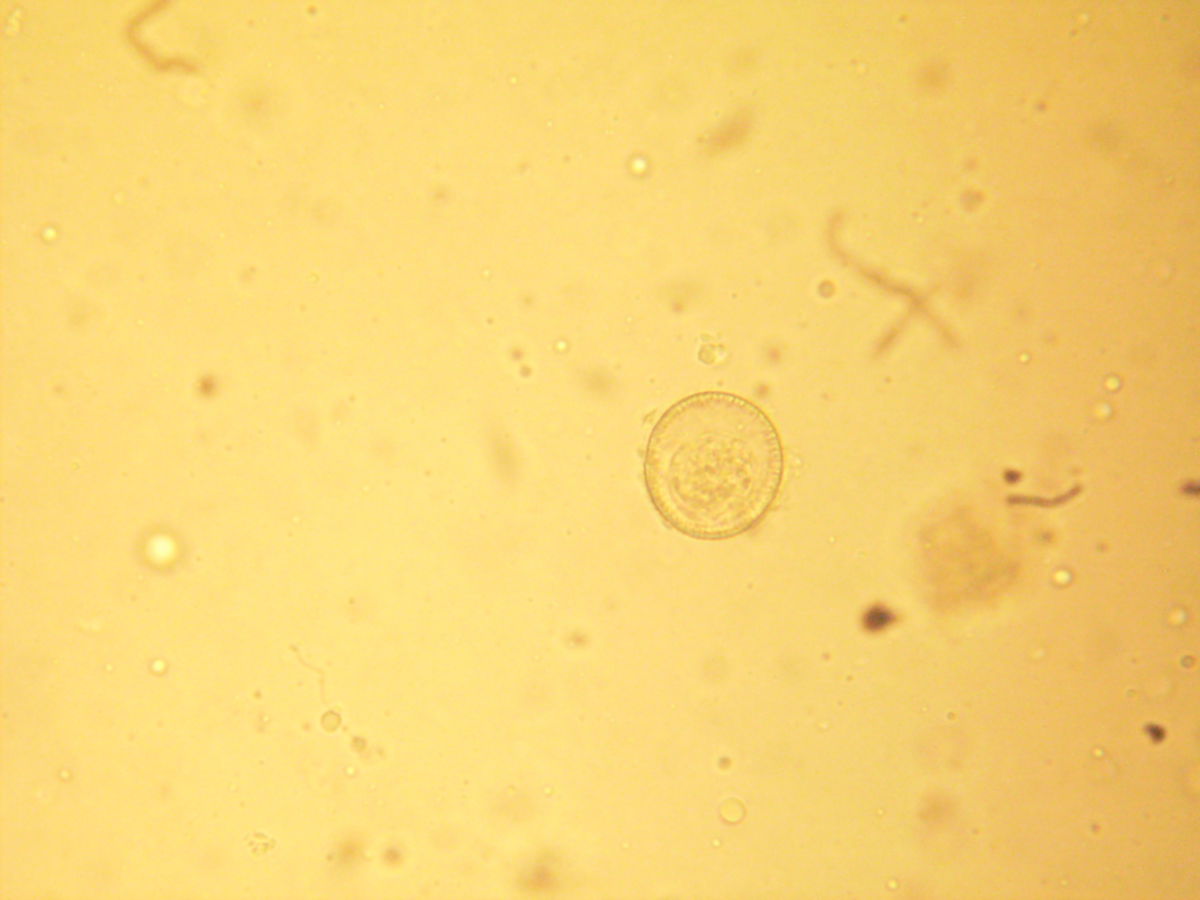
Bei der Taeniasis erfolgt die Diagnose über den Nachweis von Eiern oder Proglottiden im Stuhl (wie bei Taenia saginata). Weitere Methoden (ELISA, PCR, Antigenserologie) werden derzeit (2020) nur zu Forschungszwecken eingesetzt.[1][2] In Erprobung befinden sich Schnellteste auf Basis von RNA-Sensoren.[3]
Zystizerkose
Bei der Zystizerkose ist die Diagnosestellung schwierig. Notwendig ist der direkte Nachweis des Parasiten durch histologische Untersuchung von exzidiertem Gewebe, durch Fundoskopie oder durch neuroradiologische Untersuchungen.
Für die Neurozystizerkose existieren folgende diagnostische Kriterien:[4]
| A: Absolute Kriterien |
|
| B: Neuroradiologische Kriterien | Major-Kriterien (B1):
|
Bestätigende Kriterien (B2):
| |
Minor-Kriterien (B3):
| |
| C: Klinische Kriterien | Major-Kriterien (C1):
|
Minor-Kriterien (C2):
| |
gesicherte Diagnose:
| |
wahrscheinliche Diagnose:
| |
In der Liquoranalyse kann eine Pleozytose (lymphozytär, granulozytär oder eosinophil) nachweisbar sein. Der Proteingehalt ist meist erhöht, die Glukose liegt im Normbereich oder ist erniedrigt.
Therapie
Taeniasis
Die Taeniasis mit Taenia solium wird mit einer Einzeldosis Praziquantel (10 mg/kgKG) behandelt. Weiterhin ist Niclosamid (2 g) wirksam.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Zystizerkose
Bei einer Zystizerkose müssen insbesondere Krampfanfälle mittels antikonvulsiver Medikamente behandelt werden. Wenn die Läsionen ohne Kalzifikation abheilen, kann die Medikation üblicherweise nach 1-2 Jahren beendet werden. Antihelminthika können zur Ausheilung der neuroradiologisch sichtbaren Läsionen sowie zur Reduktion der Krampfanfälle führen. Eingesetzt werden Albendazol (15 mg/kgKG/d für 8-28 Tage) und/oder Praziquantel (50-100 mg/kgKG/d für 15-30 Tage). Manchmal ist zu beobachten, dass Teile des Wurms (mitunter auch der ganze Wurm) im Stuhlgang auftauchen. Beide Wirkstoffe können jedoch die entzündliche Reaktion auf den Parasiten verstärken, die Krampfbereitschaft erhöhen und einen Hydrozephalus verschlechtern. Daher sollten die Patienten engmaschig überwacht werden und ggf. Glukokortikoide verabreicht werden. Da diese aber den First-Pass-Metabolismus von Praziquantel verstärken, muss begleitend Cimetidin gegeben werden.
Bei Patienten mit einem Hydrozephalus sollte der intrakranielle Druck reduziert werden, beispielsweise durch endoskopisch-chirurgische Entfernung des Zystizerkus. Alternativ kann vorher eine Entlastung durch Anlage eines ventrikuloperitonealen Shunts durchgeführt werden. Eine offene Kraniotomie zur chirurgischen Entfernung der Zystizerken ist nur selten notwendig. Weiterhin können Glukokortikoide bei Zysten im Subarachnoidalraum oder mit sehr großen Zysten hilfreich sein, um eine Arachnoiditis und Vaskulitis zu reduzieren. Bei längerer Therapiedauer kann Methotrexat verwendet werden.
Bei okulären Manifestationen sollte eine chirurgische Versorgung erfordern. Spinale Läsionen können konservativ oder operativ behandelt werden.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Prävention
Vorgebeugt werden kann einer Verbreitung von Infektionen mit Taenia solium durch eine gründliche Fleischbeschau, bei der die Finnen entdeckt werden. In der EU wird diese Kontrolle streng durchgeführt, was zu einer weitgehenden Elimination geführt hat. Es gibt nur noch kleine Herde in Süd- und Osteuropa.
Zur Prävention einer Zystizerkose muss das Risiko einer Aufnahme von Eiern z.B. über fäkale Verunreinigungen minimiert werden (persönliche Hygienemaßnahmen, adäquate Entsorgung von Fäkalien).
Quellen
- ↑ Holger Mayta et al.: Nested PCR for Specific Diagnosis of Taenia solium Taeniasis J Clin Microbiol. 2008 Jan; 46(1): 286–289. PMCID: PMC2224258
- ↑ Diaz JF et al.: Immunodiagnosis of human cysticercosis (Taenia solium): a field comparison of an antibody-enzyme-linked immunosorbent assay (ELISA), an antigen-ELISA, and an enzyme-linked immunoelectrotransfer blot (EITB) assay in Peru. Am J Trop Med Hyg. 1992 May; 46(5): 610-5.
- ↑ diagnost-x: Affordable Tapeworm Diagnostics abgerufen am 29.11.2017
- ↑ del Brutto OH et al. Revised diagnostic criteria for neurocysticercosis, J Neurol Sci. 2017;372:202-210, abgerufen am 20.07.2020