Valsartan
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsnamen: Cordinate®, Diovan® (protect/forte), Provas®, Valsacor®, div. Generika
Englisch: valsartan
Definition
Valsartan ist ein Antihypertensivum aus der Gruppe der AT1-Rezeptorantagonisten (Sartane), das zur Behandlung von arterieller Hypertonie, Herzinsuffizienz und diabetischer Nephropathie bei Diabetes mellitus Typ 2 eingesetzt wird.
Chemie
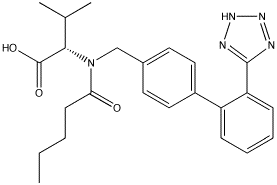
Die genaue chemische Bezeichnung (IUPAC-Name) von Valsartan ist (S)-3-Methyl-2-{N-[2'- (1H-tetrazol-5-yl)biphenyl-4-ylmethyl]pentanamido}butansäure oder (S)-3-Methyl-2-{N-[2'-(2H-tetrazol-5-yl)biphenyl-4-ylmethyl]pentanamido}-buttersäure. Die Summenformel des Stoffes lautet
- C24H29N5O3
Die Molekulare Masse (Molekulargewicht) beträgt: 435,52 g·mol−1
Wirkmechanismus
Valsartan wirkt über die kompetetive und nicht-kompetetive Blockierung der AT1-Rezeptoren, die als Bindungsstelle für das Angiotensin II fungieren.
Durch die hochaffine Blockierung der AT1-Rezeptoren wird die Kontraktilität glatter Muskelzellen gesenkt, was zu einer Senkung des peripheren Gefäßwiderstandes und konsekutiv zur Senkung des Blutdrucks führt. Gleichzeitig wird die Ausschüttung von Aldosteron aus der Nebennierenrinde gemindert.
Valsartan beeinflusst im Gegensatz zu den Antihypertensiva aus der Gruppe der ACE-Hemmer nicht den Abbau von Kininen (v.a. Bradykinin) und der Substanz P, wodurch es zu einer Vermeidung der charakteristischen Nebenwirkungen der ACE-Hemmer (z.B. ACE-Hemmer-Husten) kommt.
Pharmakokinetik
Valsartan wird oral appliziert und erreicht im Körper nach der Resorption im Dünndarm eine Bioverfügbarkeit von ca. 25%.
Valsartan wird zu 30% über die Niere eliminiert und zu 70% in der Leber verstoffwechselt
Die Plasmahalbwertszeit von Valsartan liegt bei 6 bis 9 Stunden.
Toxikologie
Im Tiermodell konnte bei der Ratte eine LD50 von > 2000 mg·kg−1 festgestellt werden.
Anwendungsgebiete
Durch seine antihypertensive Wirkung wird Valsartan vorwiegend in der Behandlung von arterieller Hypertonie eingesetzt, wenn es bei der Gabe der alternativen ACE-Hemmer zu Nebenwirkungen kommt oder diese kontraindiziert sind.
Weitere Einsatzgebiete sind:
- Chronische Herzinsuffizienz
- Diabetische Nephropathie bei Diabetes mellitus Typ 2
- Prophylaxe nach Herzinfarkt
Nebenwirkungen
Valsartan weist als AT1-Antagonist relativ wenige Nebenwirkungen auf, zu den bekannten gehören:
Kontraindikationen
Die Gabe von Valsartan ist kontraindiziert beim Vorliegen folgender Erkrankungen:
Die Gabe von Valsartan in der Schwangerschaft und Stillzeit ist kontraindiziert, da in Tierversuchen tödliche fetale und neonatale Schäden festgestellt werden konnten.
Wechselwirkungen
Die Wirkung von Valsartan wird bei der gleichzeitigen Gabe von Aspirin abgeschwächt.
Forschung
In aktuellen Forschungsansätzen wird die Wirkung von Valsartan in der Therapie und Prophylaxe der Alzheimer-Erkrankung untersucht.
Verordnungshinweis
Valsartan ist verschreibungspflichtig.
Arzneimittelrückrufe
Im Juli 2018 erfolgten in 21 Ländern Europas und in Kanada chargenbezogene Rückrufe zahlreicher valsartanhaltiger Medikamente. Es waren Arzneimittel betroffen, deren Wirkstoff vom chinesischen Hersteller Zhejiang Huahai Pharmaceutical produziert wurde. Der Grund für die Rückrufe war eine dort entstandene Verunreinigung mit N-Nitrosodimethylamin, einem Stoff, der als "wahrscheinlich krebserregend" eingestuft wird.[1][2][3] Bisherige Untersuchungen legen eine Assoziation mit einer geringen Risikoerhöhung für Leberkrebs nahe.[4]
Quellen
- ↑ Common heart drug recalled in 22 countries for possible cancer link CNN am 6. Juli 2018, abgerufen am 9. Juli 2018.
- ↑ Valsartan: chargenbezogener Rückruf valsartanhaltiger Arzneimittel, deren Wirkstoff von dem chinesischen Hersteller Zhejiang Huahai Pharmaceutical produziert wurde Bundesinstitut für Arzneimittel und Medizinprodukte am 5. Juli 2018, abgerufen am 9.Juli 2018.
- ↑ Valsartan: Actavis, Puren und Ratiopharm veröffentlichen weitere Rückrufe Deutsche Apotheker Zeitung online am 9. Juli 2018, abgerufen am 9. Juli 2018.
- ↑ Gomm W et al. N-nitrosodimethylamine-contaminated valsartan and the risk of cancer - a longitudinal cohort study based on German health insurance data. Dtsch Arztebl Int 2021;118: 357-62.






