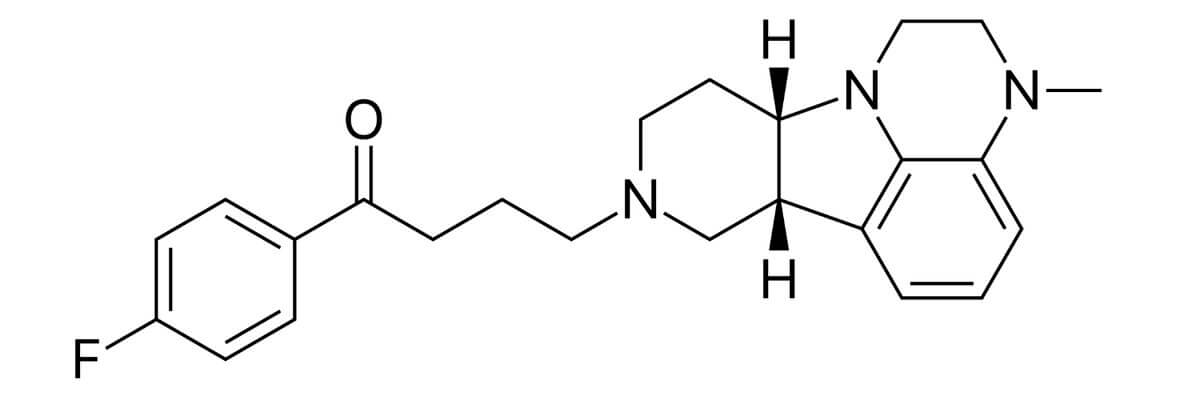
Lumateperon
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenEnglisch: lumateperone
Definition
Lumateperon ist ein atypisches Antipsychotikum der zweiten Generation mit multimodalem Wirkmechanismus. In den USA ist die Substanz für Schizophrenie bei Erwachsenen, bei schweren Depressionen und bei depressiven Episoden im Rahmen einer bipolaren Erkrankung zugelassen. Eine EMA-Zulassung liegt bislang (2026) nicht vor.
Chemie
Die Summenformel lautet C24H28FN3O, die molare Masse beträgt 393,51 g/mol. Der ATC-Code ist N05AD10.
Wirkmechanismus
Der genaue Wirkmechanismus ist nicht abschließend geklärt (2026). Lumateperon wirkt als Antagonist an zentralen 5-HT2A-Rezeptoren und moduliert D2-Rezeptoren. Die D2-Rezeptorbesetzung in klinischen Dosierungen fällt jedoch deutlich geringer aus als bei anderen Antipsychotika. In klinischen Studien zeigte sich eine geringere Rate extrapyramidaler Nebenwirkungen als bei anderen Antipsychotika.
Zusätzlich hemmt Lumateperon den Serotonin-Transporter (SERT) mit schwacher bis moderater Intensität, was mit antidepressiven Effekten und einer Reduktion von Negativsymptomen in Verbindung gebracht wird. Die geringe Affinität für Muskarin- und Histaminrezeptoren soll für die schwächer ausgeprägte Beeinflussung metabolischer Parameter verantwortlich sein.
Pharmakokinetik
Strukturell handelt es sich um ein Pyridopyrroloquinoxalin-Derivat. Die ATC-Einordnung in die Gruppe der Butyrophenon-Derivate (N05AD) erfolgt formal, obwohl Lumateperon strukturell von klassischen Butyrophenonen abweicht.
Lumateperon hat bei oraler Applikation einen ausgeprägten First-pass-Effekt. Die Tmax liegt bei 1–2 Stunden und die Halbwertszeit bei etwa 18 Stunden. Der Metabolismus erfolgt hepatisch über UGT-Isoformen, Aldo-Keto-Reduktasen und CYP-Enzyme. Klinisch relevant ist insbesondere CYP3A4. Lumateperon hemmt in klinisch relevanten Dosen keine wichtigen CYP450-Enzyme und ist kein P-Glykoprotein-Substrat.
Indikationen
Indikationen für die Einnahme von Lumateperon sind:
- Schizophrenie bei Erwachsenen
- Depressive Episoden bei bipolarer Störung Typ I und II, als Monotherapie oder adjunktiv zu Lithium bzw. Valproat
- Adjunktive Therapie der major depressiven Störung in Kombination mit einem oralen Antidepressivum (Zulassung seit November 2025)
Eine EMA-Zulassung besteht für keine dieser Indikationen.
Darreichungsformen
Hartkapseln zu 42 mg, 21 mg und 10,5 mg Lumateperon.
Dosierung
Die empfohlene Dosierung von Lumateperon beträgt 42 mg einmal täglich oral, ohne Titrationsbedarf, unabhängig von den Mahlzeiten. Eine Dosisreduktion ist bei gleichzeitiger Gabe von moderaten CYP3A4-Inhibitoren (z.B. Verapamil) oder Leberinsuffizienz Child-Pugh B/C erforderlich. Eine weitere Reduktion ist bei starken CYP3A4-Inhibitoren (z.B. Ketoconazol) notwendig.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Nebenwirkungen
Warnhinweise
- Erhöhte Mortalität bei älteren Patienten mit Demenz-assoziierter Psychose (nicht zugelassene Indikation).
- Erhöhtes Suizidalitätsrisiko unter antidepressiver Therapie bei Minderjährigen (für diese Altersgruppe nicht zugelassen).
Wechselwirkungen
CYP3A4 ist der klinisch relevanteste Interaktionspfad. Starke Induktoren (z.B. Carbamazepin, Rifampicin, Johanniskraut) sollten vermieden werden. UGT-Inhibitoren sind potenziell relevant. Alkohol und Sedativa verstärken die sedierende Wirkung.
Kontraindikationen
- Überempfindlichkeit gegenüber Lumateperon oder Hilfsstoffen.
- Drittes Schwangerschaftstrimenon: Risiko für neonatale extrapyramidale Symptome und Entzugssyndrome.
- Stillen: Übergang in die Muttermilch nachgewiesen, daher nicht empfohlen.
- Pädiatrie: Sicherheit und Wirksamkeit unter 18 Jahren nicht belegt.
Verordnungshinweis
In den USA ist Lumateperon verschreibungspflichtig. In Deutschland und der EU ist der Wirkstoff derzeit (2026) mangels EMA-Zulassung nicht regulär verordnungsfähig.
Quellen
- Correll et al. Efficacy and Safety of Lumateperone for Treatment of Schizophrenia: A Randomized Clinical Trial, 2020
- Calabrese et al. Efficacy and Safety of Lumateperone for Major Depressive Episodes Associated With Bipolar I or Bipolar II Disorder, 2021
- Sowa-Kućma et al., Exploring the Pharmacological and Clinical Features of Lumateperone, 2024
- FDA. Prescribing Information Caplyta (lumateperone), aktualisierte Fassung 11/2025.
- Johnson & Johnson. FDA approval of CAPLYTA for MDD. Pressemitteilung, 6. November 2025.
- Drugs.com. Lumateperone (Monograph).