Dostarlimab
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsname: Jemperli®
Definition
Dostarlimab ist ein monoklonaler Antikörper aus der Gruppe der Checkpoint-Inhibitoren. Er wird zur Therapie des rezidivierten oder fortgeschrittenen Endometriumkarzinoms eingesetzt.
Biochemie
Dostarlimab ist ein humanisierter monoklonaler Antikörper des Isotyps IgG4 mit einer molekularen Masse von rund 144 kDa. Es handelt sich um ein glycosyliertes Homodimer, das aus je zwei identischen schweren γ-Ketten und leichten κ-Ketten besteht, die über Disulfidbrücken verbunden sind. Der Wirkstoff wird in gentechnisch veränderten Ovarialzellen des Chinesischen Zwerghamsters (CHO-Zellen) produziert.
Wirkmechanismus
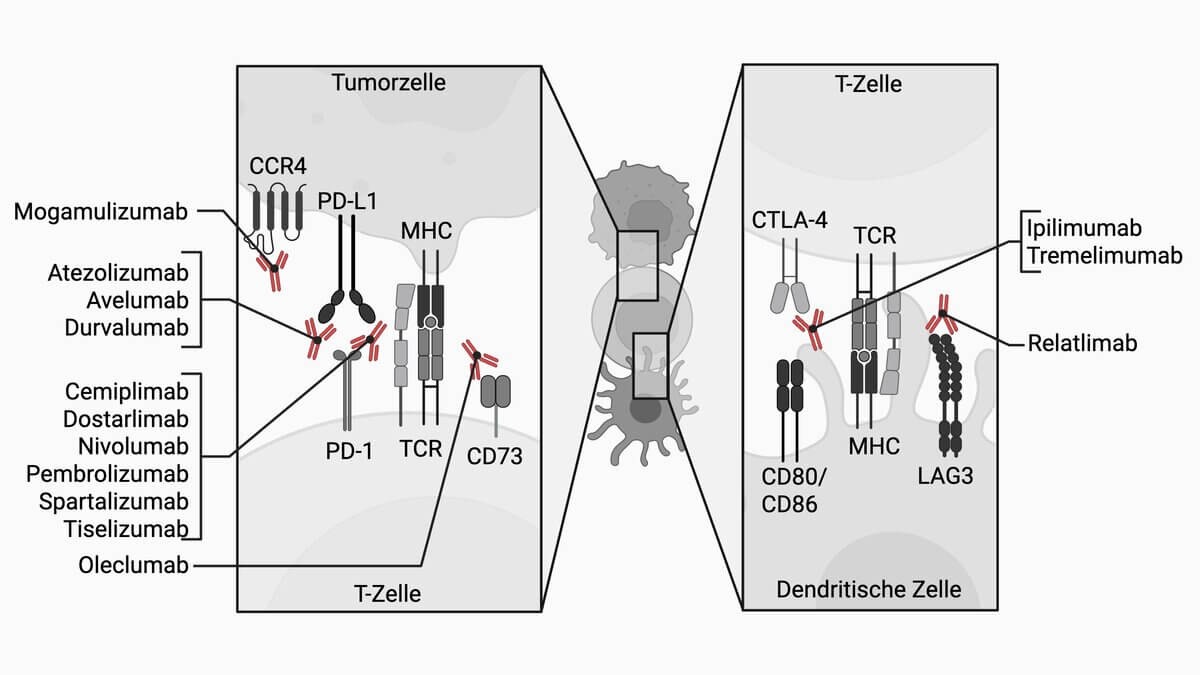
Die antineoplastische Wirkung von Dostarlimab basiert auf der Bindung an den PD-1-Rezeptor. Dadurch wird dessen Interaktion mit den Liganden PD-L1 und PD-L2 blockiert und eine Hemmung der T-Zell-Funktion auf dem PD-1-Signalweg verhindert. Dostarlimab verstärkt so typische T-Zell-Aufgaben wie die Produktion von Zytokinen und die zytotoxische Aktivität. Durch die gesteigerte Immunantwort des Körpers auf das Tumorgewebe kommt es im Effekt zu einem verminderten Tumorwachstum.
Indikation
Dostarlimab ist zugelassen:[1]
- Monotherapie zur Behandlung von erwachsenen Patientinnen mit rezidivierendem oder fortgeschrittenem Endometriumkarzinom mit Mismatch-Reparatur-Defizienz (dMMR) bzw. hoher Mikrosatelliteninstabilität (MSI-H), das während oder nach einer vorherigen Behandlung mit einer Platin-basierten Therapie progredient ist
- als Kombinationstherapie mit Carboplatin und Paclitaxel zur Erstlinienbehandlung von erwachsenen Patienten mit primär fortgeschrittenem oder rezidivierendem Endometriumkarzinom, für die eine systemische Therapie infrage kommt
Off-label-Einsatz
In einer kleinen klinischen Studie mit 12 therapienaiven Patienten wurde Dostarlimab zur Therapie des kolorektalen Karzinoms mit Mismatch-Reparatur-Defizienz eingesetzt. Es konnte in allen Fällen eine vollständige Remission erreicht werden.[2]
Dosierung
Die empfohlene Dosis in Kombination mit Carboplatin und Paclitaxel beträgt 500 mg Dostarlimab alle 3 Wochen für 6 Zyklen, gefolgt von 1.000 mg alle 6 Wochen als Monotherapie für alle nachfolgenden Zyklen.
Bei primärer Monotherapie beträgt die empfohlene Dosis 500 mg Dostarlimab alle 3 Wochen für 4 Zyklen, gefolgt von 1.000 mg alle 6 Wochen für alle nachfolgenden Zyklen.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Anwendungshinweise
Die Applikation erfolgt mittels einer intravenösen Infusionspumpe über einen Zeitraum von mindestens 30 Minuten. Das Mittel darf nicht als schnelle intravenöse Infusion oder als Bolusinjektion verabreicht werden.
Nebenwirkungen
Dostarlimab führt zu einer Veränderung der immunologischen Eigentoleranz. Entsprechend kann der Wirkstoff Entzündungsreaktionen in verschiedenen Organsystemen triggern. Häufige (≥ 1/100 bis < 1/10) oder sehr häufige (≥ 1/10) Nebenwirkungen von Dostarlimab sind:
Wechselwirkungen
Es wurden keine Studien zur Untersuchung von Wechselwirkungen durchgeführt. Da monoklonale Antikörper keine Substrate des Cytochrom-P450-Systems sind und nicht von Wirkstoff-Transportern erfasst werden, sind Interaktionen mit kleinmolekularen Wirkstoffen nicht zu erwarten.
Kontraindikationen
- Überempfindlichkeit gegen den Wirkstoff
Nutzenbewertung
Auf der Basis der vom IQWiG ausgewerteten Studiendaten wurde der Zusatznutzen von Dostarlimab vom G-BA wie folgt eingeordnet (Stand 2021):[3]
- Ein Zusatznutzen ist nicht belegt.
Der Kombinationstherapie von Dostarlimab mit Carboplatin und Paclitaxel bei neu aufgetretenem Endometriumkarzinom mit Mikrosatelliteninstabilität wurde vom G-BA ein erheblicher Zusatznutzen attestiert. (Stand 2025).[4]
Therapiekosten
Die Jahrestherapiekosten pro Fall liegen bei rund 100.000 €.
Quellen
- ↑ Fa. GSK: Fachinformation Dostarlimab (Jemperli), zuletzt abgerufen am 29.08.2025
- ↑ Andrea Cercek et al.: PD-1 Blockade in Mismatch Repair–Deficient, Locally Advanced Rectal Cancer. New England Journal of Medicine June 5, 2022 DOI: 10.1056/NEJMoa2201445
- ↑ Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie: Anlage XII – Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach § 35a SGB V Dostarlimab (Endometriumkarzinom, nach vorheriger Platin-basierter Therapie) vom 2. Dezember 2021
- ↑ Website Gemeinsamer Bundesauschuss: Gebärmutterschleimhautkrebs. G-BA attestiert Immuntherapie erheblichen Zusatznutzen in neuem Anwendungsgebiet. Zuletzt abgerufen am 29.08.2025