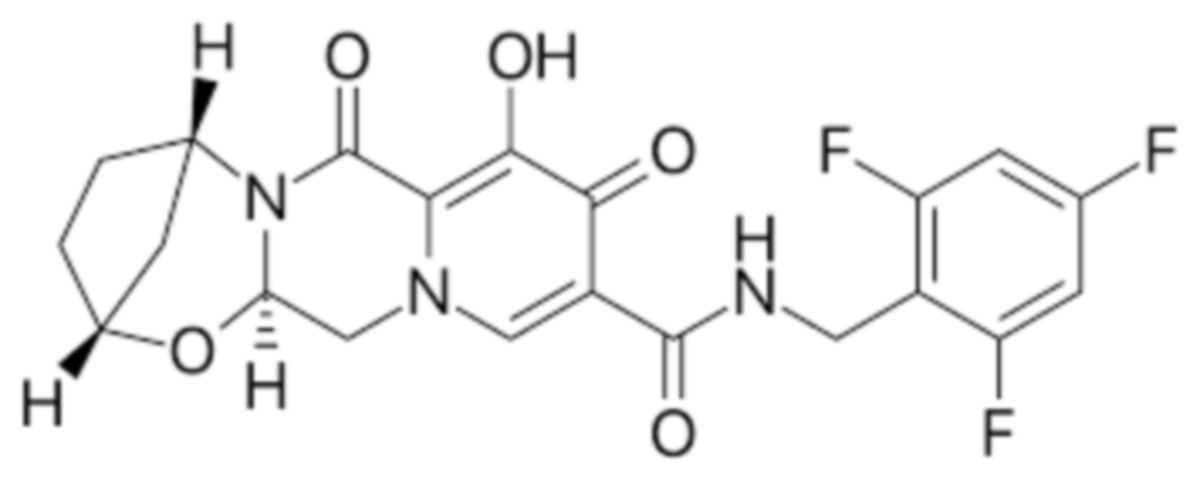
Bictegravir
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsname: Biktarvy®
Definition
Bictegravir ist ein Integrase-Inhibitor aus der Klasse der Virostatika. Der Arzneistoff wird zur Therapie von HIV-Infektionen eingesetzt.[1]
Chemie
Hintergrund
Zur Vermeidung von Resistenzen werden für die initiale HIV-Therapie immer mehrere Wirkstoffe aus verschiedenen Wirkstoffklassen kombiniert. Um die Adhärenz zu erhöhen, sollen laut der deutsch-österreichischen Leitlinie zur antiretroviralen Therapie bevorzugt Fixkombinationen eingesetzt werden.
Bictegravir ist derzeit nur als Bestandteil einer fixen Dreierkombination mit dem Nukleosidischen Reverse-Transkriptase-Inhibitor Emtricitabin und dem Reverse-Transkriptase-Inhibitor Tenofovir erhältlich.[1]
Wirkmechanismus
Bictegravir bindet an das aktive Zentrum der viralen Integrase. Dieses HIV-eigene Enzym katalysiert den Einbau des retroviralen Genoms in die Wirtszelle. Hier greift der Wirkstoff ein und verhindert den Stangtransfer und die DNA-Integration des HI-Virus, wodurch die damit einhergehende Replikation ausbleibt.[2]
Pharmakokinetik
Maximale Plasmaspiegel werden etwa 2 bis 4 Stunden nach oraler Einnahme der Fixkombination erreicht. Bictegravir wird hauptsächlich über die Leber ausgeschieden. Die Eliminationshalbwertszeit liegt bei 17,3 Stunden.[2]
Indikation
- Kombinationstherapie mit Emtricitabin und Tenofovir bei erwachsenen Patienten, die mit dem HI-Virus infiziert sind [2]
Dosierung
Die tägliche Dosis beträgt 50 mg Bictegravir, 200 mg Emtricitabin und 25 mg Tenofovir in Form einer Filmtablette.[2]
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Nebenwirkungen
Folgende Nebenwirkungen traten in den zulassungsrelevanten klinischen Studien häufig (≥ 1:100) auf:[2]
Wechselwirkungen
Bictegravir wird primär über CYP3A4 und UGT1A1 metabolisiert. Die Plasmaspiegel können durch Induktoren oder Inhibitoren dieser Enzyme beeinflusst werden. Um eine Komplexbildung zu vermeiden, darf der Arzneistoff nicht gleichzeitig mit magnesium- oder aluminiumhaltigen Antazida eingenommen werden.[2]
Kontraindikationen
- Überempfindlichkeit gegenüber dem Wirkstoff
- gleichzeitige Anwendung von Rifampicin, Johanniskraut und anderen CYP34A-Induktoren[2]
Nutzenbewertung
Ein Zusatznutzen einer Therapie mit Bictegravir wird vom G-BA auf der Basis der vom IQWiG ausgewerteten Studienergebnisse wie folgt eingeordnet:[3]
- nicht belegter Zusatznutzen gegenüber einer zweckmäßigen Vergleichstherapie mit Rilpivirin oder Dolutegravir jeweils in Kombination mit 2 Nukleosid-/Nukleotidanaloga
Kosten
Die Jahrestherapiekosten betragen pro Patient rund 11.000 €.[3]
Quellen
- ↑ 1,0 1,1 Pharmazeutische Zeitung Online Arzneistoffe | Bictegravir abgerufen am 23.11.18
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 Fachinformation Bictegravir Biktarvy® 50 mg/200 mg/25 mg Filmtabletten abgerufen am 23.11.18
- ↑ 3,0 3,1 3,2 IQWIg-Berichte-Nr. 670 Bictegravir/Emtricitabin/Tenofoviralafenamid (HIV-Infektion) Nutzenbewertung gemäß § 35a SGB V abgerufen am 23.11.2018