Proteinstruktur
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: Proteinkonformation
Englisch: protein structure
Definition
Unter Proteinstruktur versteht man in der Biochemie verschiedene Strukturebenen von Proteinen bzw. Peptiden. Man teilt diese Strukturen hierarchisch auf in eine Primärstruktur (Aminosäuresequenz), Sekundärstruktur, Tertiärstruktur und Quartärstruktur. Wird ein Protein in Bezug auf die räumliche Anordnung erwähnt, spricht man auch oft vom Begriff Proteinkonformation. Daraus resultiert auch der Begriff Konformationsänderung, der eine Änderung der räumlichen Proteinstruktur bedeutet.
Hintergrund
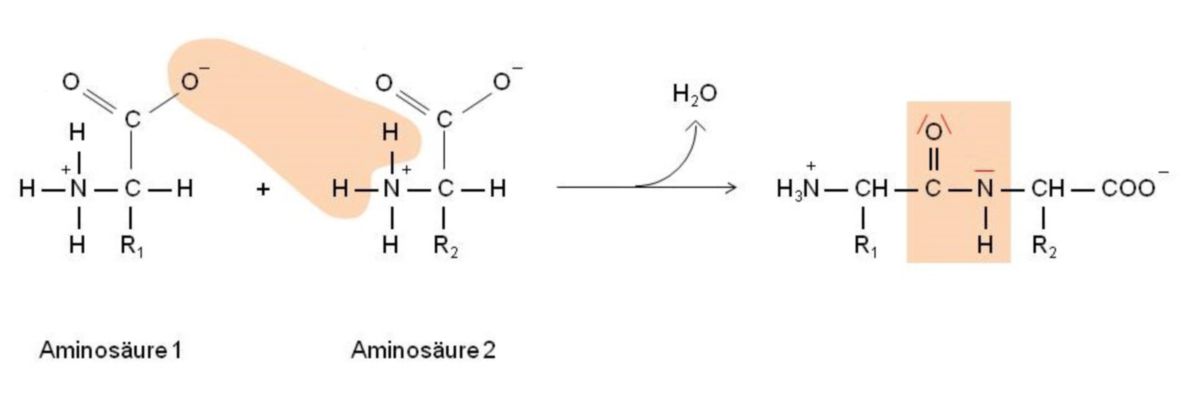
Grundlage für die Anordnung von Proteinen ist die Peptidbindung. Sie ist die Bindungsart, die Aminosäuren in der Regel immer auf die gleiche Weise miteinander verbindet. In Zellen werden Peptidbindungen normalerweise unter Vermittlung von Ribosomen gebildet. Eine Peptidbindung ist die Verbindung zwischen der Carboxylgruppe einer Aminosäure und der Aminogruppe einer anderen Aminosäure unter Abspaltung von Wasser (Kondensation).
Das Stickstoffatom trägt ein freies Elektronenpaar, das unter dem elektronenziehenden Einfluss des Sauerstoffatoms steht (auf Grund der hohen Elektronegativität des Sauerstoffs). Somit zieht der Sauerstoff das freie Elektronenpaar zu einem gewissen Teil in die Bindung zwischen Stickstoff- und Kohlenstoffatom hinein. Die Peptidbindung erhält dadurch einen partiellen Doppelbindungscharakter. Das bewirkt eine Aufhebung der freien Drehbarkeit der C=O-Gruppe und der NH-Gruppe.
Das Sauerstoff- und Wasserstoffatom der Peptidbindung spielen bei der Strukturbildung aller Peptide und Proteine eine wichtige Rolle. Moleküle können sich so aneinander anlagern, dass sämtliche Peptidbindungen zweier Aminosäurenketten direkt gegenüberliegen. Die Wasserstoffatome der Peptidbindungen sind im Vergleich zu den Sauerstoffatomen gegenüberliegender Peptidbindungen vergleichsweise positiv polarisiert. Resultat ist die Ausbildung sog. Wasserstoffbrücken, die beide Aminosäureketten miteinander verbinden.
Basics
Unter der nativen Struktur eines Proteins versteht man die definierte dreidimensionale Struktur, in der das Protein seine physiologische Funktion ausübt. Aminosäuren, die in kleinen Peptiden enthalten sind, können untereinander nur wenige Wechselwirkungen eingehen. Sie bilden deshalb im Gegensatz zu den Proteinen in der Regel keine stabilen Strukturen aus. Solange ein vorliegendes Protein seine native Struktur noch nicht eingenommen hat, liegt es in einer nicht-nativen Struktur vor. Verliert ein Protein seine native Struktur, ist es denaturiert.
In den Zellen können denaturierte Proteine nur teilweise wieder in den nativen Zustand zurückversetzt werden. Meist ist eine abgelaufene Denaturierung irreversibel. Funktionell unbrauchbare Proteine werden anschließend von Proteasen hydrolysiert. Aus den daraus freigesetzten Aminosäuren werden wieder neue Polypeptide synthetisiert.
Der Begriff Proteindomäne bezeichnet einen größeren Teil einer Aminosäurekette, der unabhängig von den anderen Proteinanteilen eine eigene dreidimensionale Struktur ausbildet. In der Regel bilden derartige Proteindomänen im menschlichen Körper auch funktionelle Einheiten des Proteins.
Einteilung
Primärstruktur
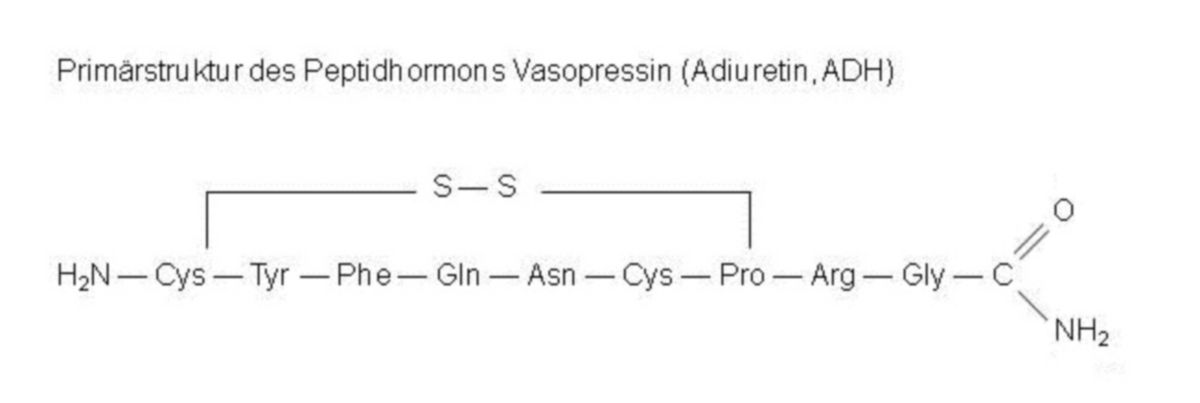
Der Begriff Primärstruktur beschreibt die lineare Anordnung der Aminosäuren in einem Protein, die Aminosäuresequenz. Die Primärstruktur allein reicht nicht aus, um die Proteinfunktion zu gewährleisten. Dazu sind Proteinfaltungen erforderlich, die Sekundär-, Tertiär- und Quartärstrukturen bilden.
Bildet man eine Aminosäuresequenz ab, stellt man die freie Aminogruppe der ersten Aminosäure konventionsgemäß auf die linke Seite, die freie Carboxylgruppe der letzten Aminosäure rechts dar. Dementsprechend unterscheidet man auch zwischen einem N-terminalen und einem C-terminalen Ende. Beim Menschen beginnt die Proteinbiosynthese an der N-terminalen Aminosäure.
Sekundärstruktur
Regelmäßige Strukturen innerhalb von Polypeptiden, die sich aufgrund von ausgebildeten Wasserstoffbrücken zwischen Peptidbindungen aneinanderheften, werden als Sekundärstruktur bezeichnet. Typische Sekundärstrukturelemente sind:
- α-Helix: Es handelt sich um eine rechtsgängige Schraube, bei der jeweils 3,6 Aminosäuren eine Windung formen. Jede Windung hat eine Ganghöhe von 0,54 nm und wird durch intramolekulare Wasserstoffbrücken stabilisiert.
- β-Faltblatt: Hier lagern sich Aminosäurenketten weitgehend in gestreckter Konformation nebeneinander und bilden so ein Beta-Faltblatt aus. Die einzelnen Faltblattstrukturen werden durch Wasserstoffbrücken stabilisiert, die sich zwischen zwei parallel oder antiparallel liegenden Aminosäureketten ausbilden.
- U-förmige Verbindungsstücke (engl. loop bzw. turn, deutsch: Schleife): Solche Schleifen sind U-förmige Abschnitte der Aminosäurekette, welche die α-Helices und β-Faltblattstrukturen eines Proteins miteinander verbinden. Ein Beispiel ist die β-Schleife.
Seltenere Sekundärstrukturen sind die 310-Helix und die π-Helix.
Tertiärstruktur
Die Tertiärstruktur beschreibt die dreidimensionale Struktur einer kompletten Aminosäurekette, einschließlich der Anordnung sämtlicher Aminosäurereste. Sie wird nicht nur durch Wasserstoffbrückenbindungen, sondern durch verschiedene Wechselwirkungen der Aminosäurereste stabilisiert. Die Kräfte, die an der Stabilisierung einer Tertiärstruktur beteiligt sind, werden durch die funktionellen Gruppen der verschiedenen Aminosäuren erzeugt. Zu ihnen zählen:
Einige Proteine liegen nicht in Form einer definierten Tertiärstruktur vor. In diesem Fall spricht man von intrinsisch ungeordneten Proteinen (IDP).
Quartärstruktur
Die Quartärstruktur entsteht durch Zusammenlagerung verschiedener Aminosäureketten in Tertiärstruktur zu einem Proteinkomplex. Die einzelnen Untereinheiten werden als Protomere bezeichnet, das gesamte funktionelle Protein als Oligomer.
Proteinfaltung
Die Proteinfaltung, mit der die dreidimensionale Struktur eines Proteins erreicht wird, erfolgt teilweise spontan (während der Translation), teilweise durch die Mitwirkung von Enzymen oder Chaperonen. Liganden beeinflussen ebenfalls die Proteinstruktur, so dass manche Proteine - je nach Komplexierung mit Cofaktoren oder Substraten - verschiedene Formen einnehmen können (Konformationsänderung). Die Fähigkeit, die Raumstruktur zu verändern, ist für viele Enzymaktivitäten wichtig.
Strukturbestimmung
Um herauszufinden, welche räumliche Proteinstruktur gegeben ist, werden verschiedenste experimentelle Methoden zur Hand genommen, u.a.:
- Die Kristallstrukturanalyse erstellt meist mittels Röntgenstrahlen das Beugungsbild eines Proteinkristalls, woraus man dessen dreidimensionale Struktur errechnen kann
- Die NMR-Spektroskopie ermöglicht die Bestimmung der Proteinstruktur in Lösung und kommt damit physiologischen Bedingungen näher als kristallographische Verfahren. Aufgrund der intrinsischen Dynamik von Proteinen ergibt sich jedoch keine einzelne, starre Struktur, sondern ein Ensemble konformationsverwandter Strukturen. Zur Beschreibung der Proteinstruktur wird daher üblicherweise ein Satz berechneter Modelle dargestellt, aus denen sich die wahrscheinlichsten Konformationen ableiten lassen.
Die Proteinstruktur ist von physikochemischen Randbedingungen wie pH-Wert, Temperatur, Salzgehalt, Gegenwart anderer Proteine etc. abhängig. Über eine Native-PAGE, eine Größenausschlusschromatographie oder über eine isopyknische Zentrifugation kann der Stokes-Radius eines nativen Proteins ermittelt werden. Beide Methoden können mit einer Quervernetzung oder mit einem Alaninscan kombiniert werden.
Strukturvorhersage
Gibt es bereits Proteine, die eine ähnliche Sequenz und eine bekannte Struktur aufweisen, kann man bei der Vorhersage räumlicher Proteinstrukturen (Proteinstrukturvorhersage) sehr gute Ergebnisse erzielen. Ermöglicht wird dies durch das sogenannte homology modelling. Hierbei wird die neue Sequenz auf die Sequenz, dessen Struktur schon bekannt ist, abgebildet und damit in die Struktur quasi "eingepasst, eingefügt". Dieses Verfahren ähnelt stark dem Sequenzalignment.
In den letzten Jahren haben sich neben den traditionellen Verfahren spezialisierte Deep-Learning-Modelle etabliert, welche die Strukturvorhersage revolutioniert haben, z.B. Alpha-Fold.
Klinik
Liegt eine Störung bei der Bildung einer funktionsfähigen Raumstruktur vor, kann eine Proteinfaltungserkrankung entstehen. Ein Beispiel dafür ist Chorea Huntington. Auch Prionkrankheiten wie BSE oder Morbus Alzheimer werden durch Fehlbildungen der Proteinstruktur ausgelöst.