Sorafenib
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsname: Nexavar®
Englisch: Sorafenib
Definition
Sorafenib ist ein oral anwendbarer Arzneistoff aus der Klasse der Proteinkinaseinhibitoren, der zu den Multikinase-Inhibitoren zählt, da er verschiedene Kinasen hemmt. Er wird u.a. zur Behandlung fortgeschrittener Nieren- und Leberzellkarzinome eingesetzt.
Chemie
Sorafenib ist eine polyzyklische organische Verbindung mit der Summenformel C21H16ClF3N4O3. Ihr Molekulargewicht beträgt rund 464,8 g/mol.
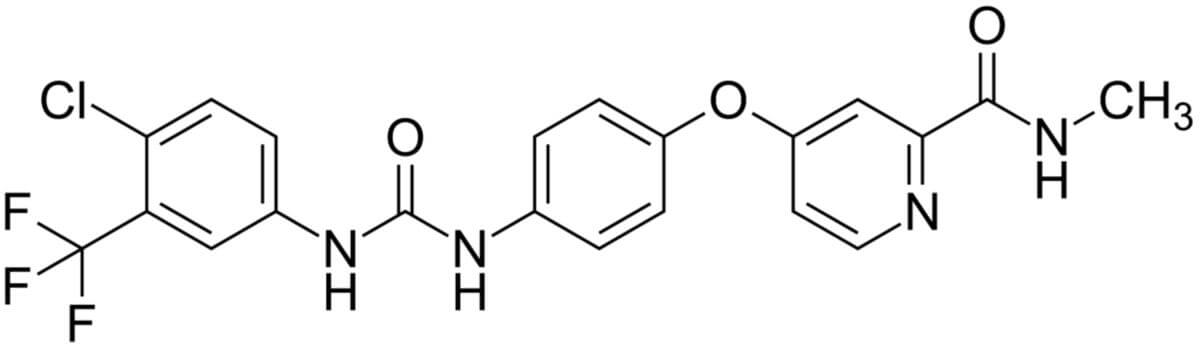
Strukturformel
Wirkmechanismus
Sorafenib stoppt die vermehrte Zellteilung und unterbindet die Blutversorgung des Tumors. Die Substanz soll über einen dualen Wirkmechanismus verfügen:
- Sorafenib unterbricht den Signalweg, der die Tumorzelle zu fortgesetzter Teilung anregt. Genauer Angriffspunkt ist die RAF-Kinase, die von Sorafenib gehemmt wird. Diese Kinase aktiviert eine Kaskade von Enzymen, die letztendlich im Zellkern die Zellteilung auslöst.
- Sorafenib hemmt die Angioneogenese des Tumors, indem die intrazelluläre Tyrosinkinasedomäne des VEGF-Rezeptors blockiert wird. Neu gebildete Tumorzellen werden nicht mehr an das Gefäßsystem angeschlossen, und daher nicht mit Nährstoffen versorgt.
Indikationen
- Leberzellkarzinom (HCC): Behandlung von Patienten, welche sich in einem fortgeschrittenen Tumorstadium befinden und bei denen weder eine Resektion, noch eine Transplantation in Frage kommt.
- Nierenzellkarzinom (RCC): Behandlung von Patienten mit fortgeschrittenem Nierenzellkarzinom, bei denen eine vorherige Interferon-alpha- oder Interleukin-2-basierte Therapie versagt hat oder die für diese Therapie nicht geeignet sind.
- Differenziertes Schilddrüsenkarzinom (DTC): Behandlung von Patienten mit progressivem, lokal fortgeschrittenem oder metastasiertem, differenziertem Schilddrüsenkarzinom, das gegenüber einer Radiojodtherapie refraktär ist.
- Akute myeloische Leukämie bei Nachweis einer FLT3-Mutation
Dosierung
Die empfohlene Dosis von Sorafenib bei Erwachsenen ist 400 mg (2 Tabletten à 200 mg) 2 x täglich - entsprechend einer Tagesgesamtdosis von 800 mg.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Nebenwirkungen
Neben vermehrten Diarrhoen ist die häufigste unerwünschte Nebenwirkung eine Hautreaktion, die vor allem Hände und Füße betrifft und meist in den ersten 6 Wochen der Einnahme auftritt (sog. Hand-Fuß-Syndrom). Ebenfalls ist in der Frühphase der Behandlung eine leichte Hypertonie beschrieben worden. Bei der Einnahme von Sorafenib besteht ein erhöhtes Blutungsrisiko, weshalb eine simultane orale Antikoagulation eventuell kontraindiziert sein kann.
Wechselwirkungen
Die gleichzeitige Gabe von CYP3A4-Induktoren (z.B. Rifampicin, Johanniskraut, Phenytoin, Carbamazepin, Phenobarbital oder Dexamethason) kann zu einer verminderten Aktivität von Sorafenib führen.
Sorafenib hemmt die Glucuronidierung durch UGT1A1 und UGT1A9. Bei der gleichzeitigen Gabe von Sorafenib mit Arzneimitteln, die über diesen Stoffwechselweg metabolisiert werden (z.B. Irinotecan) ist Vorsicht geboten.
Nutzenbewertung
Sorafenib wurde in Europa als Orphan Drug zugelassen. Nach § 35a SGB V gilt damit der medizinische Zusatznutzen bereits durch die Zulassung als belegt.
Kosten
Die Jahrestherapiekosten einer Behandlung mit Sorafenib liegen bei rund 60.000 €.[1]
Quellen
- ↑ Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII – Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach § 35a SGB V – Axitinib (Ablauf der Befristung) BAnz AT 19.10.2017 B2