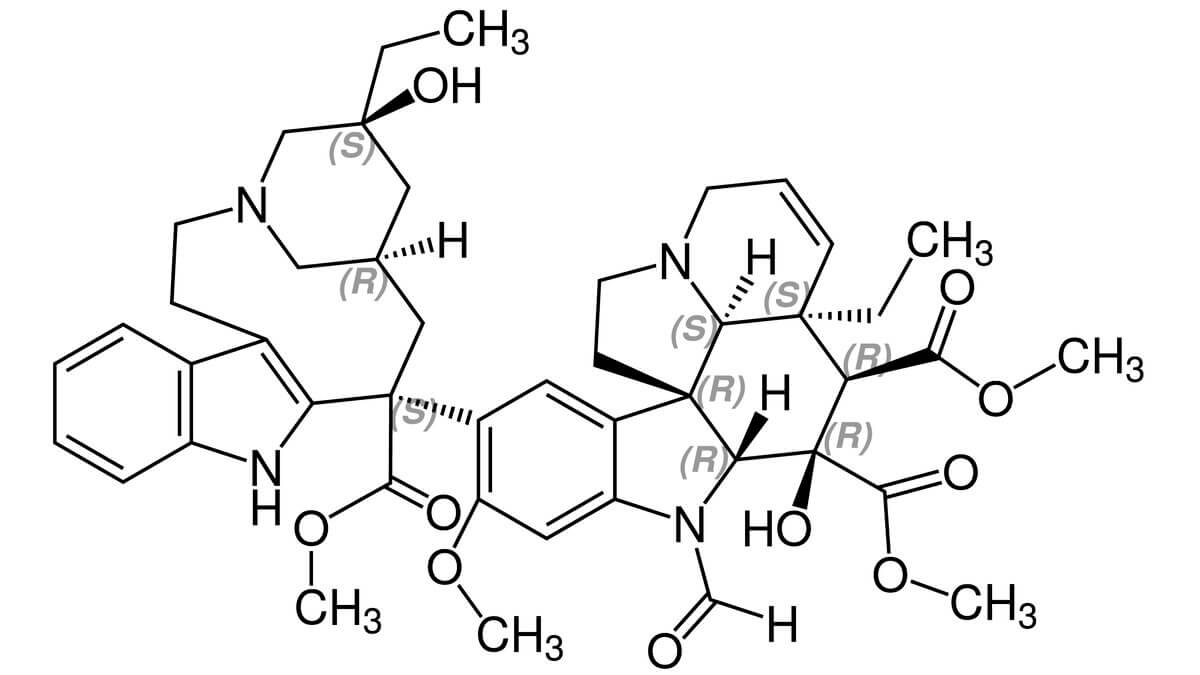
Vincristin
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonyme: Vincristinum, Vincristinsulfat, Leurocristin, Vincristini sulfas PhEur
Handelsname: Oncovin®
Englisch: vincristine
Definition
Vincristin ist ein Zytostatikum aus der Gruppe der Vincaalkaloide. Der Mitosehemmstoff wird überwiegend als Bestandteil standardisierter Chemotherapie-Kombinationsprotokolle bei hämatologischen Neoplasien und ausgewählten soliden Tumoren eingesetzt. Klinisch ist Vincristin vor allem durch seine neurotoxische, dosislimitierende Wirkung charakterisiert.
Geschichte
Die Vincaalkaloide wurden im 20. Jahrhundert aus dem Madagaskar-Immergrün (Catharanthus roseus) entwickelt. Vincristin wurde 1961 erstmals aus der rosafarbenen Catharanthe (Catharanthus roseus) isoliert und in den frühen 1960er-Jahren in die klinische Onkologie eingeführt.
Chemie
Vincristin ist ein bisindolisches Alkaloid pflanzlichen Ursprungs und gehört chemisch zu den halbsynthetischen Vincaalkaloiden. In Arzneimitteln liegt es in der Regel als Sulfat vor. Die Summenformel von Vincristinsulfat lautet C46H56N4O10·H2SO4, die molare Masse beträgt 923,04 g/mol.
Wirkmechanismus
Wie alle Vincaalkaloide bindet Vincristin an Tubulin und hemmt die Polymerisation sowie die Dynamik der Mikrotubuli. Dadurch wird die Ausbildung des mitotischen Spindelapparats gestört, sodass es während der Mitose zu einem Arrest in der Metaphase kommt.
Durch die gestörte Spindelfunktion wird die geordnete Trennung der Chromosomen auf die Tochterzellen verhindert. Dies hemmt vor allem die Proliferation rasch teilender Zellen, weshalb Vincristin primär Tumorzellen schädigt.
Darüber hinaus beeinträchtigt Vincristin auch die Funktion axonaler Mikrotubuli und damit den intrazellulären Transport in Neuronen. Dies ist wesentlich für die typische neurotoxische Wirkung des Arzneistoffs und erklärt insbesondere die Chemotherapie-induzierte periphere Neuropathie sowie autonome neurologische Nebenwirkungen.
Pharmakokinetik
Vincristin wird nach intravenöser Injektion rasch verteilt und zeigt einen triphasischen Abfall der Serumkonzentration. In der Fachinformation werden initiale, intermediäre und terminale Halbwertszeiten von etwa 5 Minuten, 2,3 Stunden und 85 Stunden angegeben. Die terminale Halbwertszeit kann interindividuell stark schwanken. Vincristin ist Substrat von P-Glykoprotein, wodurch die Penetration in das zentrale Nervensystem begrenzt ist.
Der Wirkstoff wird überwiegend hepatisch metabolisiert, insbesondere über CYP3A-Isoenzyme, und vor allem biliär bzw. fäkal eliminiert. Bei eingeschränkter Leberfunktion steigt das Risiko einer Kumulation und Toxizität.
Indikation
Vincristin wird in der Regel nicht als Monotherapie, sondern im Rahmen tumorspezifischer Kombinationsprotokolle eingesetzt. Schwerpunkt der Anwendung sind lymphoproliferative Erkrankungen, insbesondere akute lymphatische Leukämien (ALL) sowie Hodgkin- und Non-Hodgkin-Lymphome. Weitere wichtige zugelassene bzw. etablierte Indikationen sind unter anderem:
- Neuroblastom
- Rhabdomyosarkom
- Ewing-Sarkom
- Nephroblastom
- Wilms-Tumor
- Retinoblastom
- Multiples Myelom
- metastasiertes Mammakarzinom
- kleinzelliges Bronchialkarzinom
- Immunthrombozytopenie (ITP) nach Versagen anderer Therapien.
Darreichungsformen
Vincristin ist als Injektionslösung bzw. Injektions-/Infusionslösung zur ausschließlich intravenösen Anwendung verfügbar. In Deutschland sind bzw. waren insbesondere Durchstechflaschen mit 1 ml, 2 ml und 5 ml bei einer Konzentration von 1 mg/ml verfügbar.
Dosierung
Vincristin darf nur unter Aufsicht in der Anwendung zytotoxischer Arzneimittel erfahrener Ärzte gegeben werden. Die Dosierung erfolgt protokollabhängig. Typische Dosierungen sind:
- Erwachsene: 1,4 mg/m² Körperoberfläche i.v. einmal wöchentlich, meist mit einer Maximaldosis von 2 mg pro Gabe
- Kinder: meist 1,5 bis 2,0 mg/m² i.v. einmal wöchentlich
- Kleinkinder mit geringem Körpergewicht: in einzelnen Fachinformationen initial 0,05 mg/kg.
Bei erhöhtem direktem Serumbilirubin bzw. relevanter Leberfunktionsstörung ist eine Dosisreduktion erforderlich. Bei einem direkten Bilirubinwert über 3 mg/dl wird in Fachinformationen in der Regel initial eine 50%ige Dosisreduktion empfohlen.
Vincristin darf ausschließlich intravenös verabreicht werden. Eine intrathekale Applikation ist kontraindiziert und in aller Regel tödlich.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Nebenwirkungen
Dosislimitierend ist vor allem die Neurotoxizität. Zu den wichtigsten unerwünschten Wirkungen zählen:
- Chemotherapie-induzierte periphere Neuropathie (CIPN) mit Parästhesien, Dysästhesien, neuropathischen Schmerzen, distaler Schwäche und Gangstörung
- autonome Neuropathie mit Obstipation, abdominellen Koliken, Harnverhalt und paralytischem Ileus
- Hirnnervenlähmungen und okulomotorische Störungen
- Atrophie des Nervus opticus
- Syndrom der inadäquaten ADH-Sekretion (SIADH) mit Hyponatriämie
- Alopezie
- Hautausschläge
- Ödeme
- Gliederschmerzen, Myalgien
- Polyurie
- Hypertonie
- seltener myelosuppressive Effekte wie Leukopenie, Anämie oder Thrombozytopenie
- anaphylaktischer Schock (selten)
Neurologische Symptome können nach Therapieende zunächst andauern oder sich weiter verschlechtern. Dieses Fortbestehen oder Nachschwingen wird als Coasting-Phänomen beschrieben. Die neurologischen Ausfallserscheinungen können dann unter Umständen irreversibel sein.
Bei Extravasation kommt es zu einer lokalen Gewebeschädigung.
Wechselwirkungen
Klinisch besonders relevant sind Wechselwirkungen über CYP3A und P-Glykoprotein. Starke CYP3A-Inhibitoren können die Exposition gegenüber Vincristin erhöhen und schwere Toxizitäten begünstigen. Besonders bedeutsam sind Azol-Antimykotika wie Itraconazol, Voriconazol und Posaconazol, unter denen vermehrt Neurotoxizität, Ileus und SIADH beobachtet wurden. Auch weitere neurotoxische Begleitmedikationen können das Nebenwirkungsprofil ungünstig beeinflussen.
Kontraindikationen
Wichtige Kontraindikationen sind:
- Überempfindlichkeit gegen Vincristin oder andere Bestandteile des Präparats
- intrathekale Anwendung
- demyelinisierende Form der Charcot-Marie-Tooth-Krankheit.
Besondere Vorsicht ist bei vorbestehender Neuropathie, schwerer Leberfunktionsstörung und erhöhtem Risiko für paralytischen Ileus geboten.
Verordnungshinweis
Vincristin ist verschreibungspflichtig und darf nur in hierfür qualifizierten onkologischen Strukturen angewendet werden. Wegen des hohen Risikos letaler Medikationsfehler muss jede Zubereitung eindeutig gekennzeichnet werden. Fachinformationen verlangen den deutlichen Warnhinweis: „VINCRISTIN AUSSCHLIESSLICH ZUR INTRAVENÖSEN VERABREICHUNG – BEI ANDERER ANWENDUNGSART TÖDLICH!“. Zur Fehlervermeidung wird die Bereitstellung in Minibags bzw. Infusionsbeuteln anstelle von Spritzen empfohlen.
Zulassung
In den USA erfolgte die initiale FDA-Zulassung am 10. Juli 1963 unter dem Handelsnamen Oncovin®. In Deutschland wird Vincristin seit den 1960er-Jahren medizinisch eingesetzt. Über den öffentlich dokumentierten Altbestand des BfArM ist der Wirkstoff spätestens vor dem 30.04.1990 als verkehrsfähiges Arzneimittel nachweisbar. Für die Europäische Union besteht für konventionelles Vincristin keine einheitliche zentrale EMA-Erstzulassung. Es ist über nationale Zulassungen in mehreren Mitgliedstaaten verfügbar. Die EMA führt Vincristin auch im Jahr 2024 weiterhin als Wirkstoff mit national zugelassenen Arzneimitteln in der Europäischen Union.
ATC-Code
- L01CA02 - Vincristin
Literatur
- FDA: VinCRIStine Sulfate Injection, Prescribing Information, abgerufen am 8. April 2026
- Pfizer Deutschland: Vincristin Pfizer, Fachinformation, abgerufen am 8. April 2026
- Pfizer USA: VinCRIStine Sulfate Injection, Product Label, abgerufen am 8. April 2026
- Fachinformation.de: Vincristinsulfat-TEVA 1 mg/ml Injektionslösung, abgerufen am 8. April 2026
- Teva Deutschland: Vincristinsulfat-TEVA 1 mg/ml Injektionslösung, Fachinformation (PDF), abgerufen am 8. April 2026
- European Medicines Agency: Vincristine – List of nationally authorised medicinal products, abgerufen am 8. April 2026
- European Medicines Agency: PSUSA/00003121/202308 zu Vincristine, abgerufen am 8. April 2026
- BfArM: Arzneimittelinformationssystem AMIce, abgerufen am 8. April 2026
- PharmNet.Bund: Arzneimittel-Informationssystem, abgerufen am 8. April 2026
- WHO Collaborating Centre for Drug Statistics Methodology: ATC/DDD Index, L01CA02 Vincristine, abgerufen am 8. April 2026
- Li et al., Vincristine-induced peripheral neuropathy: A mini-review, NeuroToxicology, 2020
- Li et al., Characterising vincristine-induced peripheral neuropathy in adults: symptom development and long-term persistent outcomes, Supportive Care in Cancer, 2024
- Shukla et al., Vincristine-based nanoformulations: a preclinical and clinical studies overview, Drug Delivery and Translational Research, 2024