Endoleak
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: Endoleckage
Definition
Ein Endoleak ist ein Leck zwischen der Gefäßprothese und dem Aneurysmasack nach der endovaskulären Versorgung (EVAR) eines Aortenaneurysmas.
Epidemiologie
Endoleaks treten bei 20 bis 40 % der Patienten nach einer EVAR auf.
Ursache
Einige Endoleaks scheinen unvermeidbar zu sein, da bereits bestehende, aus dem Aneurysmasack entspringende offene Gefäßäste vorhanden sind. Ein Endoleak kann aber auch als Folge einer schlechten Patienten- bzw. Transplantatauswahl auftreten.
Einteilung
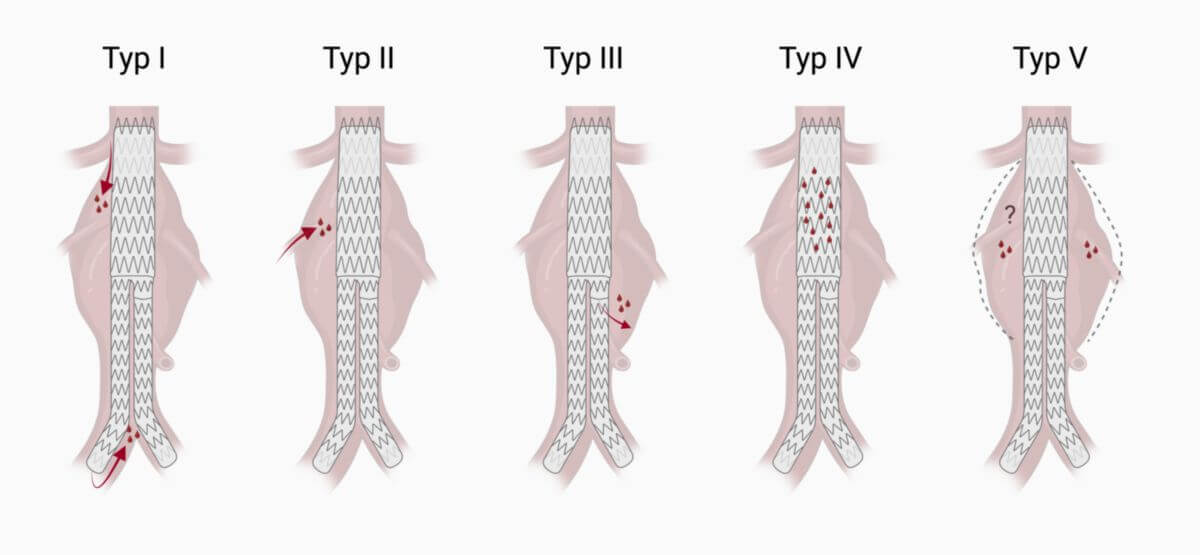
Basierend auf ihrem Entstehungsmechanismus lassen sich Endoleaks in 5 Typen einteilen, bei denen z.T. Subtypen existieren.
Typ I
Ein Endoleak Typ I entsteht durch eine unzureichende Abdichtung an der Ansatzstelle des Grafts. Je nach Lokalisation unterscheidet man weiter:
- Typ Ia: Leck befindet sich in der proximale Landungszone
- Typ Ib: Leck befindet sich in der distalen Landungszone
- Typ Ic: Leck befindet sich im Bereich des iliakalen Verschlusses, also an der Überlappung der beiden Komponenten.
Der Typ I macht ca. 10 % der Fälle aus und tritt insbesondere nach TEVAR auf. Ursächlich ist meist eine ungeeignete Patienten- oder Stentgraft-Auswahl, seltener eine Migration des Stentgrafts. Ein Endoleak Typ I kann unmittelbar nach dem Einsetzen des Stentgrafts aus verschiedenen Gründen auftreten, beispielsweise:
- unvollständige Dilatation des Stentgrafts
- Tortuosität der Aorta
- steile Angulation der Aorta
Verzögerte Endoleaks vom Typ I hängen mit Veränderungen der Aortenkonfiguration zusammenhängen, wenn der Aneurysmasack schrumpft. Diese werden als Hochdruck-Endoleaks bezeichnet und weisen ein hohes Rupturrisiko auf.
Typ II
Beim Endoleak Typ II wird der Aneurysmasack durch einen Seitenast mit Blut gefüllt. Man unterscheidet zwischen:
- Typ IIa: einzelnes zuführendes Blutgefäß
- Typ IIb: mehrere zuführende Blutgefäße
Einfache Endoleaks entstehen in der Regel durch einen retrograden Fluss aus Kollateralarterien, insbesondere aus den Arteriae lumbales oder der Arteria mesenterica inferior. Sie können auch von anderen Aortenkollateralen wie der Arteria iliaca interna, der Arteria sacralis mediana oder akzessorischen Nierenarterien ausgehen.
Typ-II-Endoleaks kommen beim Bauchaortenaneurysma mit 80 % am häufigsten vor. Insgesamt handelt es sich mit 50 % um die häufigste Art des Endoleaks. Es kommt bei ca. 10 bis 44 % der Patienten vor.
Typ III
Ein Endoleak Typ III entsteht durch mechanisches Versagen des Stentgrafts:
- Typ IIIa: Verbindung zwischen modularen Komponenten gelöst
- Typ IIIb: Bruch oder Löcher im Stentgraft
Ursächlich sind mangelhaftes Material, eine extreme Abwinkelung eines Segments oder eine unsachgemäße Überlappung der Module beim Einsetzen. Ein Endoleak Typ III ist relativ selten und tritt nur in etwa 2 % der Fälle nach einer EVAR auf.
Typ IV
Endoleaks vom Typ IV treten auf, wenn aufgrund der Porosität des Transplantats Blut austritt. Mit ungefähr 0,3 % tritt Typ IV sehr selten auf und wird meist im unmittelbar postoperativen Angiogramm entdeckt. Dieser Typ erfordert keine Behandlung und bildet sich in der Regel innerhalb weniger Tage nach dem Einsetzen des Transplantats zurück.
Typ V
Ein Endoleak Typ V wird auch als Endotension bezeichnet. In diesem Fall zeigt sich eine im Verlauf fortgesetzte Expansion des Aneurysmasackes > 5 mm ohne nachweisbare Endoleckage. Vermutete Ursachen sind:
- Pulsationen der Transplantatwand mit Übertragung der Pulswelle über den Aneurysmasack auf die native Aneurysmawand
- Transsudat durch Ultrafiltration von Blut durch die Transplantatmembran
- nicht identifiziertes Leck unterhalb der Auflösung der Bildgebung
Klinik
Meist sind Endoleaks asymptomatisch, jedoch kann durch weitere Expansion des Aneurysmas das Risiko für eine Aortenruptur steigen. Daher vereinbart man nach einer EVAR lebenslang eine jährliche Nachkontrolle, um Endoleaks frühzeitig zu erkennen. Diese Kontrollen erfolgen in der Regel mittels CT-Angiographie (CTA).
Diagnose
Die Diagnose eines Endoleaks erfolgt durch bildgebende Verfahren. Am häufigsten wird die CTA eingesetzt. Weiterhin können Ultraschall, MR-Angiographie (MRA) und die digitale Subtraktionsangiographie (DSA) angewendet werden.
Die CT-Untersuchung wird meist dreiphasig durchgeführt, das heißt nativ, mittels einer arteriellen sowie einer venösen Kontrastmittelphase. Das native Bild ist als Baseline nützlich, insbesondere weil Verkalkungen mit Kontrastmittel verwechselt werden können. In nativen Bild kann bereits eine dichteangehobene akute Blutung im Aneurysmasack zu sehen sein. Nach Gabe von Kontrastmittel zeigt sich im Falle eines Endoleaks ein fokaler oder ein diffuser Anstieg der Dichte im Aneurysmasack aufgrund des Kontrastmittelextravasats. Langsame Endoleaks können in der venösen Phase erkannt werden.
Therapie
Die Therapie eines Endoleaks richtet sich danach, welcher Typ vorliegt.
Typ I
Endoleaks vom Typ I werden in der Regel sofort nach ihrer Detektion behandelt, da sie sich normalerweise nicht spontan rückbilden. Häufig wird mittels Ballonangioplastie die proximale Ansatzstelle so umgeformt, dass eine Abdichtung erreicht wird. Bleibt sie erfolglos, kommen ballonexpandierbare Bare-metal Stents zum Einsatz. Weiterhin werden Verlängerungsmanschetten oder gecoverte Stents verwendet. In einigen Fälle ist eine chirurgische Reparatur notwendig.
Typ II
Endoleaks vom Typ II thrombosieren normalerweise spontan. Je nach Literatur wird trotzdem eine Behandlung bei einem Aneurysmadurchmesser von über 9 bis 10 mm empfohlen. Eine Embolisation des Gefäßastes ist indiziert, wenn der Aneurysmasack sich weiter vergrößert. Manchmal wird vor dem Einsetzen des Stentgrafts eine präventive Embolisation kaliberstarker Lumbalarterien, der Arteria iliaca interna oder der Arteria mesenterica inferior durchgeführt. Jedoch existieren über die Effektivität dieses Verfahrens nur beschränkt Daten.[1]
Typ III
Bei einem mechanischen Transplantatversagen werden in der Regel zusätzliche Stentgraft-Komponenten eingesetzt.
Typ IV
Ein Endoleak aufgrund von Transplantatporosität bedarf meist keiner Behandlung.
Typ V
Wenn ein fortgesetztes Wachstum des Aneurysmasacks nachgewiesen wird, kann eine weitere Behandlung mit zusätzlichen endoluminalen Komponenten (Cuffs oder Verlängerungen) erfolgreich sein. Alternativ kommen offen-chirurgische Verfahren zum Einsatz.
Quellen
- ↑ Hauck et al. Endovaskuläre Aortenreparatur bei Endoleaks, Die Radiologie, 2022
Literatur
- Rosen RJ, Green RM Endoleak management following endovascular aneurysm repair, J Vasc Interv Radiol. 2008;19(6 Suppl):S37-S43
- Kougias P et al. Successful treatment of endotension and aneurysm sac enlargement with endovascular stent graft reinforcement, J Vasc Surg. 2007;46(1):124-127
- White SB, Stavropoulos SW Management of Endoleaks following Endovascular Aneurysm Repair, Semin Intervent Radiol. 2009;26(1):33-38
- Stavropoulos SW, Charagunndla SR Imaging techniques for detection and management of endoleaks after endovascular aortic aneurysm repair, Radiology. 2007;243(3):641-655
- Hong C et al. Clinical significance of endoleak detected on follow-up CT after endovascular repair of abdominal aortic aneurysm, AJR Am J Roentgenol. 2008;191(3):808-813
- Bashir MR et al. Endoleaks after endovascular abdominal aortic aneurysm repair: management strategies according to CT findings, AJR Am J Roentgenol. 2009;192(4):W178-W186
- Rozenblit AM et al. Detection of endoleaks after endovascular repair of abdominal aortic aneurysm: value of unenhanced and delayed helical CT acquisitions, Radiology. 2003;227(2):426-433
- Kudo T et al. Type 1a endoleak following Zone 1 and Zone 2 thoracic endovascular aortic repair: effect of bird-beak configuration, Eur J Cardiothorac Surg. 2017;52(4):718-724
- Shen A et al. Natural History Of an Untreated Type 1 Endoleak: A Case Report, Cureus. 2017;9(7):e1507
- Chen J, Stavropoulos SW Management of Endoleaks, Semin Intervent Radiol. 2015;32(3):259-264
- Brown A et al. Type II endoleaks: challenges and solutions, Vasc Health Risk Manag. 2016;12:53-63
- Steinmetz E et al. Type II endoleak after endovascular abdominal aortic aneurysm repair: a conservative approach with selective intervention is safe and cost-effective, J Vasc Surg. 2004;39(2):306-313
- Sidloff DA et al. Type II endoleak after endovascular aneurysm repair, Br J Surg. 2013;100(10):1262-1270
- Avgerinos ED et al. Type II endoleaks, J Vasc Surg. 2014;60(5):1386-1391
- Tolia AJ et al. Type II endoleaks after endovascular repair of abdominal aortic aneurysms: natural history, Radiology. 2005;235(2):683-686
- Güntner O et al. Inferior mesenteric arterial type II endoleaks after endovascular repair of abdominal aortic aneurysm: are they predictable?, Radiology. 2014;270(3):910-919
- Bryce Y et al. Type II endoleaks: diagnosis and treatment algorithm, Cardiovasc Diagn Ther. 2018;8(Suppl 1):S131-S137
- Moll FL et al. Management of abdominal aortic aneurysms clinical practice guidelines of the European society for vascular surgery, Eur J Vasc Endovasc Surg. 2011;41 Suppl 1:S1-S58
- Maleux G et al. Incidence, etiology, and management of type III endoleak after endovascular aortic repair, J Vasc Surg. 2017;66(4):1056-1064
- Teutelink A et al. Fabric tears as a new cause of type III endoleak with Ancure endograft, J Vasc Surg. 2003;38(4):843-846
- Eng ML et al. Treatment options for late type III endoleaks after endovascular aneurysm repair, Ann Vasc Surg. 2015;29(3):594.e5-594.e5.94E9
- Wachal K et al. Diagnosis and treatment of a patient with type IV endoleak as a late complication after endovascular aneurysm repair, Wideochir Inne Tech Maloinwazyjne. 2014;9(4):667-670