Thyreotroper Regelkreis
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonyme: Hypophysen-Schilddrüsen-Regelkreis, Hypothalamus-Hypophysen-Schilddrüsen-Achse, Thyreotrope Achse, Astwood-Hoskins-Regelkreis, HPT-Achse
Englisch: Thyrotropic feedback control
Definition
Der thyreotrope Regelkreis ist ein Regelkreis, der zwischen der Hypophyse und der Schilddrüse aufgespannt wird. Er reguliert die Konzentration an Schilddrüsenhormonen im Plasma.
Physiologie
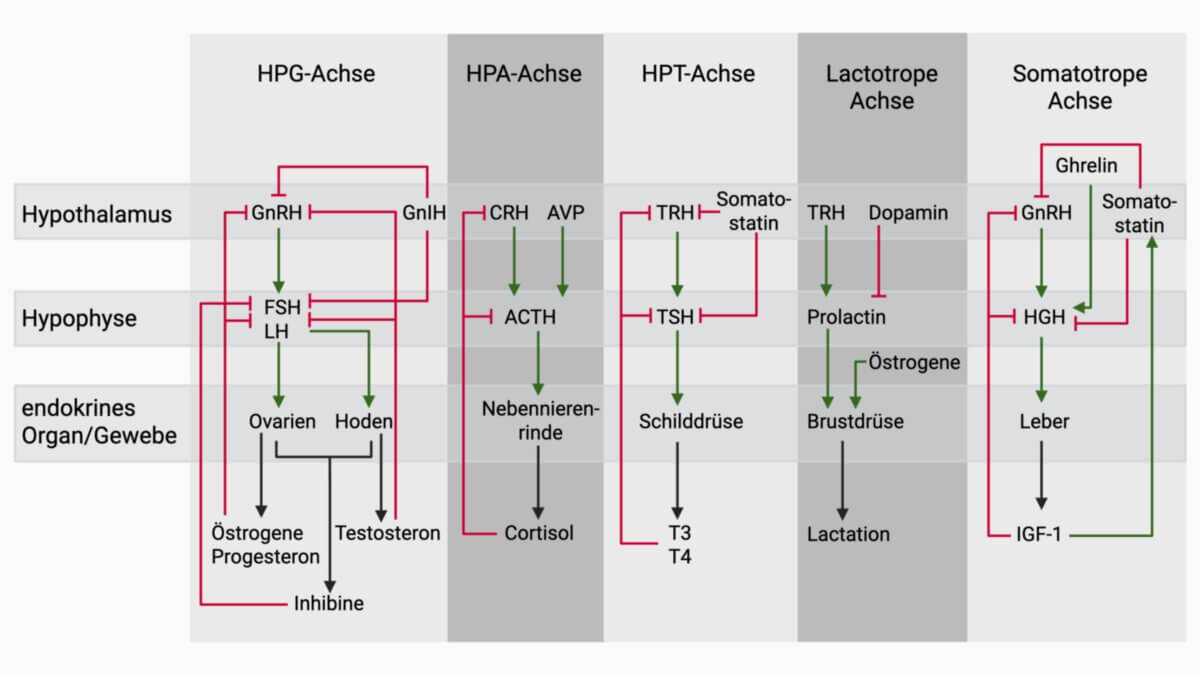
Die Hypophyse schüttet das Steuerhormon Thyreotropin (TSH) aus, das in der Schilddrüse die Sekretion von Thyroxin (T4) und Trijodthyronin (T3) anregt. Umgekehrt hemmen Schilddrüsenhormone im Sinne einer Gegenkoppelung die Ausschüttung von TSH, so dass sich Gleichgewichtsspiegel der beteiligten Hormone einstellen. Darüber hinaus hängt die TSH-Inkretion von dem Spiegel des Releasing-Hormons TRH ab, das vom Hypothalamus ausgeschüttet wird und den Sollwert des Regelkreises vorgibt.
Abgesehen von diesem Hauptregelkreis gibt es weitere eingeschaltete Rückkoppelungsschleifen, z.B. ein Ultra-Short-Feedback von TSH auf seine eigene Ausschüttung (Brokken-Wiersinga-Prummel-Regelkreis), ein Long-Feedback von Schilddrüsenhormonen auf die TRH-Freisetzung und Regelkreise, welche die Plasmaproteinbindung von T4 und T3 einstellen.
Funktionszustände des Hypophysen-Schilddrüsen-Regelkreises
- Euthyreose (Normale Schilddrüsenfunktion)
- Hypothyreose (Schilddrüsenunterfunktion)
- Primäre Hypothyreose (Regelkreis in der Schilddrüse unterbrochen, z.B. durch mangelnde Inkretionsleistung nach Operation oder bei Autoimmunthyreopathien)
- Sekundäre Hypothyreose (Regelkreis in der Hypophyse unterbrochen, z.B. im Rahmen einer HVL-Insuffizienz)
- Tertiäre Hypothyreose (Vorgabe des Sollwertes fehlt durch Mangel an TRH, z.B. im Rahmen einer Schädigung des Hypothalamus, eines Pickardt-Syndroms oder eines Non-Thyroidal-Illness-Syndroms.)
- Hyperthyreose (Schilddrüsenüberfunktion)
- Primäre Hyperthyreose (Inappropriate Sekretion von Schilddrüsenhormonen durch eine Erkrankung der Schilddrüse, z.B. bei Autonomien und beim Morbus Basedow)
- Sekundäre Hyperthyreose (z.B. durch TSH-produzierende Tumoren der Hypophyse)
- Thyreotoxikose (Überversorgung mit Schilddrüsenhormonen, z.B. durch Hyperthyreosen oder durch Medikamente)
- Schilddrüsenhormonresistenz (Unterbrechung des Regelkreises an den Rezeptoren in der Hypophyse und der Peripherie)
Diagnostik
Geschichte
Die Existenz eines zwischen Hypophyse und Schilddrüse aufgespannten Regelkreises wurde erstmals 1940 von W. T. Salter nach dem Vorbilld der beiden kurz zuvor entdeckten gonadotropen Regelkreise postuliert. Astwood und Hoskins konnten wenige Jahre später sowohl die Existenz als auch die pathophysiologische Relevanz dieses Regelkreises aufdecken.
Etwa zwei Jahrzehnte später gelang es Panda und Turner, die Interdependenz zwischen Thyroxin- und TSH-Spiegel erstmals quantitativ zu erfassen.
Kakita et al. wiesen 1984 die Existenz eines Ultra-Short-Feedback-Mechanismus der TSH-Sekretion bei Kaninchen nach.
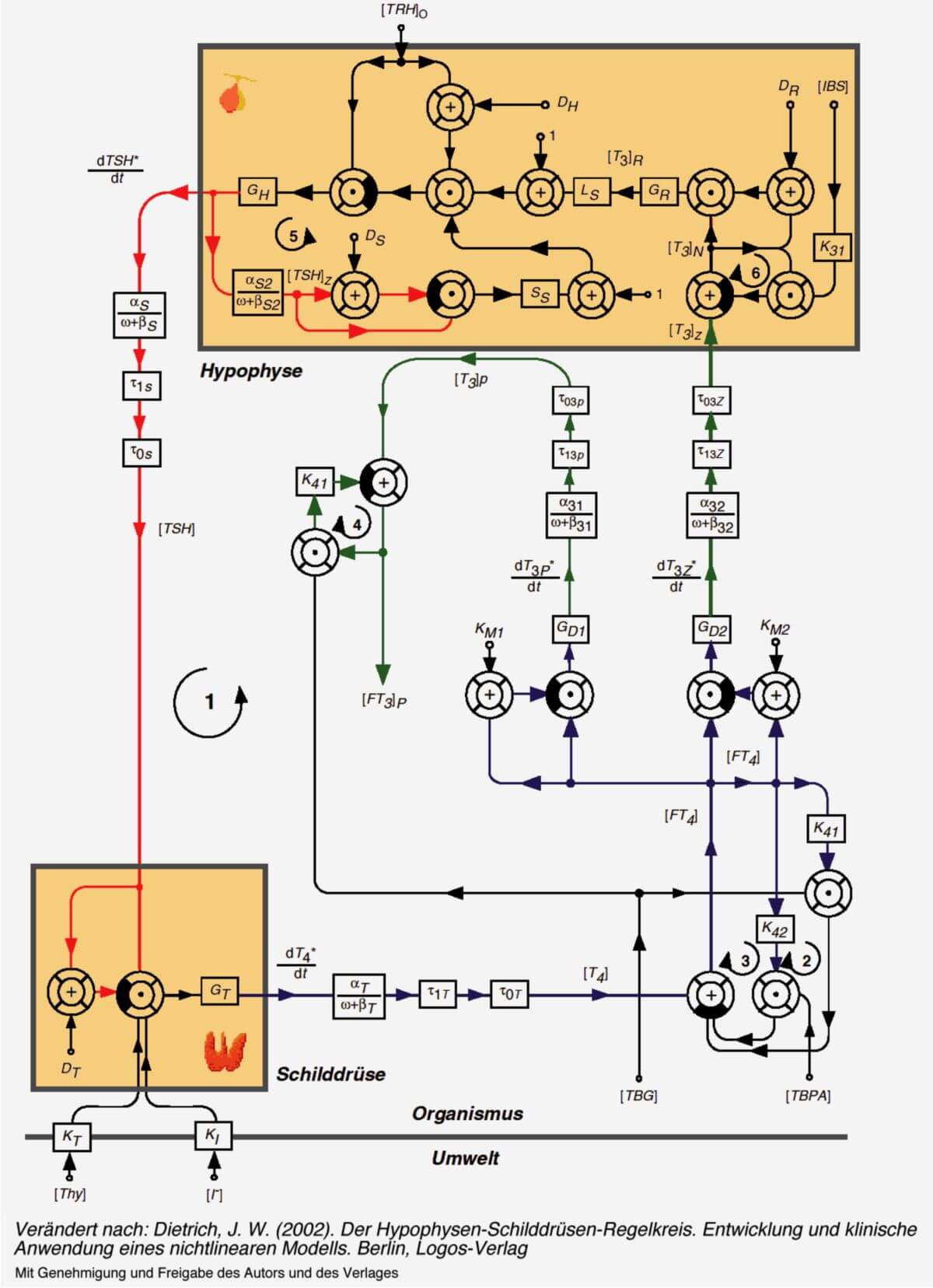
Nachdem ein mathematisches Modell der thyreotropen Achse die Existenz dieses Mechanismus durch in silico - Modelle auch am Menschen nahegelegt hatte (Dietrich et al. 2004), konnte die Arbeitsgruppe um Brokken, Wiersinga und Prummel dieselbe auch in vivo nachweisen. Die kontinuierliche Suppression des TSH-Spiegels trotz Euthyreose bei Patienten mit Morbus Basedow demonstriert die klinische Relevanz dieses Mechanismus.
Derzeit zeichnet sich auch die Existenz eines Long-Feedback-Mechanismus von Iodothyroninen auf die hypothalamische TRH-Sekretion ab. Dieser Effekt könnte u.a. für die Pathogenese eines Non-Thyroidal-Illness-Syndroms relevant sein.
Podcast

Web-Link
- SimThyr: Numerisches Simulationsprogramm des thyreotropen Regelkreises (Mac, Windows, Linux).
Literatur
- Salter, WT (1940). The Endocrine Function of Iodine. Harvard University Press, Cambridge.
- Hoskins, RG (1949). The thyroid-pituitary apparatus as a servo (feed-back) mechanism. J. clin. Endocr. Metab. 9, 1429-1431.
- Astwood EB. Mechanism of action of antithyroid compounds. Brookhaven Symp Biol. 1955 Feb;7:61-72; discussion, 72-3. PubMed PMID 14351812
- Panda JN, Turner CW. Thyroxine feed-back on the regulation of thyrotropin [TSH secretion]. J Physiol. 1968 Mar;195(1):29-37. PMID 5644487; PMCID: PMC1557901
- Prummel MF, Brokken LJ, Meduri G, Misrahi M, Bakker O, Wiersinga WM.: Expression of the thyroid-stimulating hormone receptor in the folliculo-stellate cells of the human anterior pituitary. J Clin Endocrinol Metab. 2000 Nov;85(11):4347-53. PMID: 11095478
- Brokken LJ, Scheenhart JW, Wiersinga WM, Prummel MF.: Suppression of serum TSH by Graves' Ig: evidence for a functional pituitary TSH receptor. J Clin Endocrinol Metab. 2001 Oct;86(10):4814-7. PMID: 11600546
- Brokken LJ, Wiersinga WM, Prummel MF.: Thyrotropin receptor autoantibodies are associated with continued thyrotropin suppression in treated euthyroid Graves' disease patients. J Clin Endocrinol Metab. 2003 Sep;88(9):4135-8.
- Dietrich, J. W., A. Tesche, C. R. Pickardt, U. Mitzdorf: Thyrotropic Feedback Control: Evidence for an Additional Ultrashort Feedback Loop from Fractal Analysis. Cybernetics and Systems 2004; 35(4): 315-31.
- Prummel MF, Brokken LJ, Wiersinga WM: Ultra short-loop feedback control of thyrotropin secretion. Thyroid. 2004 Oct; 14(10): 825-9. PMID 15588378
- Brokken LJ, Bakker O, Wiersinga WM, Prummel MF: Functional thyrotropin receptor expression in the pituitary folliculo-stellate cell line TtT/GF. Exp Clin Endocrinol Diabetes. 2005 Jan; 113(1): 13-20. PMID 15662590
- Dietrich JW, Landgrafe, G, Fotiadou, EH. TSH and Thyrotropic Agonists: Key Actors in Thyroid Homeostasis Journal of Thyroid Research, vol. 2012, Article ID 351864, 29 pages, 2012. doi:10.1155/2012/351864. PMID 23365787.
- Hoermann R, Midgley JE, Larisch R, Dietrich JW. Homeostatic Control of the Thyroid-Pituitary Axis: Perspectives for Diagnosis and Treatment. Front Endocrinol (Lausanne). 2015 Nov 20;6:177. doi: 10.3389/fendo.2015.00177. PMID 26635726; PMCID PMC4653296.
- Berberich J, Dietrich JW, Hoermann R, Müller MA. Mathematical Modeling of the Pituitary-Thyroid Feedback Loop: Role of a TSH-T(3)-Shunt and Sensitivity Analysis. Front Endocrinol (Lausanne). 2018 Mar 21;9:91. doi: 10.3389/fendo.2018.00091. PMID 29619006; PMCID PMC5871688.
Bildquelle
- Bildquelle Podcast: © Carly Mackler / Unsplash