McDonald-Kriterien
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
Loslegennach dem neuseeländischen Neurologen William Ian McDonald (1933–2006)
Englisch: McDonald criteria
Definition
Die McDonald-Kriterien dienen der Diagnosestellung einer Multiplen Sklerose.
Hintergrund
Die McDonald-Kriterien werden durch das International Advisory Committee on Clinical Trials in Multiple Sclerosis regelmäßig überarbeitet, um neue Forschungsergebnisse zu berücksichtigen. Die Revision von 2024 ersetzt die Fassung von 2017 und soll die Diagnosestellung beschleunigen, bei unverändert hoher Spezifität.[1]
In geeigneten Situationen kann die diagnostische Sensitivität steigen, etwa durch die Aufnahme des Sehnervs als fünfte Lokalisation sowie durch Zusatzmarker wie zentrales Venenzeichen, paramagnetische Randläsionen und kappa freie Leichtketten (kFLC).
Die aktualisierten Kriterien schaffen einen einheitlichen Rahmen für alle Verlaufsformen (schubförmig und progredient) und Altersgruppen (pädiatrisch bis Spätbeginn).
Kriterien
Für die Diagnose einer Multiplen Sklerose ist in den meisten Fällen eine typische Schubsymptomatik erforderlich. Ergänzend müssen bildgebende Befunde die räumliche Dissemination belegen. Der Nachweis einer zeitlichen Dissemination bleibt in den 2024 Kriterien als Option möglich, ist aber nicht mehr in allen Konstellationen zwingend erforderlich, da alternativ auch Liquorbefunde wie oligoklonale Banden (OKB) oder kFLC, ebenso wie spezifische radiologische Marker wie das zentrale Venenzeichen oder paramagnetische Randläsionen die Diagnose stützen können.
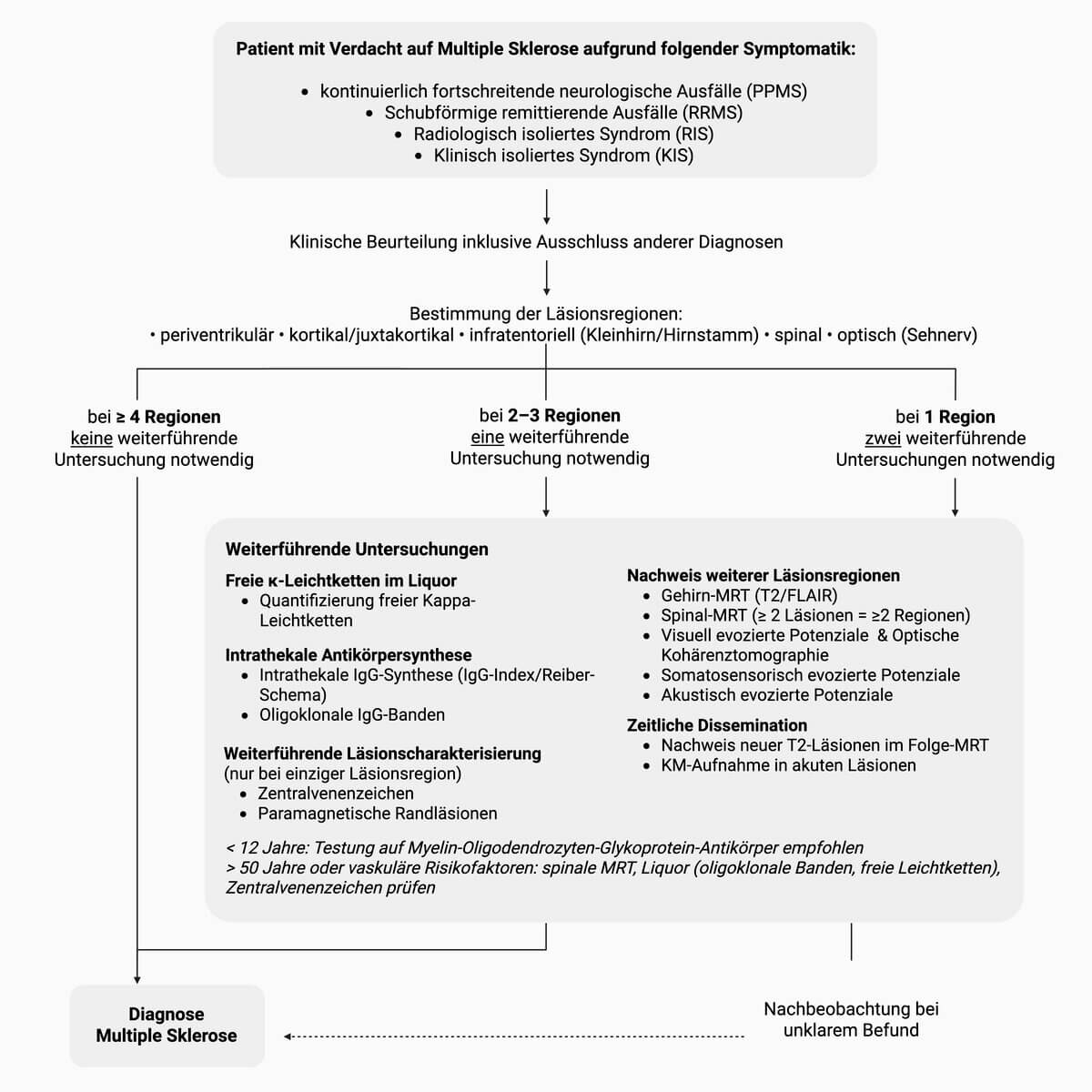
In der folgenden Tabelle sind die diagnostischen Konstellationen dargestellt, die nach den McDonald-Kriterien von 2024 die Diagnose einer Multiplen Sklerose ermöglichen.
| Anzahl klinischer Schübe | Anzahl Läsionen | Zusätzliche Kriterien erforderlich |
|---|---|---|
| ≥ 2 | Läsionen in ≥ 2 Regionen (inkl. Sehnerv) | Keine weiteren Kriterien. Klinische und paraklinische Evidenz genügt nach Ausschluss besserer Erklärungen. |
| ≥ 2 | Läsion(en) in 1 Region | Bei ≥ 2 Schüben ist die zeitliche Dissemination erfüllt. Bei Läsion(en) in 1 Region ist zusätzlich erforderlich:
a) Räumliche Dissemination oder b) mindestens ein hochspezifisches Zusatzkriterium:
|
| 1 | Läsionen in ≥ 2 Regionen | Mindestens ein Kriterium erforderlich:
|
| 1 | Läsion(en) in 1 Region | Bei Läsion(en) in 1 Region sind zusätzlich zwei Befunde in Kombination erforderlich:
|
| Klinische Progression ≥ 12 Monate (primär progrediente MS) | Läsionen in ≥ 2 Regionen | Zusätzlich mindestens eines der folgenden Kriterien:
|
| Klinische Progression ≥ 12 Monate (primär progrediente MS) | ≥ 2 spinale Läsionen | wie oben |
| Klinische Progression ≥ 12 Monate (primär progrediente MS) | Läsion(en) in 1 Region | Bei Läsion(en) in 1 Region sind zusätzlich zwei Befunde in Kombination erforderlich
|
| Keine Schübe (asymptomatische Personen mit inzidentellen, MS-typischen MRT-Läsionen) | Läsionen in ≥ 2 Regionen | Zusätzlich einer der folgenden Befunde:
|
* Das zentrale Venenzeichen wird nach der Select-6-Regel beurteilt: Es gilt als positiv, wenn mindestens 6 Marklagerläsionen eine zentrale Vene aufweisen. Bei weniger als 10 Läsionen muss die Mehrzahl eine zentrale Vene zeigen. Die Beurteilung erfolgt in SWI- oder T2*-gewichteten Sequenzen, idealerweise mit 3 Tesla.
Räumliche Dissemination
Die räumliche Dissemination im MRT ist erfüllt, wenn MS-typische Herde an mindestens zwei der folgenden Lokalisationen sichtbar sind:
| Ort | Erklärung |
|---|---|
| kortikal/juxtakortikal | Im Kortex gelegen/den Kortex direkt berührend, ohne dass weiße Substanz zwischen Kortex und der Läsion zu sehen ist |
| periventrikulär | Die Seitenventrikel direkt berührend, ohne dass weiße Substanz zwischen Ventrikel und der Läsion zu sehen ist |
| infratentoriell | Typische Läsionen im Hirnstamm oder Kleinhirn |
| spinal | Intramedulläre Läsion im Rückenmark |
| Sehnerv | Nachweis einer demyelinisierenden Sehnervbeteiligung. Auch eine subklinische (asymptomatische) Sehnervbeteiligung kann zur Erfüllung der räumlichen Dissemination herangezogen werden.
Möglich über MRT, OCT oder VEP, bei Auschluss besserer Erklärungen: MRT: eine oder mehrere Läsionen des Nervus opticus, sofern kein Befund vorliegt, der eher auf eine andere Ursache hinweist (etwa ausgeprägte Chiasmabeteiligung, Optikus-Perineuritis oder langstreckige, extensive Läsion). OCT: pathologisch bei interokulärer Differenz der peripapillären RNFL ≥ 6 µm oder der GCIPL ≥ 4 µm. Messung sollte qualitätsgesichert sein (OSCAR-IB-Kriterien), möglichst ab 3 Monaten nach einseitiger akuter Optikusneuritis.[2] [3] Anmerkung: bei bilateraler Sehnervbeteiligung sind interokuläre OCT-Differenzen weniger sensitiv. VEP: pathologisch bei verzögerter P100-Latenz oder asymmetrischer interokulärer Latenz, jeweils ≥ 2,5 Standardabweichungen über dem laborbezogenen Referenzwert. Durchführung nach ISCEV-Standards mit zentrumeigenen Normdaten.[2][4] |
Bei klinischer Progression über mindestens zwölf Monate genügen zwei spinale Läsionen für die räumliche Dissemination.
Sind MS-typische Läsionen nur in einer Region nachweisbar, ist die Diagnose bei typischer klinischer Präsentation möglich, wenn zusätzlich eine der folgenden Kombinationen erfüllt ist:
- Liquor (OKB oder kFLC-Index) und zentrales Venenzeichen positiv
- Liquor (OKB oder kFLC-Index) und mindestens eine paramagnetische Randläsion
- Zeitliche Dissemination und zentrales Venenzeichen positiv
- Zeitliche Dissemination und mindestens eine paramagnetische Randläsion
Zeitliche Dissemination
Die zeitliche Dissemination bleibt weiterhin definiert durch:
- neue T2-Läsionen im Verlauf, oder
- neue Gadolinium-aufnehmende Läsionen im Verlauf, oder
- das gleichzeitige Auftreten von Gadolinium-aufnehmenden und nicht-aufnehmenden Läsionen in einer Untersuchung, oder
- das Auftreten eines neuen klinischen Schubs.
Mit der Revision 2024 ist die zeitliche Dissemination in spezifischen Situationen für die Diagnosestellung nicht mehr zwingend erforderlich. Für einen Nachweis der zeitlichen Dissemination anhand einer Sehnervläsion mittels longitudinaler OCT oder VEP besteht derzeit keine gesicherte Evidenz.
Asymptomatische Läsionen und radiologisch isoliertes Syndrom
Nach den revidierten McDonald-Kriterien 2024 können asymptomatische Befunde, einschließlich radiologisch isoliertem Syndrom, eine MS-Diagnose ermöglichen, wenn eine räumliche Dissemination mit Läsionen in mindestens zwei von fünf typischen Regionen vorliegt und zusätzlich weitere Kriterien erfüllt sind (siehe Tabelle).
Anmerkungen
Eine rein klinische Diagnose ohne paraklinische Nachweise wird nicht empfohlen. Zur Erstabklärung erfolgt ein Gehirn-MRT mit Kontrastmittel. Ein spinale MRT sollte frühzeitig ergänzt werden, insbesondere bei spinalen Symptomen, progredientem Verlauf, höherem Alter oder vaskulären Risikofaktoren. Suszeptibilitätsgewichtete Sequenzen sind für das zentrale Venenzeichen und paramagnetische Randläsionen sinnvoll, wenn verfügbar.
Der routinemäßige Einsatz serologischer Antikörpertests auf MOG-IgG und AQP4-IgG ist nicht sinnvoll. Bei Kindern unter 12 Jahren wird eine MOG-IgG-Testung beim ersten demyelinisierenden Ereignis empfohlen. Bei Jugendlichen ab 12 Jahren und Erwachsenen erfolgt die Bestimmung von MOG-IgG beziehungsweise AQP4-IgG gezielt, wenn die Konstellation untypisch ist oder MOGAD bzw. NMOSD vermutet wird. Bleibt die Diagnose unsicher, sollte eine engmaschige klinische Reevaluation mit Verlaufs-MRT erfolgen, zum Beispiel nach 6 bis 12 Monaten.
Quellen
- ↑ Montalban et al., Diagnosis of multiple sclerosis: 2024 revisions of the McDonald criteria, The Lancet Neurology, 2025
- ↑ 2,0 2,1 Saidha et al., The use of optical coherence tomography and visual evoked potentials in the 2024 McDonald diagnostic criteria for multiple sclerosis, The Lancet Neurology, 2025
- ↑ Tewarie et al., The OSCAR-IB Consensus Criteria for Retinal OCT Quality Assessment, PLoS ONE, 2012
- ↑ Odom et al., ISCEV standard for clinical visual evoked potentials (2016 update), Documenta Ophthalmologica, 2016