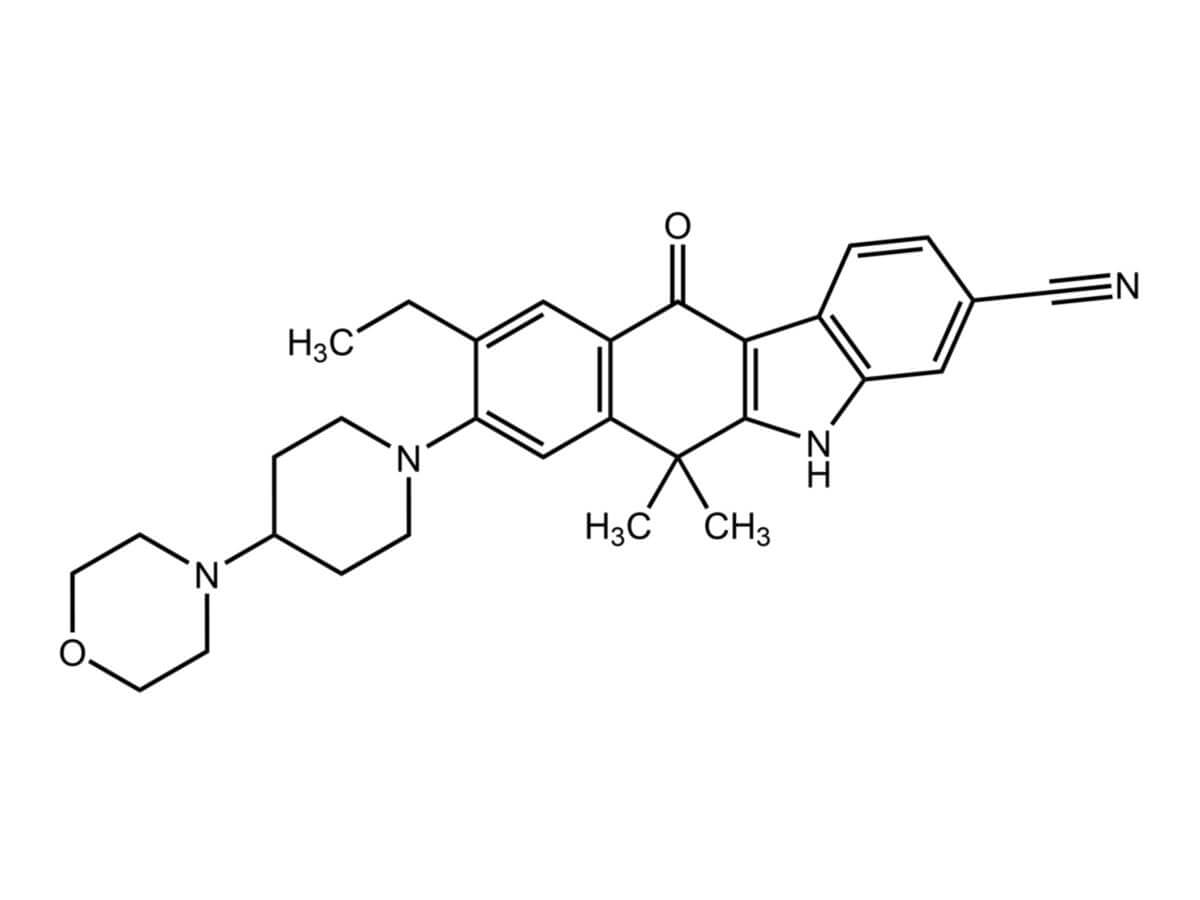
Alectinib
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsname: Alecensa®
Definition
Alectinib ist ein Arzneistoff aus der Klasse der Tyrosinkinase-Inhibitoren, der in der Onkologie zur Therapie des nicht-kleinzelligen Bronchialkarzinoms (NSCLC) eingesetzt wird.
Wirkmechanismus
Alectinib ist ein selektiver Hemmstoff der Rezeptor-Tyrosinkinasen ALK und RET. Die Hemmung dieser Kinasen unterbricht ALK- and RET-abhängige Signalwege sowie STAT3 und PI3K/AKT. Es verhindert dadurch das Wachstum von Tumorzellen, bei denen ALK und RET überexprimiert sind. Es kommt zur Apoptose der Tumorzellen.[1]
Wie bei anderen Tyrosinkinase-Inhibitoren kann es durch Mutation der Tumorzellen im Laufe der Behandlung mit Alectinib zu einer Resistenzentwicklung kommen, die eine Rebiopsie und einen Medikationswechsel notwendig macht. Für die Resistenzentwicklung sind eine Amplifikation des mutierten ALK-Gens oder die Entwicklung neuer ALK-Varianten mit veränderter Aminosäuresequenz verantwortlich.
Pharmakokinetik
Maximale Plasmaspiegel von Alectinib werden nach etwa 4 bis 6 Stunden erreicht. Der Arzneistoff hat eine hohe Plasmaproteinbindung (> 99 Prozent). Alectinib und sein Hauptmetabolit M4, werden hauptsächlich über CYP3A4 metabolisiert. Die Plasmahalbwertszeit für Alectinib beträg ca. 32,5 Stunden. Der entsprechende Wert für M4 liegt bei 30,7 Stunden.[1]
Indikation
- Erstlinientherapie des ALK-positiven, fortgeschrittenen nicht-kleinzelligen Lungenkarzinoms (NSCLC) bei erwachsenen Patienten.
- Monotherapie des ALK-positiven, fortgeschrittenen nicht-kleinzelligen Bronchialkarzinoms (NSCLC) bei erwachsenen Patienten, die zuvor mit Crizotinib behandelt wurden.
- Monotherapie als adjuvante Behandlung nach vollständiger Tumorresektion bei erwachsenen Patienten mit ALK-positivem nicht-kleinzelligem Lungenkarzinom (NSCLC) mit hohem Rezidivrisiko.
Dosierung
Die empfohlene Tagesdosis von Alectinib beträgt 1.200 mg, aufgeteilt in zwei Dosen à 600 mg (vier Hartkapseln à 150 mg).[1]
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Nebenwirkungen
Folgende Nebenwirkungen traten in den zulassungsrelevanten klinischen Studien unter Alectinib sehr häufig (≥ 1/10) auf:[1]
- Anämie
- Obstipation
- Erbrechen
- Übelkeit
- Diarrhö
- Hepatotoxizität (AST↑, ALT↑, Bilirubin↑)
- Exanthem
- Myalgie, CPK-Erhöhung
- Ödeme
- Gewichtszunahme
Wechselwirkungen
Die Wirkung von Alectinib kann durch CYP3A4-Induktoren und Inhibitoren beeinflusst werden.[2] Alectinib und M4 besitzen das Potenzial, die Plasmakonzentrationen gleichzeitig angewendeter P-Glykoprotein-Substrate und BCRP-Transporter zu erhöhen. Auch eine Wechselwirkung mit oralen Kontrazeptiva kann nicht vollständig ausgeschlossen werden.[1]
Kontraindikationen
- Überempfindlichkeit gegenüber dem Wirkstoff
- Schwangerschaft und Stillzeit (teratogene Wirkung)[1]
Nutzenbewertung
Nach Einschätzung des G-BA besteht für Alectinib bei Patienten mit ALK-positivem NSCLC, die für eine adjuvante platinbasierte Chemotherapie geeignet sind, ein Anhaltspunkt für einen erheblichen Zusatznutzen.
Dagegen hält der G-BA einen Zusatznutzen bei Patienten mit ALK-positivem NSCLC nach vorheriger adjuvanter platinbasierter Chemotherapie oder bei Patienten, die nicht für eine solche Chemotherapie geeignet sind, für nicht belegt.[4]
Kosten
Die Jahrestherapiekosten betragen pro Patient rund 100.000 €.[5]
Quellen
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 Fachinformation Alecensa®, abgerufen am: 24.08.2018.
- ↑ Liu YN et al. Effects of drug-drug interactions and CYP3A4 variants on alectinib metabolism. Arch Toxicol. 2023
- ↑ European Medicines Agency (EMA) Abgerufen am:24.08.2018
- ↑ Alectinib (Neues Anwendungsgebiet: nicht-kleinzelliges Lungenkarzinom, ALK+, hohes Rezidivrisiko, adjuvante Therapie). G-BA Beschluss 16.01.2025, abgerufen am 18.01.2025
- ↑ IQWiG-Berichte – Nr. 612 Alectinib (nicht kleinzelliges Lungenkarzinom) Nutzenbewertung gemäß § 35a SGB V abgerufen am 24.8.2018