Nicht-homologe Endverknüpfung
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: Nichthomologe End-zu-End-Verknüpfung
Englisch: Non-homologous end-joining, Nonhomologous end-joining (NHEJ), Canonical Non-homologous end-joining (c-NHEJ)
Definition
Die Nicht-homologe Endverknüpfung, kurz NHEJ, ist ein Mechanismus zur DNA-Reparatur von Doppelstrangbrüchen.
Mechanismus
Im Gegensatz zur Homologie-gerichteten Reparatur werden bei der NHEJ die getrennten Stränge unabhängig von ihrer Sequenz wieder zusammengefügt. Da es bei diesen Prozessen üblicherweise zu Substanzverlusten kommt, ist dieser Mechanismus fehleranfällig.[1]
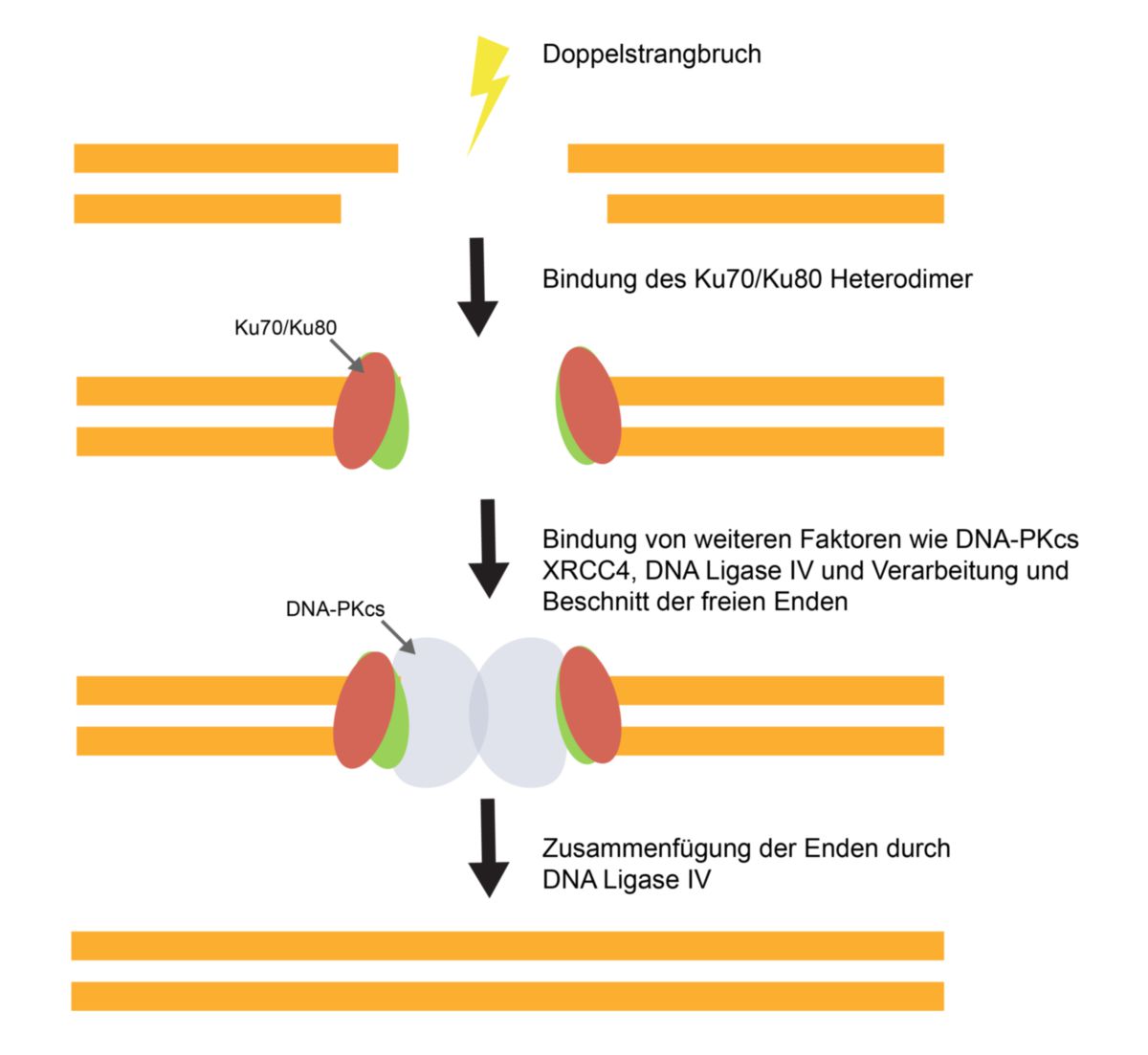
- Zufälliger Doppelstrangbruch: Entstehung eines Doppelstrangbruchs, beispielsweise durch chemische Mutagene oder ionisierende Strahlung.[2]
- Erkennen der freien Endstücke durch Ku70/Ku80: Ein Heterodimer, bestehend aus Ku70/Ku80 bindet an die offenen Enden. Dieser Prozess findet bereits wenige Sekunden nach einem Strangbruch statt, da Ku70/Ku80 eine hohe, sequenzunabhängige Affinität für freie DNA-Enden besitzt und in hoher Konzentration im Zellkern vorliegt. Ku70/Ku80 dient als Gerüst für die Bindung von weiteren Faktoren wie DNA-PKcs, XRCC4, DNA-Ligase IV. Sowohl die Reihenfolge der Rekrutierung als auch die Zusammensetzung der Faktoren variiert je nach Art des Doppelstrangbruchs.[3][4]
- Bearbeitung der Enden: Bevor die Enden zusammengefügt werden können, müssen üblicherweise einige Nukleotide entfernt werden und blockierende Hydroxyl- oder Phosphatgruppen modifiziert werden. Diese Exo- und Endonukleasen werden durch die DNA-PKcs phosphoryliert und aktiviert.[5]
- Ligation der Endstücke: Die gebundene DNA-Ligase IV kann nun die Endstücke zusammenfügen.[6]
Hintergrund
Ein DNA-Doppelstrangbruch ist einer der kritischsten DNA-Schäden für die Zelle. Unreparierte Brüche können zum Zelltod (Apoptose) oder zur Entartung der Zelle führen (Karzinogenese). In der menschlichen Zelle werden diese Schäden am häufigsten mit dem NHEJ-Mechanismus repariert, da dieser schnell und unabhängig vom Zellzyklus stattfinden kann. Fehlerfreie Mechanismen wie die Homologe Rekombination benötigen ein Schwesterchromatid als Vorlage, welches nur in der S- und G2-Phase vorliegt.
Obwohl durch NHEJ potentiell neue Mutationen eingeführt werden können, ist das onkogene Potential freier DNA-Enden größer, da es hier zu chromosomalen Rearrangements kommen kann.[7] Viele Proteine des NHEJ sind außerdem an Prozessen der V(D)J-Rekombination beteiligt, die ebenfalls das Zusammenfügen von freien DNA-Enden erfordert.[8]
Quellen
- ↑ Anthony J.F. Griffiths: Introduction to Genetic Analysis. W.H. Freeman and Company, 2005, Seite 472-473.
- ↑ Davis, Anthony J., and David J. Chen. “DNA Double Strand Break Repair via Non-Homologous End-Joining.” Translational cancer research 2.3 (2013): 130–143. PMC. Web. 11 Jan. 2018.
- ↑ Davis, Anthony J., and David J. Chen. “DNA Double Strand Break Repair via Non-Homologous End-Joining.” Translational cancer research 2.3 (2013): 130–143. PMC. Web. 11 Jan. 2018.
- ↑ Mari, Pierre-Olivier et al. “Dynamic Assembly of End-Joining Complexes Requires Interaction between Ku70/80 and XRCC4.” Proceedings of the National Academy of Sciences of the United States of America 103.49 (2006): 18597–18602. PMC. Web. 11 Jan. 2018
- ↑ Bernstein NK, Williams RS, Rakovszky ML, et al. The molecular architecture of the mammalian DNA repair enzyme, polynucleotide kinase. Mol Cell. 2005;17:657–70
- ↑ Davis, Anthony J., and David J. Chen. “DNA Double Strand Break Repair via Non-Homologous End-Joining.” Translational cancer research 2.3 (2013): 130–143. PMC. Web. 11 Jan. 2018.
- ↑ Bruce Alberts: Molekularbiologie der Zelle. Wiley-VCH Verlag, 2017, S. 305-307.
- ↑ Anthony J.F. Griffiths: Introduction to Genetic Analysis. W.H. Freeman and Company, 2005, Seite 472-473.