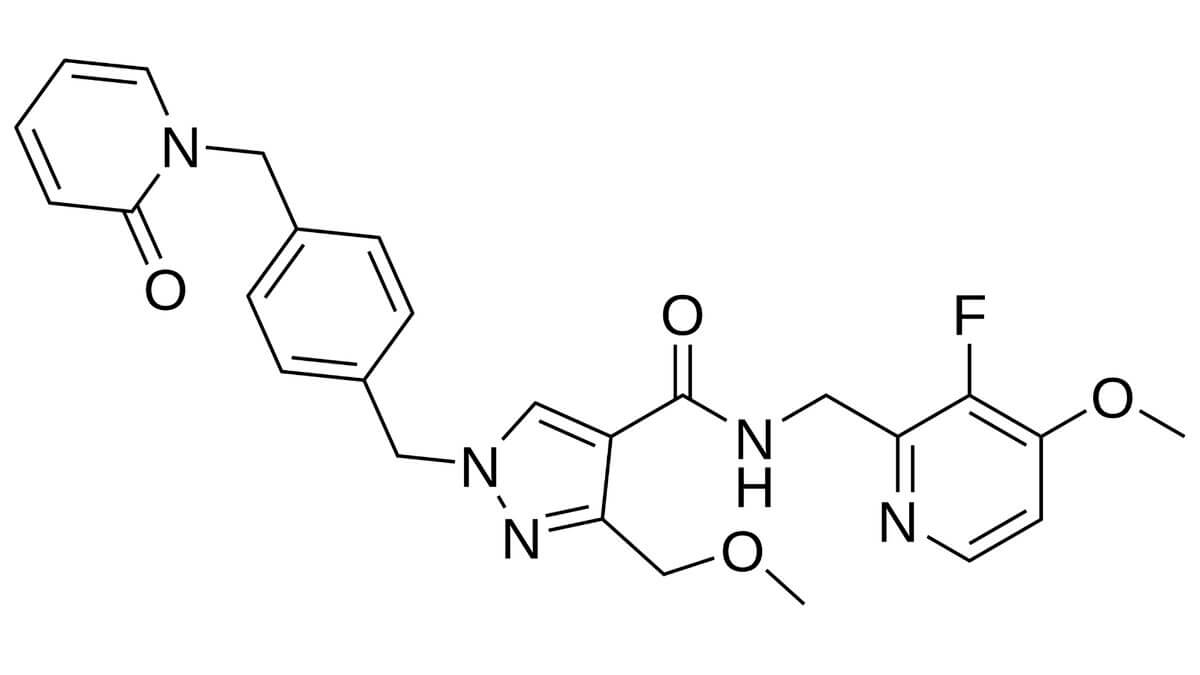
Sebetralstat
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsname: Ekterly®
Englisch: sebetralstat
Definition
Sebetralstat ist ein oral verfügbarer, kompetitiver Plasmakallikrein-Inhibitor. Er wird zur Akutbehandlung des hereditären Angioödems (HAE) eingesetzt.
Chemie
Die Summenformel lautet C₂₆H₂₆FN₅O₄. Die molare Masse beträgt etwa 491 g/mol. Die Substanz weist eine hohe Selektivität gegenüber Plasmakallikrein auf.
Wirkmechanismus
Beim hereditären Angioödem führt ein Mangel oder eine Dysfunktion des C1-Inhibitors zu einer gesteigerten Aktivität des Kallikrein-Kinin-Systems. Plasmakallikrein spaltet hochmolekulares Kininogen zu Bradykinin, das eine erhöhte Gefäßpermeabilität und Ödembildung verursacht.
Sebetralstat hemmt kompetitiv und reversibel Plasmakallikrein. Dadurch wird die Bradykininfreisetzung reduziert und die Progression einer HAE-Attacke abgeschwächt.
Pharmakokinetik
Sebetralstat wird nach oraler Gabe rasch resorbiert. In klinischen Studien wurde bereits 15 Minuten nach Einnahme eine nahezu vollständige Hemmung der Plasmakallikrein-Aktivität beobachtet. Die Eliminationshalbwertszeit beträgt etwa 3,7 Stunden.
Indikationen
Sebetralstat wird zur symptomatischen Behandlung akuter Attacken des hereditären Angioödems bei Erwachsenen und Jugendlichen ab 12 Jahren eingesetzt.
Darreichungsform
Sebetralstat ist als Filmtablette zu 300 mg zur oralen Anwendung verfügbar.
Dosierung
Die empfohlene Dosierung beträgt 300 mg bei den ersten Anzeichen einer bevorstehenden Attacke. Bei nicht ausreichender Wirkung kann 3 Stunden nach der ersten Dosis eine zweite Gabe erfolgen.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Nebenwirkungen
Mögliche Nebenwirkungen sind u.a.:
- Kopfschmerzen
- Gastrointestinale Beschwerden
- Fatigue
- Rückenschmerzen
Kontraindikationen
- Überempfindlichkeit gegenüber dem Wirkstoff
- Anwendung bei Kindern unter 12 Jahren (mangels Daten)
- Schwangerschaft und Stillzeit (Einzelfallentscheidung nach strenger Nutzen-Risiko-Abwägung)
Zulassung
Sebetralstat wurde im September 2025 als erste orale On-Demand-Therapie zur Behandlung akuter HAE-Attacken von der europäischen Arzneimittelbehörde zugelassen.
Literatur
- Fachinformation Ekterly, abgerufen am 26.11.2025
- Gelbe Liste: Neueinführung Ekterly: Erste orale Akuttherapie bei hereditärem Angioödem, abgerufen am 26.11.2025