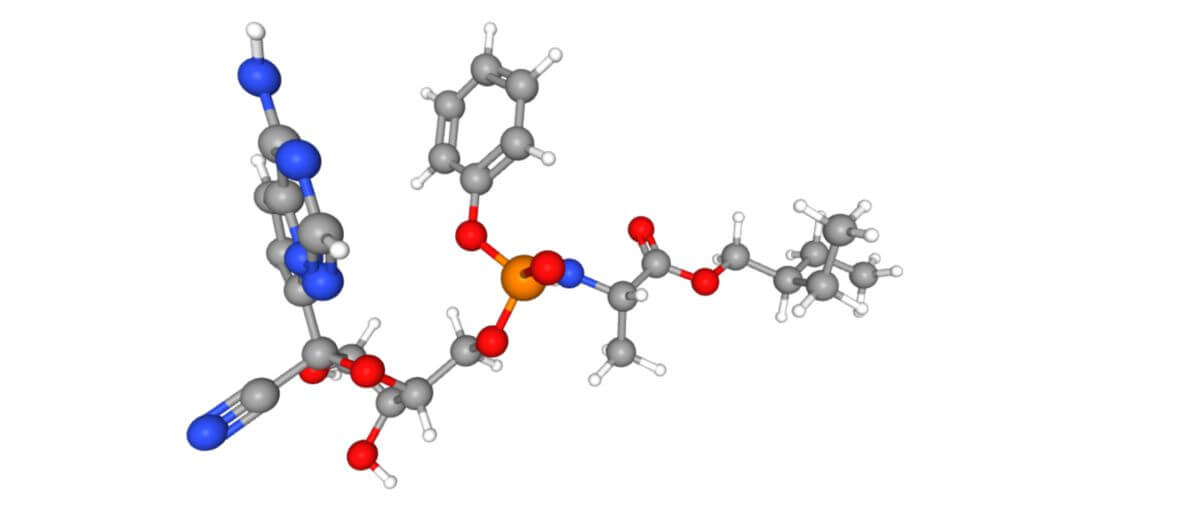
Remdesivir
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: GS-5734
Handelsname: Veklury®
Englisch: remdesivir
Definition
Remdesivir, kurz RDV, ist ein experimentelles Virostatikum aus der Klasse der Nukleotidanaloga.
Chemie
Remdesivir ist das Monophosphoramidat-Prodrug eines Adenosin-Nukleotidanalogons. Die Summenformel von Remdesivir ist C27H35N6O8P. Die molare Masse beträgt rund 602,6 g/mol.
Wirkmechanismus
Der aktive Metabolit von Remdesivir stört die Aktivität der viralen RNA-Polymerase, indem Remdesivir-Triphosphat statt Adenosintriphosphat (ATP) in die RNA eingebaut wird.[1] Das führt zu einer verminderten RNA-Produktion. Es ist noch nicht geklärt, ob es dabei zu einem Kettenabbruch oder zu RNA-Mutanten kommt.
Wirkspektrum
Remdesivir wurde von Gilead ursprünglich gegen Infektionen mit dem Ebola- oder Marburg-Virus entwickelt. Gegen das Ebola-Virus erwies es sich jedoch als weniger effektiv als eine Vergleichstherapie mit monoklonalen Antikörpern.[2] Es zeigt aber gegen andere Erreger antivirale Aktivität, u.a. gegen:
- Coronaviren
- MERS-CoV
- SARS-CoV
- SARS-CoV-2 (2019-nCoV)
- Respiratory-Syncytial-Virus
- Junin-Viren
- Lassa-Viren
- Nipah-Viren
Die Wirkung gegen viele verschiedene Viren hat dem Wirkstoff den Label "Breitspektrumvirostatikum" eingetragen. Ob sich die Substanz tatsächlich bei allen genannten Viren bewährt, muss noch durch klinische Studien geklärt werden.
Experimenteller Einsatz bei COVID-19
Im Zusammenhang mit der COVID-19-Pandemie stellte Gilead den Wirkstoff für klinische Prüfungen zur Verfügung.[3] Eine Testmedikation in China fand mit Unterstützung der chinesischen Gesundheitsbehörden statt. Im tierexperimentellen Setting war Remdesivir wirksam gegen MERS-CoV und SARS-CoV.
Im Februar 2020 wurde eine randomisierte kontrollierte Studie mit hospitalisierten COVID-19-Patienten am Nebraska Medical Center (UNMC), USA begonnen. Seit März 2020 laufen auch in Deutschland in mehreren Zentren Phase-III-Studien mit Remdesivir.
In einer randomisierten klinischen Studie in China mit 237 COVID-19-Patienten, deren Ergebnisse im April 2020 irrtümlich vorpubliziert wurden, zeigte Remdesivir keine überzeugende Wirkung.[4]
Im Okober 2020 veröffentlichte die WHO Daten der SOLIDARITY-Studie mit mehr als 11.200 hospitalisierten COVID-19-Patienten. Im Remdesivir-Arm der Studie waren 2.750 Patienten vertreten. Der Wirkstoff zeigte keinen signifikanten Einfluss auf die Mortalität und konnte auch die Aufenthaltsdauer in der Klinik nicht maßgeblich verkürzen.[5]
Im November 2020 sprach sich die WHO offziell gegen einen Einsatz von Remdesivir bei hospitalisierten COVID-19-Patienten aus.[6]
Zulassung
Am 1.5.2020 erhielt der Hersteller Gilead von der FDA eine Emergency Use Authorization (EUA) für Remdesivir.
Am 03.07.2020 erteilte die EU-Kommission eine bedingte Marktzulassung für Patienten mit schwerem COVID-19.
Kosten
Eine 5tägige Behandlung mit Remdesivir kostet rund 2.000 Euro (Stand 7/2020).
Quellen
- ↑ Gordon CJ et al.: The antiviral compound remdesivir potently inhibits RNA-dependent RNA polymerase from Middle East respiratory syndrome coronavirus. Journal of Biological Chemistry, February 24, 2020, abgerufen am 26.2.2020
- ↑ McNeil DG: "A Cure for Ebola? Two New Treatments Prove Highly Effective in Congo". The New York Times. 12. August 2019, abgerufen am 26.2.2020
- ↑ Joseph, Saumya Sibi; Samuel, Maju: "Gilead working with China to test Ebola drug as new coronavirus treatment". Thomson Reuters, abgerufen am 31.1.2020
- ↑ Gilead antiviral drug remdesivir flops in first trial. Financial Times, 23.4.2020, abgerufen am gleichen Tag
- ↑ Remdesivir has little effect on Covid-19 mortality, WHO study says. Financial Times online 15.10.2020, abgerufen am 16.10.2020
- ↑ WHO recommends against the use of remdesivir in COVID-19 patients, who.int, abgerufen am 20.11.2020