FlexiEssay: Entwicklung von Leishmanien in der Sandmücke
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenDieser Text ein so genannter FlexiEssay. So nennen wir Texte, die keinen lexikalischen Inhalt haben. FlexiEssays geben die persönliche Einschätzung des Autors wieder. Sie werden von uns nicht inhaltlich überprüft. Wie bei allen anderen Texten gilt: Lies dir den Artikel kritisch durch, vergleiche ihn mit anderen Publikationen und bilde dir eine eigene Meinung.
Verdauungsprozess der Sandmücke (Nomenklatur)
Sandmücken sind Vektoren für die Übertragung von Leishmanien auf Wirbeltiere (und den Menschen) und gehören zu den "Poolsaugern". Anders als die "Kapillarsauger" wie zum Beispiel die Stechmücken ritzen weibliche Exemplare mit ihren breiten sägeähnlichen Mundwerkzeugen die Haut eines Wirbeltiers (bisweilen schmerzhaft) auf und nehmen mit ihrem Saugrüssel (Proboscis) aus dem Pool (der Pfütze) von Blut, Lymphe und Zellflüssigkeit ihre Nahrung auf, die mittels der Pumpmuskulatur von Cibarium (hinterer Teil der Mundhöhle) und Pharynx (Schlund) zunächst bis zum Vorderdarm weiterbefördert wird. Der vordere Teil des Verdauungsapparats bis zum Vorderdarm wird bei Insekten als Stomodaeum bezeichnet. An einer Verengung zwischen Vorderdarm (englisch: foregut) und Mitteldarm (englisch: midgut) sorgt der Schließmuskel der Valvula cardiaca (oder auch einfach Cardia, englisch: stomodeal valve) in der Funktion eines Ventils dafür, dass keine bereits weiterverdaute Nahrung aus dem Mitteldarm in den Vorderdarm zurückfließen kann. Am hinteren Ende des Mitteldarms trennt mit analoger Ventilfunktion der Schließmuskel der Valvula pylorica (englisch: pyloric valve) den Mitteldarm vom Enddarm (englisch: hindgut).[1][2]
Im Mitteldarm der Sandmücke werden wie bei den meisten Gliederfüßern die aufgenommenen Mahlzeiten von einer für verwertbare Nährstoffe durchlässigen, aus mehreren peritrophischen Membranen bestehenden peritrophischen Hülle (englisch: peritrophic matrix) umschlossen und in dieser Hülle verdaut. Die verdauten, nicht verwerteten Nahrungsreste werden in der peritrophischen Hülle eingeschlossen an den Enddarm weitergegeben.[3][4]
Entwicklung von Leishmanien des Subgenus Leishmania in der Sandmücke
Leishmanien durchlaufen einen mit einer Vermehrung verbundenen Entwicklungszyklus.
Überblick
Bei einem mit Leishmanien vom Subgenus Leishmania infizierten gleichwarmen Wirbeltier werden während einer ersten Blutmahlzeit der weiblichen Sandmücke auch mit Amastigoten gefüllte Makrophagen (und ebenfalls bei der Zerstörung von Zellen freigesetzte Amastigoten) aufgesaugt und bis in den hinteren Mitteldarm weitertransportiert, wo die amastigoten Leishmanien durch den beginnenden Verdauungsprozess aus den Makrophagen freigesetzt werden, die Sandmücke infizieren und sich im Weiteren extrazellulär im Darm der Sandmücke weiterentwickeln. Mittels mehrerer Formveränderungen verwandeln sich die Amastigoten in verschiedene Subformen von Promastigoten, vermehren sich, wandern in der Sandmücke nach vorn und infizieren in ihrer metazyklischen Form bei der nächsten Blutmahlzeit das dann gestochene Wirbeltier. Die zweite Blutmahlzeit findet 1-2 Wochen nach der vorherigen statt. Zwischenzeitlich ernähren sich die weiblichen Sandmücken wie die männlichen von Pflanzensäften (gern von Obstbäumen) und Blattlausexkrementen (englisch: sugarmeal phase). Einige Sandmückenspezies können zusätzlich während der noch nicht vollendeten Promastigoten-Formveränderungskette eine erneute Blutmahlzeit zu sich nehmen, vor einer Ausreifung zu metazyklischen Promastigoten sind die dann vorhandenen Leishmanien jedoch noch nicht infektiös. Bei der Mehrheit der Sandmückenspezies reicht jedoch der Zeitraum zwischen zwei Blutmahlzeiten zu einer Ausbildung der infektiösen metazyklischen Form aus.[3]
Änderung der morphologischen Subform von Promastigoten
Im hinteren Mitteldarm wird noch innerhalb der von der peritrophischen Hülle umschlossenen zunächst noch wenig verdauten Blutmahlzeit aufgrund der Änderung der Umgebungsparameter (Absenkung der Temperatur im wechselwarmen Sandmückenkörper im Vergleich zum gleichwarmen Wirbeltierkörper, Erhöhung des pH-Werts) die Umwandlung vom Amastigoten zum zunächst wenig beweglichen, noch rundlichen prozyklischen Promastigoten (mit einer Geißel am Vorderende in Bezug auf die Bewegungsrichtung) eingeleitet. Die Mutation in die prozyklische Form wird von der Ausbildung einer Glykokalyx und der Expression einer Metalloprotease begleitet, die gemeinsam vor den Verdauungsenzymen des Mitteldarms schützen.[4] Bei den prozyklischen Promastigoten setzt ein erster Replikationsprozess noch innerhalb der wenig verdauten Blutmahlzeit ein. Nach wenigen Tagen endet diese Vermehrungsphase, und die prozyklischen Einzeller differenzieren zu länglichen, extrem beweglichen nectomonaden Promastigoten, die in Richtung des vorderen Mitteldarms wandern, sich zunächst im vorderen Teil der peritrophischen Hülle ansammeln, diese durchbrechen und so der Blutmahlzeit und deren weiterer Verdauung entfliehen. Mittels verschiedener (teils speziesspezifischer) Anbindungstechniken gelingt es den nectomonaden Einzellern, sich am Darmepithel anhaftend bis zur Valvula cardiaca vorzuarbeiten, wo sie sich in die kürzere leptomonade Form umwandeln und in dieser Form einen neuen Replikationszyklus einleiten.[3][4][5][6] Die leptomonaden Promastigoten erzeugen über die Geißeltasche zudem ein überwiegend aus filamentösem Phosphoglycan bestehendes Gel, das PSG (promastigote secretory gel), das in der Folge einen vom vorderen Mitteldarm bis zum Vorderdarm verlaufenden Pfropfen bildet und die Valvula cardiaca verstopft.[3][4]
Ein sehr geringer Anteil der leptomonaden Einzeller heftet sich mit ihren Geißelenden hemidesmosom-ähnlich an der Cuticula der Valvula cardiaca fest an und differenziert dort zu haptomonaden Promastigoten. Deren Rolle wird noch nicht vollständig verstanden.[5][3] Vermutlich schädigen sie durch die eine sekretierte Chitinase den Schließmuskel und bilden so eine Voraussetzung für die Ausbildung des PSG-Pfropfens.[4]
Ein weiterer Teil der leptomonaden Einzeller differenziert schließlich zu metazyklischen Promastigoten, deren überwiegender Teil am Vorderende des PSG-Pfropfens angesiedelt ist. Ein Teil wandert auch weiter nach vorn in die Pharynx, das Cibarium und in den Saugrüssel und bettet sich dort in den Speichel der Sandmücke ein.[3][4]
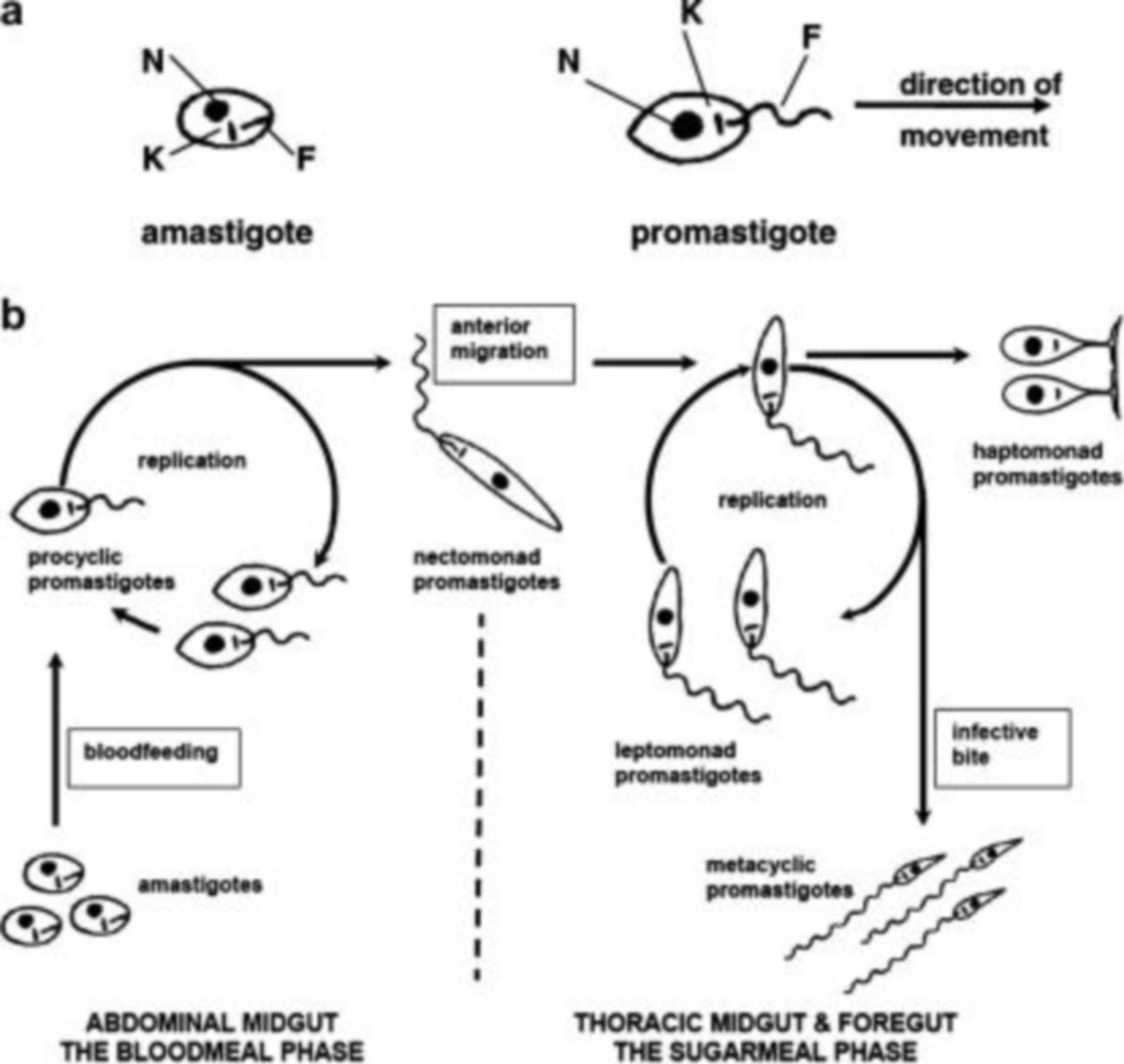
Bilderläuterung: Morphologische Formen von Leishmanien (Subgenus Leishmania) im Sandmücken-Vektor[3]
N=Zellkern, K=Kinetoplast, F=Geißel
Entwicklungssequenz vom Amastigoten zu den folgenden morphologischen Subformen von Promastigoten
- prozyklisch – erste morphologische Subform der Formveränderungskette eines Trypanosomatiden in einem Arthropoden
- Nectomonade = "schwimmender Einzeller"
- Leptomonade = "kleiner (oder schmaler) Einzeller"
- Haptomonade = "sich anheftender Einzeller“
- metazyklisch – Subform der morphologischen Form eines Wirbeltiere infizierenden Trypanosomatiden (also der Gattung Leishmania oder Trypanosoma), die in einem Arthropoden ausreift und für einen Wirbeltier-Wirt infektiös ist. Im Wirbeltier-Wirt wird eine neue Formveränderungskette des Trypanosomatiden eingeleitet.
Neben den genannten Formveränderungen enthält die Entwicklung also 2 Replikationsphasen bei den prozyklischen und den leptomonaden Promastigoten. Metazyklische Promastigoten können sich nicht replizieren, auch nicht in Leishmanien-Kulturen. In Kulturen gewachsene Promastigoten sind für Wirbeltiere nicht unmittelbar infektiös. Sofern die prozyklischen Promastigoten aus Amastigoten gewonnen werden, kann man allerdings heute den gesamten Entwicklungsvorgang in der Sandmücke in vitro nachbilden und die nachträgliche Metazyklogenese einer Kultur leptomomader Promastigoten stimulieren.[6]
Entwicklung von Leishmanien des Subgenus Viannia in der Sandmücke
Leishmanien des Subgenus Viannia sind nur in der Neuen Welt vorhanden. Alle befallenen Sandmücken gehören der Gattung Lutzomyia an. Wie nach einer Infektion von Sandmücken des Subgenus Leishmania entwickeln sich in der wenig verdauten Blutmahlzeit im hinteren Mitteldarm der Sandmücke aus den Amastigoten die prozyklischen Promastigoten und replizieren sich dort. In der Folge wird aber dann die Mehrheit der Parasiten in der Valvula pylorica und im benachbarten Enddarm aufgefunden.
Bei der Entwicklung von Promastigoten vom Typ Viannia können zum gegenwärtigen Zeitpunkt noch nicht alle Beobachtungen vernünftig gedeutet werden. Der derzeitige Forschungsstand besteht aus einigen Hypothesen, noch nicht aus gesicherten Erkenntnissen. Eine Hypothese besagt, dass neben den im Enddarm gefundenen Nectomonaden ein noch nicht quantifizierter kleinerer Teil in Richtung der vorderen Mitteldarms wandert und dass deren Entwicklung in ihren groben Zügen denen der Entwicklung von Promastigoten des Subgenus Leishmania folgt, dass also die im Enddarm aufgefundenen Promastigoten für den Lebenszyklus von Viannia-Leishmanien nicht relevant sind.
Als heute wahrscheinlichere Hypothese wird allerdings postuliert, dass die im Enddarm aufgefundenen Parasiten im Anschluss den Weg nach vorn antreten. Diese These wird durch die Beobachtung bestärkt, dass sich Haptomonaden fest an der Cuticula der Valvula pylorica anheften, ähnlich wie sich die Haptomonaden des Subgenus Leishmania an der Cuticula der Valvula cardiaca festsetzen. Nach dieser heute favorisierten Hypothese würden also die Viannia-Promastigoten eine ähnliche Entwicklung nehmen wie die Subgenus-Leishmania-Promastigoten, sie würden lediglich einen Umweg über den Enddarm mit zusätzlichen Haptomonaden an der Valvula pylorica nehmen. Ein Schwachpunkt dieser Hypothese ist allerdings darin zu sehen, dass man bisher so gut wie keine Belege dafür gefunden hat, dass sich Viannia-Promastigoten als Nectomonaden mit Anhaftungstechniken am Darmepithel fortbewegen können. Man hat also keine Vorstellung davon, wie sich die Viannia-Promastigoten bis zur Valvula cardiaca vorarbeiten. Trotz des partiellen Nichtwissens wird diese These jedoch für wahrscheinlich gehalten, da das Ende des Entwicklungsprozesses, nämlich metazyklische Promastigoten und PSG, auch für die Viannia-Formveränderungskette in der Sandmücke belegt ist.[3]
Die Infektion des Wirbeltiers
Bei einer Blutmahlzeit der infizierten Sandmücke muss aufgrund der Verstopfung der Valvula cardiaca und großer Teile von Vorder- und Mitteldarm zunächst zumindest ein Teil des PSG-Pfropfens in den aufgeschnittenen Pool von Blut und Lymphe regurgitiert werden, bevor die neue Blutmahlzeit aufgenommen werden kann. An der Infektion des Wirbeltiers sind also drei Elemente beteiligt: die metazyklischen Promastigoten, der Speichel der Sandmücke und der erbrochene PSG-Pfropfen. Neuere Forschungsergebnisse legen nahe, dass zwar auch der Speichel der Sandmücke und die im Speichel enthaltenen Promastigoten an der Infektion beteiligt sind, dass aber dem regurgitierten Gel die entscheidende Rolle zukommt, eine große Menge Makrophagen an den aufgesägten Pool von Blut und Lymphe zu locken, die dann die im Speichel und im Gel vorhandenen infektiösen metazyklischen Promastigoten phagozytieren. Durch das PSG werden ungefähr fünf Mal mehr Makrophagen angezogen als durch den Speichel der Sandmücke.[7] In den Makrophagen eines gleichwarmen Wirbeltiers wandeln sich dann die Promastigoten wieder in Amastigoten um, die sich vermehren, die Zellen sprengen und dann wieder neue Makrophagen für ihre jetzt intrazelluläre Lebensweise befallen.
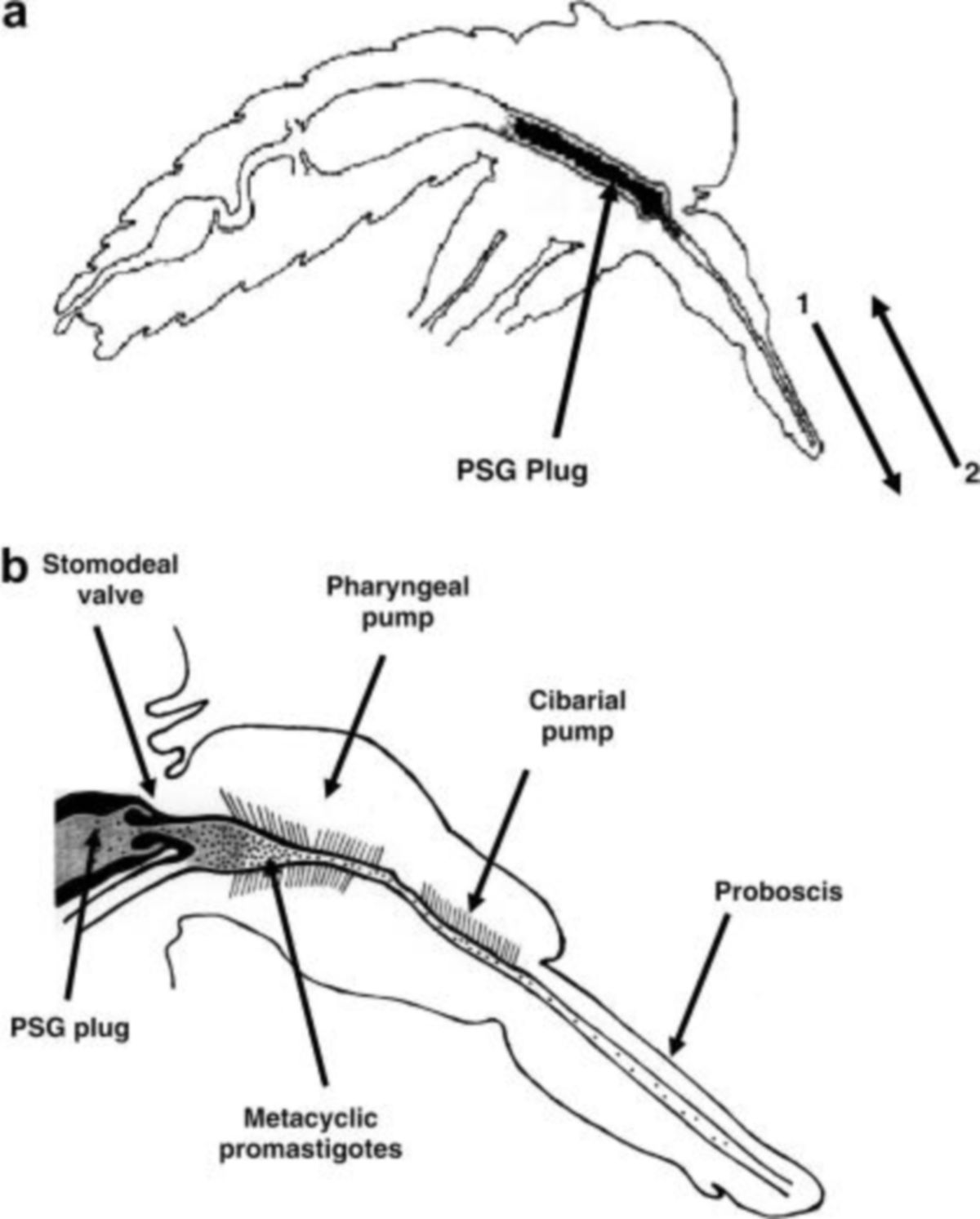
Bilderläuterung: Sagittalschnitt durch eine weibliche Leishmanien-infizierte Sandmücke
(a) PSG-Pfropfen (PSG = promastigote secretory gel) zwischen vorderem Mitteldarm und Vorderdarm. Der Pfropfen muss zumindest teilweise erbrochen werden (1), bevor eine neue Blutmahlzeit aufgenommen werden kann (2). Bei der Regurgitation werden metazyklische Promastigoten und PSG in die aufgeritzte Wunde des Wirbeltiers injiziert. (b) Detail aus vorderem Mitteldarm und Vorderdarm. Der entstehende PSG-Pfropfen erzwingt, dass die Valvula cardiaca (englisch: stomodeal valve) geöffnet wird. Der Pfropfen (schattiert) kann sich so bis in die Pharynx-Region ausdehnen. Metazyklische Promastigoten (punktiert) konzentrieren sich am vorderen Ende des Pfropfens, können jedoch auch im Vorderdarm, im Cibarium sowie im Saugrüssel aufgefunden werden.[3]
Quellen
- ↑ John R. Meyer Digestive and Excretory Systems Tutorial 2016. Man kann jeweils unten auf der jeweiligen Seite nach STOMODAEUM, MESENTERON und PROCTODAEUM abzweigen. Anklicken eines Links zeigt das jeweils betroffene Organ im präsentierten Bild an.
- ↑ Spektrum Biologie Insekten
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 3,7 3,8 Paul A. Bates Transmission of Leishmania metacyclic promastigotes by phlebotomine sand flies Int J Parasitol. 2007 Aug; 37(10-3): 1097–1106
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 Michael Heimann Entwicklung eines ELISA zur Diagnose von viszeraler Leishmaniose, Dissertation, Gießen 2008
- ↑ 5,0 5,1 Sunter/Gull Shape, form, function and Leishmania pathogenicity: from textbook descriptions to biological understanding Open Biol. 2017 Sep; 7(9): 170165
- ↑ 6,0 6,1 Gossage et al. Two separate growth phases during the development of Leishmania in sand flies: implications for understanding the life cycle Int J Parasitol. 2003 Sep 15; 33(10): 1027–1034
- ↑ Imperial College London Wer kommt heute zu Besuch? Weiße Blutzellen füttern Leishmanien Cordis Projektbericht 2009
Hinweise
FlexiEssays geben die persönliche Einschätzung des Autors wieder, die nicht notwendigerweise mit der allgemeinen Lehrmeinung kongruent ist. Sie werden zu einem späteren Zeitpunkt einen eigenen Platz im Flexikon finden.