Kleinzelliges Bronchialkarzinom
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonyme: kleinzelliges Lungenkarzinom, Haferzellkarzinom, "Kleinzeller"
Englisch: Small Cell Lung Cancer(SCLC), oat cell carcinoma
Definition
Als kleinzelliges Bronchialkarzinom, kurz SCLC, bezeichnet man ein Bronchialkarzinom, das bei mikroskopischer Betrachtung aus kleinen Zellen (APUD-Zellen) besteht. Es wird den neuroendokrinen Karzinomen zugerechnet.
Pathologie
Etwa 15-20 % aller Bronchialkarzinome sind kleinzellige BC.[1] Der wichtigste bekannte Risikofaktor für die Entstehung ist das Rauchen.
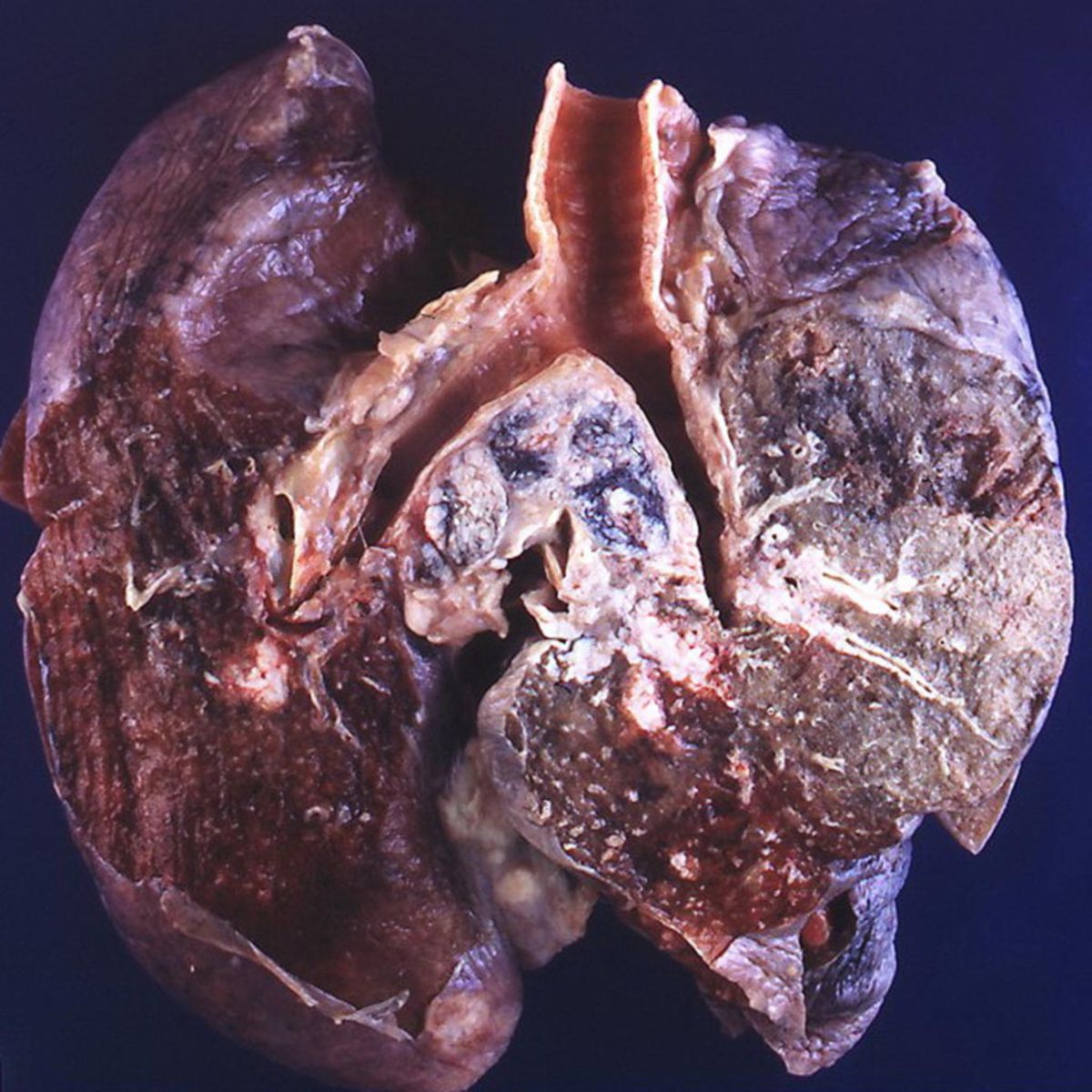
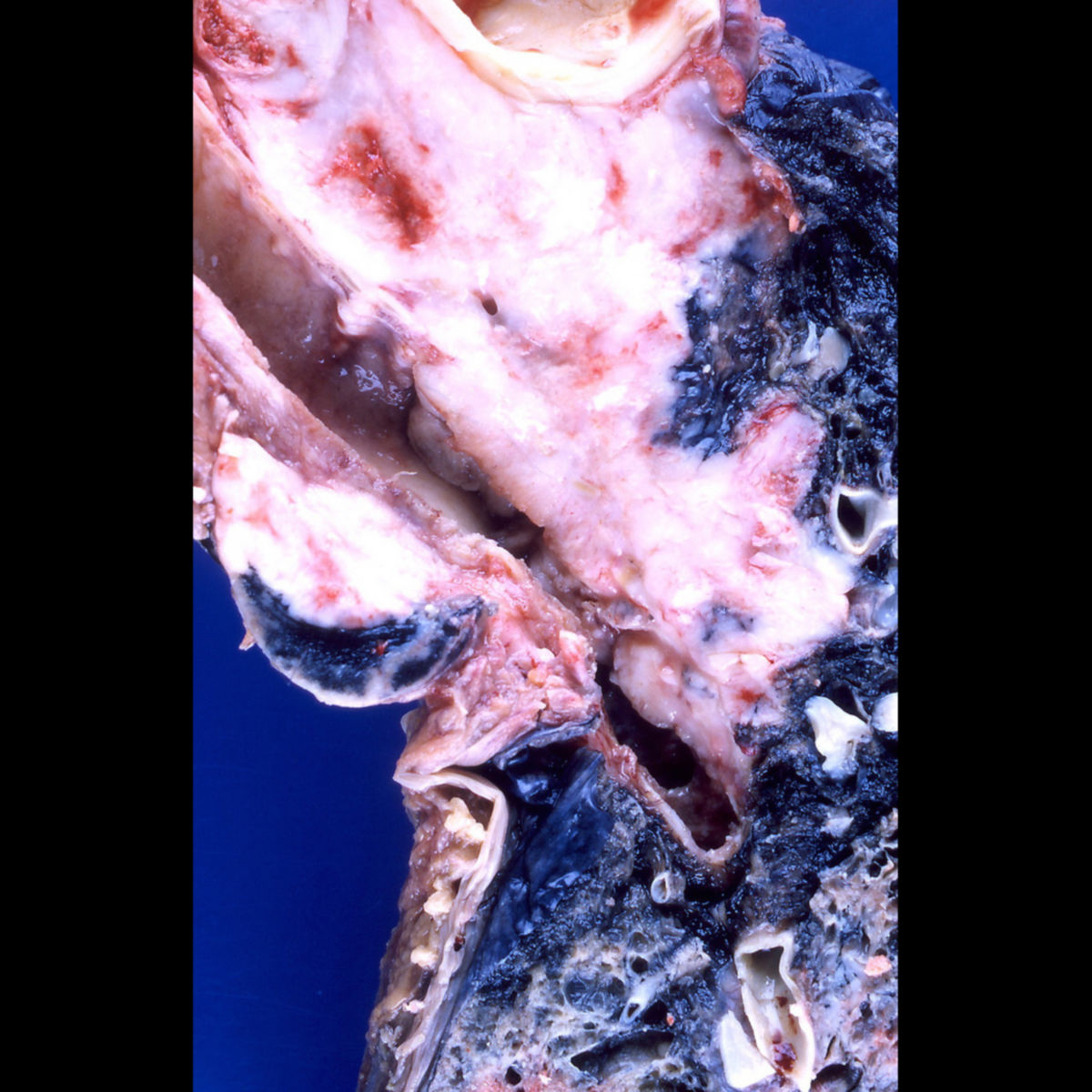
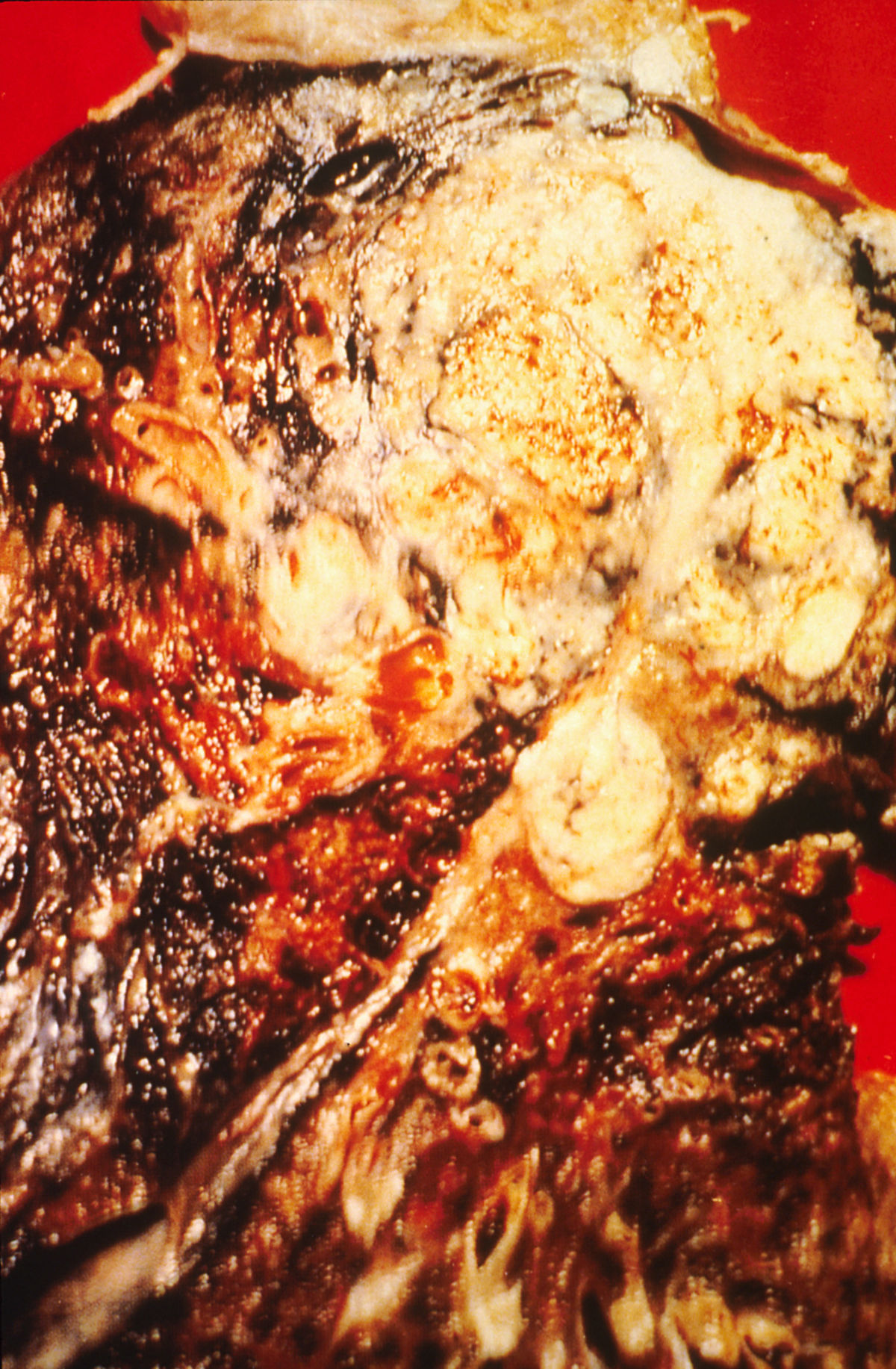
Das Karzinom ist meist zentral in der Lunge lokalisiert. Durch lymphogene und hämatogene Metastasierung kommt es frühzeitig zu einer Tumoraussaat in Gehirn, Knochen, Leber und Nebennierenrinde.
Da es sich um endokrine Zellen handelt, kann der Tumor Hormone produzieren, die unter physiologischen Umständen nicht in der Lunge gebildet werden. Dies führt zur Entstehung eines so genannten paraneoplastischen Syndroms. So kann z.B. durch die ACTH-Produktion eines kleinzelligen Bronchialkarzinoms ein Cushing-Syndrom entstehen. Eine weitere mögliche paraneoplastische Erscheinung ist das Lambert-Eaton-Syndrom (PLEMS), das in einigen Fällen lange vor der klinischen Manifestation des Tumors selbst aufttritt.
Histopathologie
Histologische Subtypen
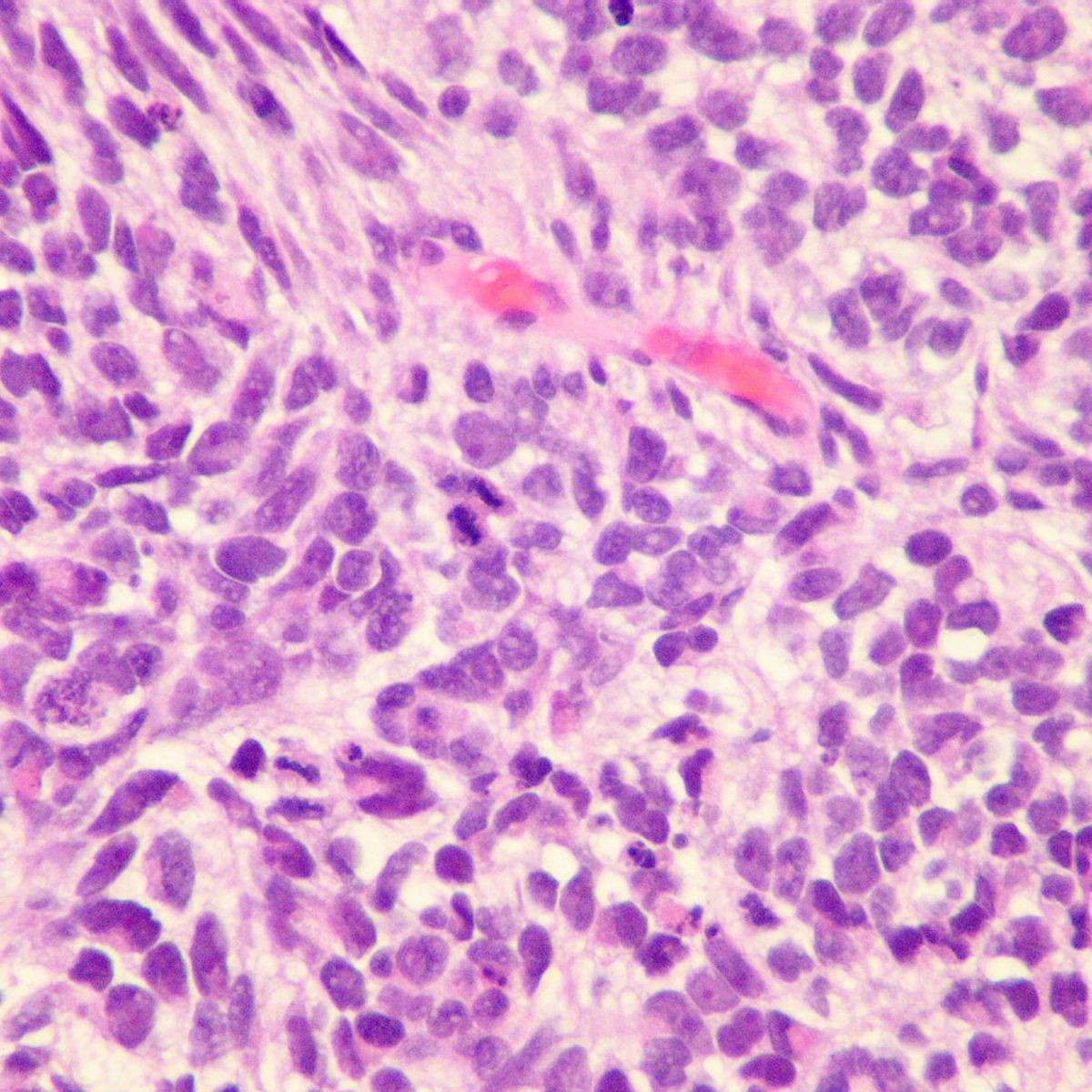
Das kleinzellige Bronchialkarzinom geht von den neuroendokrinen APUD-Zellen (Kultschitzky-Typ) aus. Man unterscheidet
- Oat-cell-Typ
- intermediärer Typ
- kombinierter Oat-cell-Typ
Molekulare Subtypen
Auf der Grundlage unterschiedlicher Genexpression kann man beim SCLC mehrere molekulare Subtypen unterscheiden. Dazu zählen:[2]
- ASCL1 (SCLC-A)
- NEUROD1 (SCLC-N)
- POU2F3 (SCLC-P)
- geringe Expression von ASCL1, NEUROD1 und POU2F3 (SCLC-I)
Die unterschiedlichen Subtypen sind auch durch ein individuelles Ansprechen auf verschiedene Substanzen der medikamentösen Tumortherapie charakterisiert.
siehe auch: Lungenkarzinom (Pathologie)
Einteilung
Beim kleinzelligen Bronchialkarzinoms ist die TNM-Klassifikation, die ansonsten für die Einteilung von Tumoren am häufigsten verwendet wird, nur bedingt geeignet. Man spricht stattdessen von
- Limited Stage: LS-SCLC, auf eine Lungenhälfte und angrenzende Lymphknoten beschränkt
- Extensive Stage: ES-SCLC, ausgebreiteter Tumor
Symptome
Die Symptomatik entspricht im Wesentlichen der anderer Bronchialkarzinome.
Beim kleinzelligen Bronchialkarzinom kommt es aufgrund seines neuroendokrinen Ursprungs zudem in ca. 10 % der Fälle zum Auftreten von paraneoplastischen Syndromen:
Diagnostik
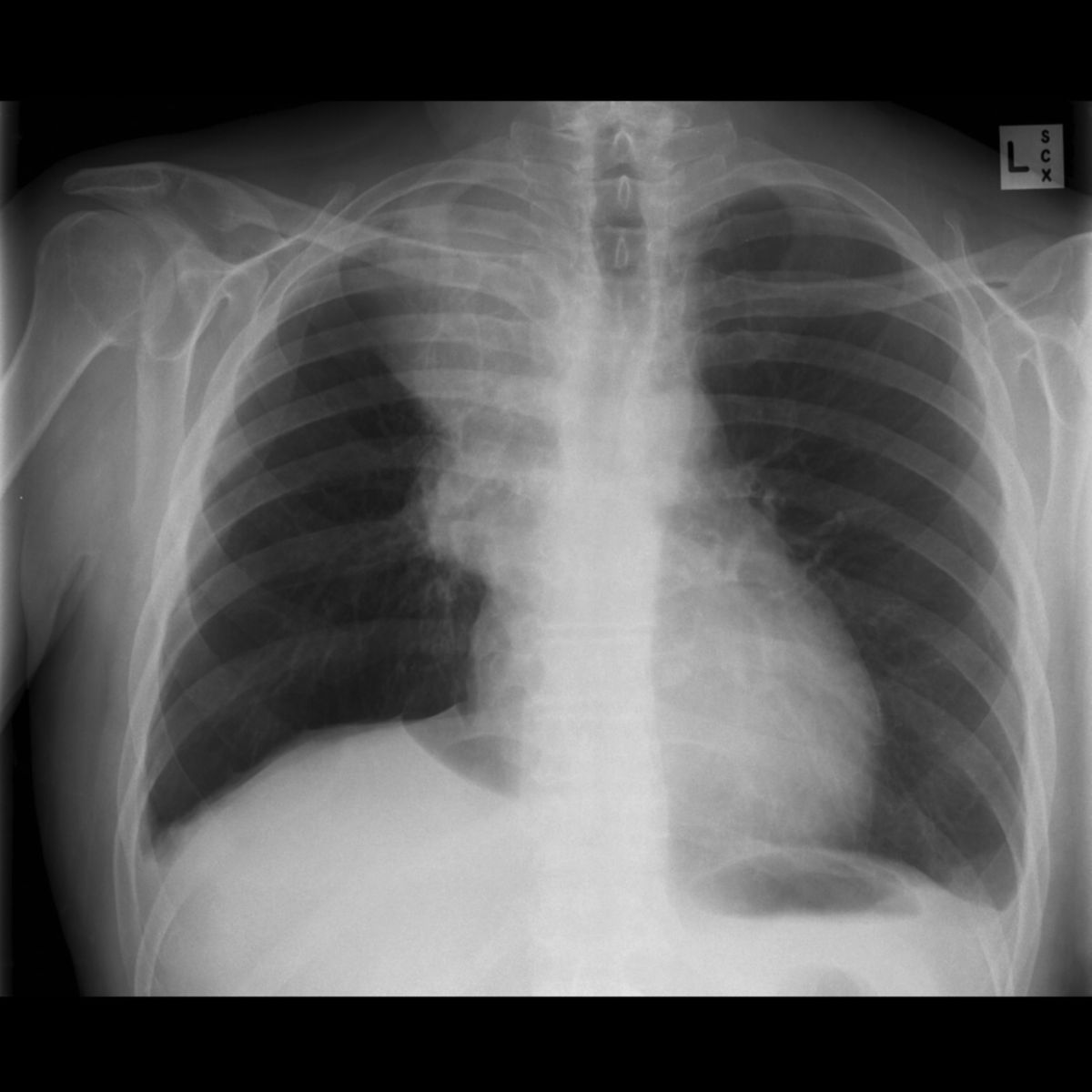
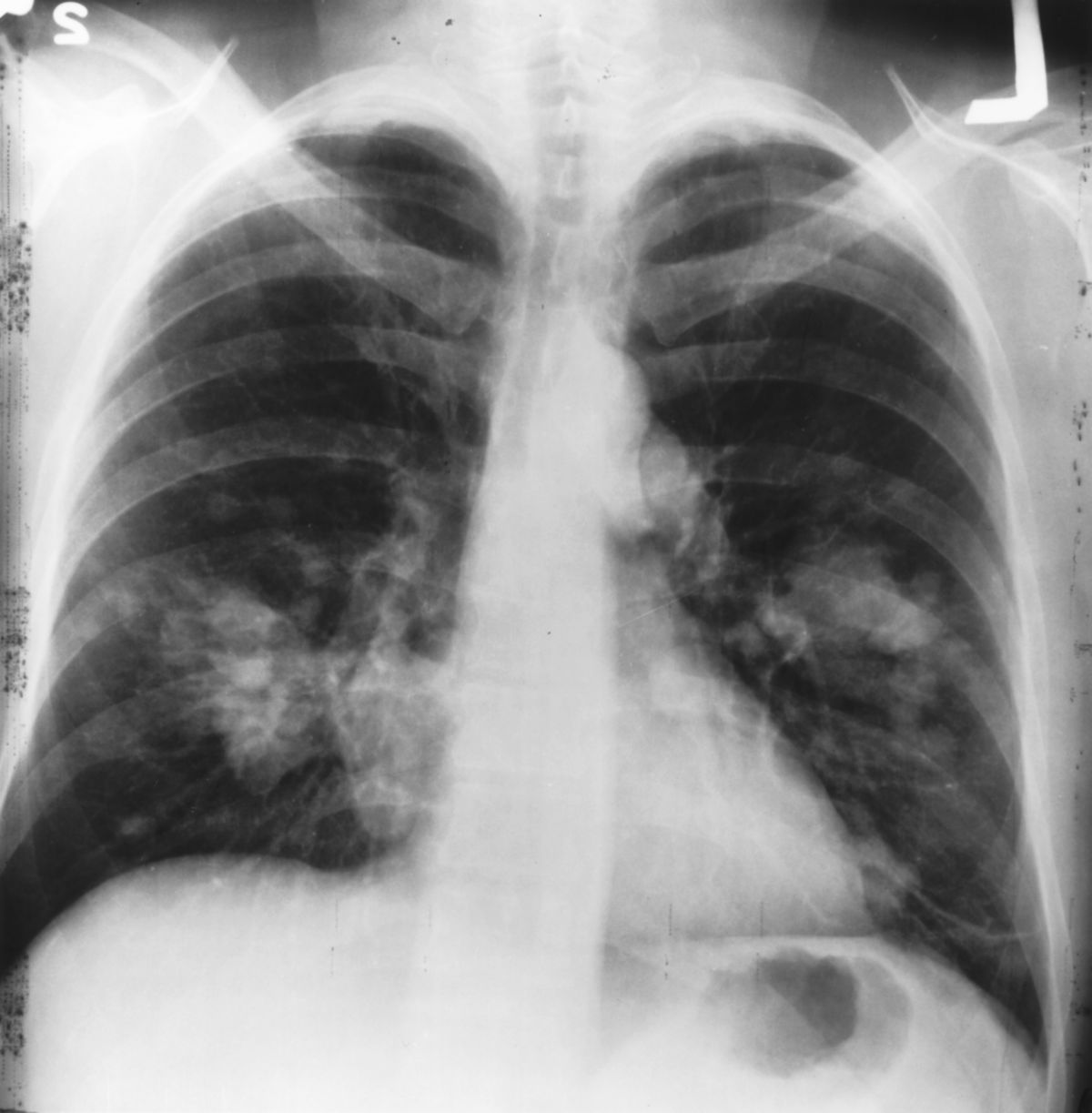
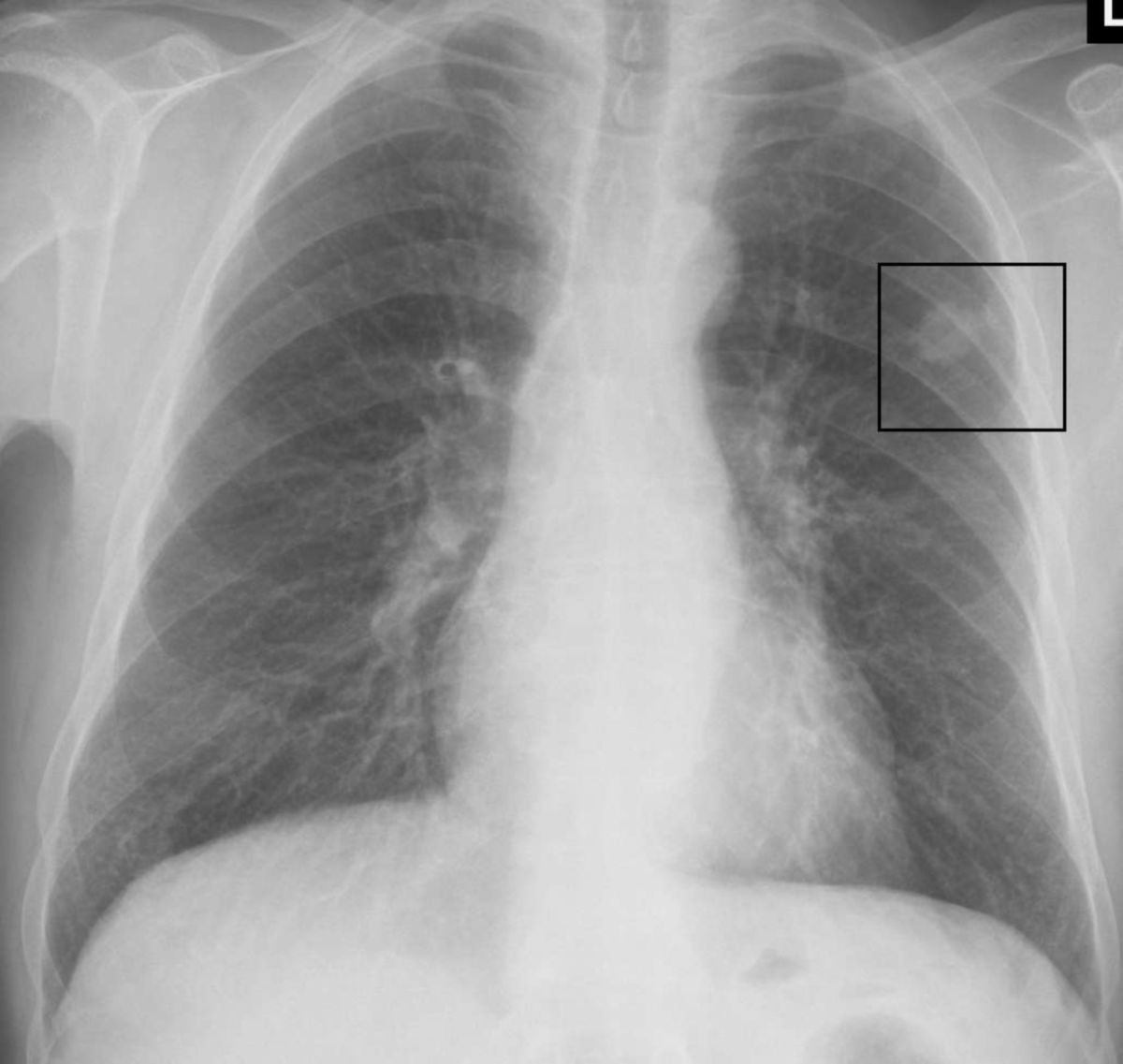
- Bildgebung (Röntgenthorax, CT, MRT)
- Bronchoskopie mit EBUS und ggf. transbronchialer Nadelaspiration
- Biopsie bzw. transthorakale Feinnadelaspiration
- Mediastinoskopie
- Tumormarker
- Neuronenspezifische Enolase (NSE)
- Pro-Gastrin-Releasing-Peptid (ProGRP)
- Staging zum Ausschluss bzw. Nachweis einer Organmetastasierung
- Abdomen-CT oder -MRT
- Schädel-MRT
- Knochenszintigraphie (oder PET-CT)
Antikörper gegen Hu-Proteine (anti-Hu, HuAb, ANNA-1) finden sich beim Anti-Hu-Syndrom.
Therapie
Das kleinzellige Bronchialkarzinom ist in der überwiegenden Zahl der Fälle leider zum Zeitpunkt der Diagnosestellung bereits metastasiert (besonders ins Gehirn, Knochen, Leber und Nebennieren) und daher oft inoperabel.
Daher ist die Prognose in der Regel schlecht und es wird meist ein palliativer Therapieansatz mit Chemotherapie bzw. Polychemotherapie - ggf. ergänzt durch eine Radiotherapie bzw. Radiochirurgie gewählt.
Limited Disease
Sie liegt in etwa ca. 30% der SCLC vor. Bis ca. T2N0M0 ist eine Tumorresektion (OP) mit kurativer Absicht möglich, die um eine adjuvante Polychemotherapie ergänzt wird. Bei begrenzten Tumorstadien, die über T2N0M0 hinausgehen, ist eine Chemotherapie mit simultaner Radiotherapie der Goldstandard.
Das gängigste Chemotherapie-Schema besteht zurzeit (2026) aus den Substanzen Cisplatin oder Carboplatin in Kombination mit Etoposid (vgl. z.B. NCCN Guideline). Darunter sind hohe Response-Raten zu erwarten, mitunter bishin zu einer vollständigen Remission. Als Zweitlinientherapie bzw. bei Rezidiven ist ein Versuch mit Topotecan möglich.
Radiotherapie: Es gilt v.a. das Mediastinum zu bestrahlen, um dortige Lymphknotenmetastasen (mit 40 Gy) zu zerstören. Eine solche Strahlendosis kann mitunter zu schwerwiegenden Komplikationen führen, u.a. zur lebensgefährlichen Lungenfibrose. Weitere mögliche unerwünschte Folgen der Radiotherapie sind eine strahleninduzierte Myokarditis bzw. Perikarditis, sowie eine Schädigung des Rücken- und Knochenmarks. Manche Folgen treten erst mehrere Monate, oder sogar mehr als 1 Jahr nach der Bestrahlung auf.
Ergänzend zur Chemotherapie und thorakalen Radiotherapie ist auch in einem frühen Stadium nach der Remission an eine prophylaktische Schädelradiatio (Radiotherapie des Schädels) zu denken, um eventuell vorhandene Hirnmetastasen zu zerstören und somit zerebrale Rezidive zu vermeiden.
Extensive Disease
Sie betrifft ca. 70% der SCLC. Im ausgedehnten Stadium ist der Therapieansatz palliativ. Es wird eine Polychemotherapie (v.a. ACO-, CEV- oder PE-Schema) oder bei Metastasen in Hirn und Knochen eine Radiotherapie durchgeführt. Eine Ergänzung der Chemotherapie um eine Immuntherapie scheint sich nach aktuellem Stand (2021) positiv auf die Überlebenszeit auszuwirken. Zum Einsatz kommen Checkpoint-Inhibitoren, wie z.B. Atezolizumab und Durvalumab.
Prognose
Im Frühstadium erwirkt eine Chemotherapie oft ein gutes Ansprechen und führt, leider oft nur zeitweise, zur Remission (Verschwinden des Tumors). Durch eine hochdosierte Chemotherapie in Kombination mit Radiotherapie können im Durchschnitt bis zu 10% der SCLC erfolgreich dauerhaft geheilt werden. Im fortgeschrittenen Stadium ist die Prognose sehr ungünstig.
Quiz
Quellen
Literatur
Bildquelle
- Bildquelle Quiz: ©Robina Weermeijer / Unsplash