Golf-gekoppelter Rezeptor
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenDefinition
Die Golf-gekoppelten-Rezeptoren sind eine Untergruppe der G-Protein-gekoppelten-Rezeptoren. Sie werden im Striatum und in sensorischen Neuronen des Riechepithels exprimiert und vermitteln ihre Wirkung über die Steigerung der intrazellulären cAMP-Konzentration.
Struktur
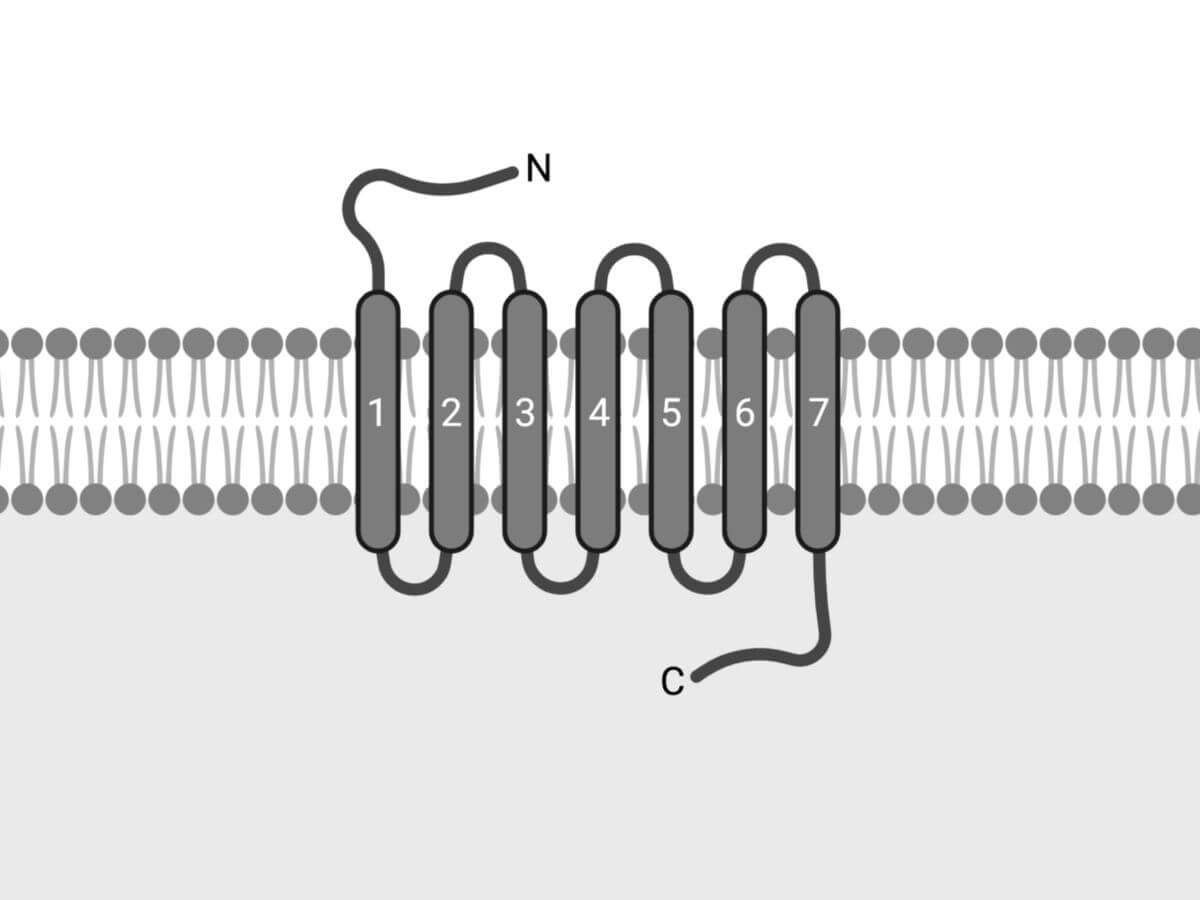
Alle G-Protein-gekoppelten-Rezeptoren bestehen aus sieben Transmembrandomänen, die α-helical angeordnet sind (heptahelikale Rezeptoren). Der N-Terminus liegt dabei extrazellulär, der C-Terminus intrazellulär.
Wirkmechanismus
Nach der Bindung eines extrazellulären Liganden (z.B. Duftstoff) wird an der α-Untereinheit des G-Proteins GDP zu GTP getauscht. Sie dissoziiert danach von der βγ-Untereinheit. Die aktivierte αolf-Untereinheit bindet anschließend an die Adenylatzyklase (AC), diese setzt nun ATP zu cAMP um.
Das gebildete cAMP aktiviert nun direkt Ionenkanäle für ein- und zweiwertige Kationen (CNG-Kanäle). Pro Aktivierung eines Rezeptors können mehrere cAMP-Moleküle gebildet werden und dementsprechend viele Kanäle geöffnet werden, was den extrem niedrigen Schwellenwert für das Wahrnehmen einiger Duftstoffe erklärt.
Im Striatum tragen Golf-gekoppelte Rezeptoren (z.B. D1-Rezeptoren) zur Regulierung der Dopamin-vermittelten Signalwege bei. Dies ist besonders wichtig für die Funktion der Basalganglien, die an der motorischen Kontrolle und am Belohnungssystem beteiligt sind.
Literatur
- Physiologie des Menschen: Mit Pathophysiologie, Springer-Lehrbuch, 32. Auflage
- Hervé, Identification of a specific assembly of the g protein golf as a critical and regulated module of dopamine and adenosine-activated cAMP pathways in the striatum, Front Neuroanat, 2011