Gaschromatographie
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: Gaschromatografie
Englisch: gas chromatography
Definition
Die Gaschromatographie, kurz GC, ist eine Methode zur Trennung von Substanzgemischen. Sie findet ihre Anwendung vor allem in der analytischen Chemie. Die Gaschromatographie ist nur für Substanzen anwendbar, die gasförmig oder unzersetzt verdampfbar sind.
Funktionsprinzip
Bei der Gaschromatographie handelt es sich um eine Sonderform der Chromatographie. Die zu analysierende Substanz, der Analyt, wird mithilfe einer gasförmigen, mobilen Phase über eine stationäre Phase (Flüssigkeitsfilm oder Feststoff) geleitet. Je nach Ausmaß der Wechselwirkungen des Analyten mit der stationären Phase wird er stark zurückgehalten oder nicht. Die Zeit, bis er das Ende der Säule erreicht, ist für diverse Stoffe individuell verschieden. Über diese sogenannte Retentionszeit kann der Analyt identifiziert werden. Auch eine quantitative Auswertung ist möglich.
Die Probe muss gasförmig oder flüchtig sein und darf beim Verdampfen nicht zerfallen. Substanzen, welche diese Voraussetzungen nicht erfüllen, können derivatisiert werden. Durch Methylierung, Silylierung, Acetylierung oder Einfügen einer Trichloracetat-Gruppe kann die Flüchtigkeit erhöht werden.
Aufbau
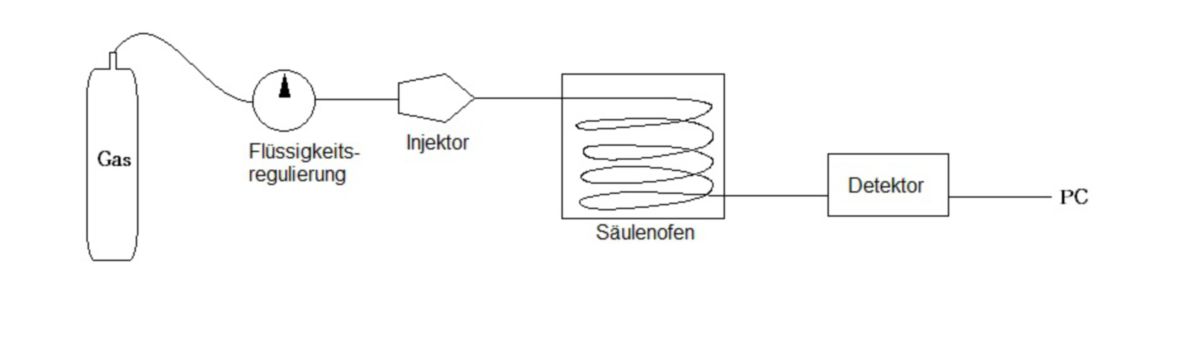
Ein Gaschromatograph ist ähnlich wie andere Chromatographen aufgebaut. Über einen Injektor wird der Analyt auf die Säule gebracht, die sich im Säulenofen befindet. Der Transport des Analyten erfolgt durch die mobile Phase, welche gasförmig ist über die stationäre Phase, die sich in der Säule befindet. Am Ende befindet sich ein Detektor.
Injektor
Der Analyt wird als wässrige Lösung injiziert. Er wird eine Mikroliterspritze aufgezogen, mit der das Septum durchstochen wird, welche den Injektor nach außen abschließt. Es gibt verschiedene Arten an Injektoren, bei denen die Substanz direkt auf die Säule aufgetragen oder zuvor verdampft wird.
Mobile Phase
Die mobile Phase ist bei der Gaschromatographie gasförmig und wird auch als Trägergas bezeichnet. Verwendet werden meist Helium, Wasserstoff oder Stickstoff, da diese Gase inert sind und so die Erfassung im Detektor nicht stören. Über die Strömungsgeschwindigkeit des Trägergases kann die Trennleistung optimiert werden.
Säule
Prinzipiell können zwei Arten an Säulen unterschieden werden:
- Gepackte Säule: Diese Säule ist mit einem feinkörnigem, porösem Sorbens gefüllt, auf welches die stationäre Phase als dünner Film aufgebracht wird. In diesem Fall ist die stationäre Phase flüssig. Die Säule hat einen Durchmesser von 3 - 8 mm und eine Länge von 0,5 - 3 m.
- Kapillarsäule: Diese Säule ist an der Innenseite mit der stationären Phase beschichtet; ansonsten ist sie hohl. In diesem Fall ist die stationäre Phase fest. Die Trennleistung einer Kapillarsäule ist bis zu 100mal höher als die einer gepackten Säule, dafür ist sie aber kürzer haltbar und kann nicht so lange verwendet werden. Der Durchmesser beträgt 0,1 - 1 mm; die Länge bis zu 30 m.
Stationäre Phase
Die stationäre Phase muss hitzestabil sein. In der Regel werden Polysiloxane, Polyethylenglykol oder Cyclodextrin verwendet. Mit Cyclodextrin ist auch eine Auftrennung von Enantiomeren möglich.
Detektor
Der Detektor detektiert den Analyten und formt dieses Signal in eine auswertbare Messgröße um. Informationen, die man aus dem Chromatogramm erhalten kann, sind die Retentionszeit, über welche die Substanz identifiert werden kann, und das Integral (Area under the curve), über welches sie quantitativ bestimmt werden kann.
Es gibt verschiedene Arten an Detektoren. Der häufigste ist der Flammenionisationsdetektor (FID), bei welchem die Probe in einer Knallgasflamme verbrannt wird. Hierbei entstehen Radikale, die zu Ionen zerfallen. Diese führen zu einer messbaren Spannung zwischen den Elektroden des Detektors. Es können alle Verbindungen detektiert werden, die beim Verbrennen in Radikale zerfallen. Dies sind alle organischen Verbindungen - die Trägergase Helium, Wasserstoff und Stickstoff sowie das Lösungsmittel Wasser zerfallen nicht in Radikale und werden nicht detektiert. Der FID ist sehr empfindlich, aber nicht selektiv.
Weitere Detektoren sind:
- Thermionischer Detektor = Stickstoff-Phosphor-Detektor (NPD). Es handelt sich um einen FID mit beheizter Alkalisalzperle (z.B. Rubidiumchlorid). Aufgrund der Alkalisalzperle werden bevorzugt stickstoff- und phopsphorhaltige Verbindungen erfasst. Viele Arzneistoffe und Gifte enthalten Stickstoff oder Phosphor; für diese ist der NPD selektiver als der FID.
- Wärmeleitfähigkeits-Detektor (WLD): Bei diesem Detektor wird die Temperaturdifferenz zwischen der Messzelle (Analyt im Trägergas) und einer Referenzzelle erfasst.
- Elektroneneinfang-Detektor (ECD): Die Probe wird durch eine Ionisationskammer mit einem Elektronenstrahler geleitet. Substanzen mit hoher Elektronenaffinität bilden Anionen, die sich im elektrischen Feld bewegen und so eine Spannung erzeugen.
- Massenspektrometer: Der Gaschromatograph kann auch an einen Massenspektrometer gekoppelt sein. Der Analysator kann über einen Jet-Separator vom Trägergas abgetrennt werden.
Anwendung
Die Gaschromatographie ist ein Verfahren mit sehr guter Trenneffizienz, das der Hochleistungsflüssigkeitschromatographie überlegen ist. Nachteil ist, dass nicht jede Substanz die Voraussetzungen zur gaschromatographischen Analyse erfüllt. Auch sind der apparative Aufwand und die damit verbundenen Kosten ein Nachteil.
Wegen der guten Trenneffizienz ist die Gaschromatographie eine Standardmethode in der chemischen, pharmazeutischen, toxikologischen und pharmakologischen Analytik.