Aldolkondensation
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonyme: Aldol-Kondensation, C-C-Verknüpfung
Englisch: aldol condensation
Definition
Unter Aldolkondensation versteht man eine Kondensationsreaktion, die in der organischen Chemie Verwendung findet. Im Verlauf dieser Reaktion bilden Aldehyde und Ketone unter Wasserabspaltung α,β-ungesättigte Carbonylverbindungen - genauer gesagt: α,β-ungesättigte Aldehyde oder Ketone.
Ablauf
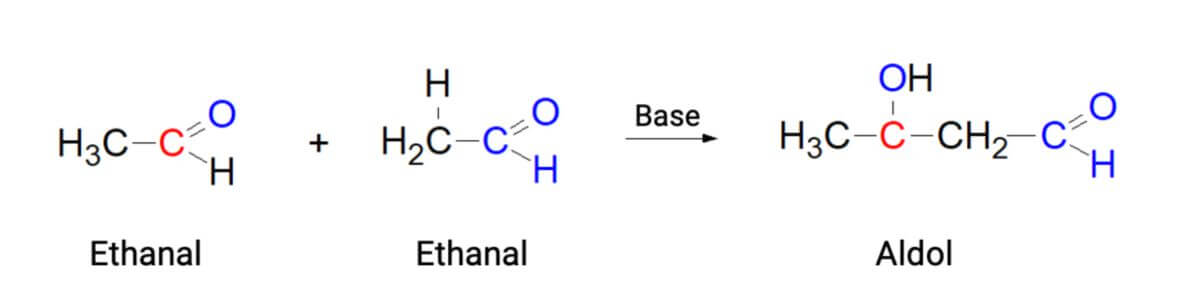
Liegt eine stark alkalische Lösung vor, so dimerisiert darin Acetaldehyd (Ethanal) zum Aldol - eine Verbindung, die je eine Aldehyd- ("-ald") und eine Hydroxygruppe ("-ol") enthält. Formal betrachtet ist ein Ethanal-Molekül an eine CO-Gruppe eines zweiten Ethanal-Moleküls addiert worden. Deshalb wird dieser Teilschritt als Aldoladdition bezeichnet. An diesen Schritt kann sich eine Wasserabspaltung (Dehydratisierung) anschließen (Aldolkondensation). Diese Reaktion läuft ähnlich mit anderen Aldehyden und Ketonen ab:
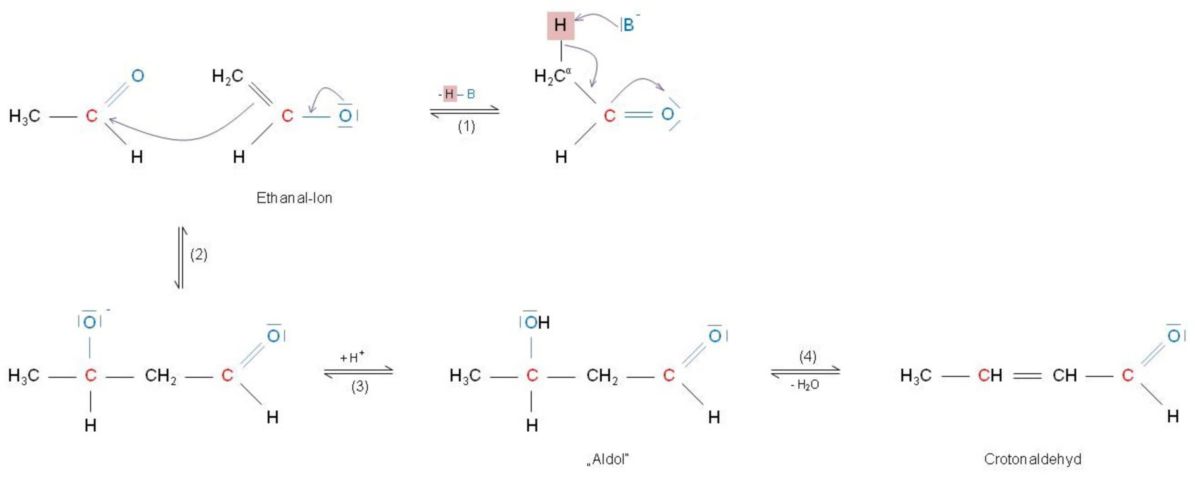
- Eines der vorliegenden aziden α-ständigen H-Atome des Ethanals wird an eine Base (z.B. OH-) abgegeben (Enolat-Bindung). In diesem Säure/Base-Gleichgewicht ist der deprotonierte Anteil gering.
- Außerdem ist das mesomeriestabilisierte Enolat-Ion ein besonders reaktives Nucleophil. Dieses reagiert mit dem α-C-Atom an der Carbonylgruppe eines unveränderten Ethanalmoleküls.
- Da eine negative Ladung vorherrscht, wird diese durch die Protonierung der Alkoxygruppe ausgeglichen. Durch diesen Teilschritt ist die Aldoladdition abgeschlossen. Alle Schritte sind bis hierhin reversibel - die Base fungiert außerdem als Katalysator.
- Häufig ist das Aldol instabil und eliminiert beim Erhitzen der Reaktionslösung Wasser (Aldolkondensation). Die daraus resultierende C=C-Doppelbindung ist zur Aldehydgruppe konjugiert. Dies kann man in der folgenden Abbildung im Crotonaldehyd erkennen. Somit ist eine α,β-ungesättigte Carbonylverbindung entstanden.
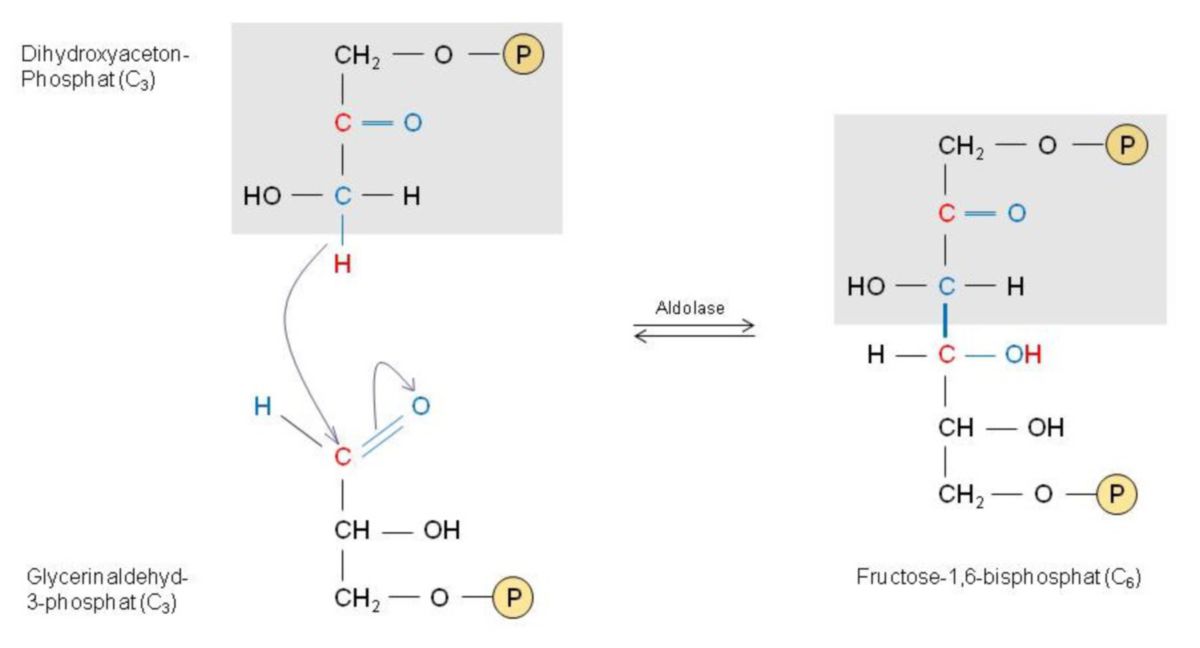
Biochemische Bedeutung
Besonders wichtig an dieser Reaktion ist, dass sie eine neue Kohenstoff-Kohlenstoff-Bindung knüpft - diese wurde in der Aldol-Formel hervorgehoben (Abb. 1 - "grau hinterlegt"). Es ist somit eine längere C-Atom-Kette enstanden - in diesem Beispiel: C2 + C2 → C4. Diese Verlängerung hat für die Synthese größerer Verbindungen große Bedeutung. Auch die Natur bedient sich an diesem Syntheseprinzip - beispielsweise beim Aufbau von Frucotse-1,6-bisphosphat aus Glycerinaldehyd- und Dihydroxyacetonphosphat. Diese Aldoladdition läuft in der Gegenwart des Enzyms Aldolase ab.