Atmungskette
Definition
Die Atmungskette ist der gemeinsame Weg, über den alle aus den verschiedensten Nährstoffen der Zelle stammenden Elektronen auf Sauerstoff übertragen werden. In der aeroben Zelle ist der molekulare Sauerstoff der letzte Elektronenakzeptor.
Aus dem Elektronentransport über die Atmungskette erzielt die Zelle ihren größten Energiegewinn, den ihr die verschiedensten Oxidationen einbringen – denn die Elektronen besitzen, wenn sie in die Atmungskette einfließen, einen relativ hohen Energiegehalt. Beim Durchfließen der Atmungskette geben sie einen erheblichen Teil ihrer Energie ab, die dann in Form von ATP (durch oxidative Phosphorylierung oder Atmungskettenphosphorylierung) konserviert wird.
Reaktionsfolgen
Die Elektronen von NADH und FADred werden zunächst auf den gemeinsamen Akzeptor Coenzym Q und dann weiter auf eine Sequenz von Cytochromen übertragen. Cytochrome sind elektronenübertragende Enzyme, die als aktive Gruppe Häm-Gruppen enthalten, die aus Porphyrin und Eisen bestehen. Sie sind rot gefärbt und ähneln in ihrer Struktur den sauerstoffübertragenden Hämoglobin in den Erythrozyten. In jedem Cytochrom-Molekül kann das Eisen in seiner zweiwertigen Form (Ferro-Form, FeII) oder in der dreiwertigen Form (Ferri-Form, FeIII) existieren. So kann das Cytochrom-Molekül in seiner FeIII-Form durch Aufnahme eines Elektrons in den reduzierten Zustand FeII überführt werden. Im reduzierten Zustand kann es das Elektron an den nächsten Überträger weitergeben und so fort. Nur das letzte Cytochrom, das Cytochrom a3 oder die Cytochromoxidase kann seine Elektronen direkt an molekularen Sauerstoff abgeben.
Der Elektronentransport über die Atmungskette lässt sich in einer Sequenz aufeinanderfolgender Reaktionen beschreiben, die durch gemeinsame Zwischenprodukte miteinander verbunden sind. Die Gesamtreaktion für die Oxidation von NADH durch molekularen Sauerstoff ergibt sich aus der Summe der Einzelreaktionen mit
Für jedes Wasserstoffatompaar, das durch jeden der vier Dehydrierungsschritte im Citratzyklus gewonnen wurde und zu einem Paar H+-Ionen wird, fließt ein Elektronenpaar in die Atmungskette und reduziert am Ende ein Atom Sauerstoff zu Wasser.
Komplexe der Atmungskette
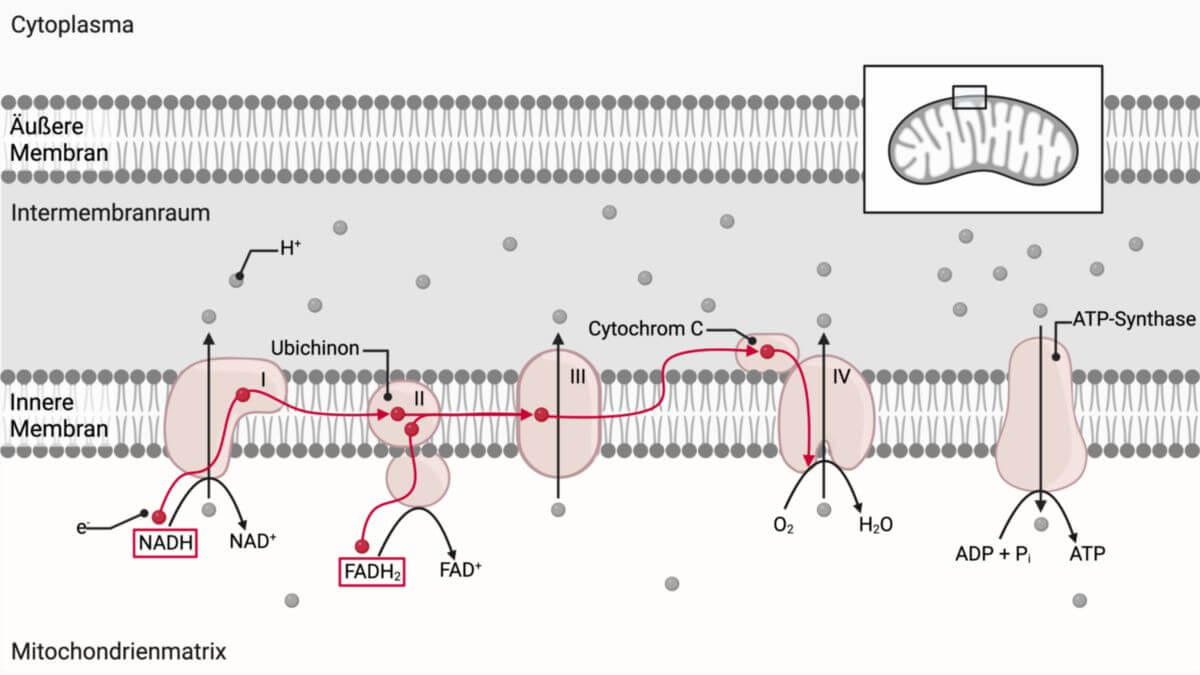
Der Mechanismus der oxidativen Phosphorylierung von ATP erfolgt an den 4 Komplexen der Atmungskette, und an einem dahinter geschalteten 5. Komplex, einem ATP-Synthase-Komplex. Diese ATP-Synthase ist als eine Art Motor zu verstehen, der durch eine protonenmotorische Kraft angetrieben wird.
Über die 4 Komplexe der Atmungskette findet ein Elektronenfluss statt, der die Energie für Protonenpumpen liefert, die H+-Ionen (Protonen) vom Matrixraum des Mitochondriums in den Intermembranraum befördern. Der genaue Mechanismus dieser Pumpen ist zurzeit noch weitgehend unverstanden. Die vier Komplexe der Atmungskette sind:
- Komplex I: NADH-Dehydrogenase
- Komplex II: Succinatdehydrogenase
- Komplex III: Cytochrom-c-Reduktase
- Komplex IV: Cytochrom-c-Oxidase
Komplex I: NADH-Dehydrogenase
Die in den katabolen Stoffwechselwegen anfallenden NADH-Moleküle werden per Malat-Aspartat-Shuttle in den Matrixraum der Mitochondrien transportiert und geben ihre Elektronen, in Form eines Hydrid-Ions (H-) an den Komplex I ab. Dieser Komplex I hat das Redoxenzym FMN (Flavinmononukleotid) als prosthetische Gruppe gebunden, das an dieser Stelle zwei Elektronen und ein Proton in Form eines Hydridions übernimmt und gleich ein Proton wieder in den Matrixraum entlässt, während es die Elektronen auf Eisen-Schwefel-Komplexe überträgt. Von den Eisen-Schwefel-Komplexen werden die beiden Elektronen auf ein Molekül Ubichinon übertragen, das dadurch zu Ubihydrochinon reduziert wird. Die für diese Reduktion nötigen Protonen werden dem Matrixraum entnommen. Die dabei frei werdende Energie dient dem Transport von 4 Protonen vom Matrixraum in den Intermembranraum.
Komplex II: Succinatdehydrogenase
Der Komplex II der Atmungskette ist gleichzeitig ein Enzym des Citratzyklus, wo er auch unter dem Namen Succinatdehydrogenase bekannt ist. Er katalysiert die Reaktion von Succinat zu Fumarat und reduziert dabei ein Molekül FAD, welches zu FADH2 reagiert. Dieses FADH2 wird, da es sich bei dem Enzym ja um den Komplex II der Atmungskette handelt, direkt in die Atmungskette eingeschleust. Die beiden Elektronen werden auf Eisen-Schwefel-Komplexe übertragen, von dort auf ein Molekül Ubichinon, das dadurch zu Ubihydrochinon reduziert. Die beiden nötigen Protonen für diese Reduktion stammen vom zuvor oxidierten FADH2. Die an diesem Komplex ablaufenden Reaktionen haben keinen Transport von Protonen zur Folge.
Komplex III: Cytochrom-c-Reduktase
An Komplex III der Atmungskette werden die zuvor reduzierten Ubichinon-Moleküle wieder regeneriert, wobei die Elektronen von Cytochrom c aufgenommen werden. Daher der Name Cytochrom-c-Reduktase. Als Elektronenüberträger dient dem Komplex III Cytochrom b, in dem die Häm-Zentren Häm-bL und Häm-bH enthalten sind. Da sowohl Cytochrom c also auch Häm jeweils nur zur Aufnahme eines Elektrons befähigt sind, aber ein komplettes Molekül Ubihydrochinon oxidiert werden muss, unterliegt der Transport von 2 Elektronen und 2 Protonen einer komplizierten Reaktionsfolge, die Q-Zyklus genannt wird. Formal werden dabei die Elektronen vom Ubihydrochinon auf Cytochrom c übertragen, sowie 2 Protonen in den Intermembranraum zurücktransportiert. Die dabei frei werdende Energie befähigt Komplex III zum Transport von 2 Protonen in den Intermembranraum.
Komplex IV: Cytochrom-c-Oxidase
Die mit Elektronen beladenen Cytochrom-c-Moleküle gelangen zum Komplex IV der Atmungskette, der diese wieder oxidiert. Daher der Name Cytochrom-c-Oxidase. An dieser Stelle vollzieht sich der Reduktionsvorgang mit dem höchsten Redox-Potential. 2 Elektronen werden auf ein halbes O2-Molekül übertragen, wobei Wasser (H2O) entsteht. Dieser als Knallgasreaktion bezeichnete Vorgang ist von allen Reduktionen in der Atmungskette der am stärksten exergone Vorgang. Als Überträger der Elektronen dienen dem Komplex IV Kupfer-, sowie Hämkomplexe. Die frei werdende Energie wird zum Transport von 4 Protonen in den Intermembranraum genutzt.
Für die Arbeit des Komplexes IV ist Sauerstoff als finaler Elektronenakzeptor unersetzlich. Dies ist der Hauptgrund, warum Lebewesen Sauerstoff zum Leben brauchen und warum ein zu geringes Angebot von Sauerstoff nicht mit dem Leben vereinbar ist.
Energetik des Elektronentransportes
Die Oxidation der verschiedenen Reduktionsäquivalente wird als "Fluss" beschrieben, weil die freie Reaktionsenthalpie der einzelnen Redox-Prozesse an den Komplexen der Atmungskette immer stärker negativ wird. Diese im Gesamten stark exergonen Prozesse befähigen die Komplexe zum Transport von insgesamt 10 Protonen pro oxidiertem NADH, bzw. von 6 Protonen pro oxidiertem FADH2. Die Oxidation von FADH2 vollzieht sich unter Ausschluss des Komplex I. Die 4 von diesem Komplex gepumpten Protonen müssen also abgezogen werden.
Die durch den Protonengradienten zustande kommende protonenmotorische Kraft treibt einen weiteren Komplex an, ATP aus ADP und Pi zu synthetisieren. Dieser Komplex trägt den Namen ATP-Synthase und stellt einen Nano-Rotationsmotor dar, der durch den Fluss der Protonen vom Intermembranraum zurück in den Matrixraum angetrieben wird. Dabei wird im Durchschnitt 1 Molekül ATP pro 3 1/3 geflossener Protonen synthetisiert.
Atmungskette und die ATP-Synthase sind aneinander strikt chemiosmotisch gekoppelt, d.h. die Funktion der ATP-Synthase ist abhängig von der Erzeugung des Protonengradienten durch die Atmungskette. Umgekehrt kommt sie – bei Ausbleiben des Elektronentransports über die Atmungskette und der Generierung des Gradienten – zum Stillstand. Den gesamten Prozess bezeichnet man als oxidative Phosphorylierung (im Gegensatz zur Substratkettenphosphorylierung). Entkoppler sind Stoffe, die den passiven Rückfluss von Protonen unter Umgehung der ATP-Synthase ermöglichen und damit die chemiosmotische Kopplung aufheben.
Zählt man alle Dehydrierungsschritte, die bei der Oxidation von Glucose stattfinden, zusammen, so kann man errechnen, dass bei der vollständigen Oxidation von einem Molekül Glucose zu Kohlendioxid und Wasser insgesamt zwölf Elektronenpaare über die Atmungskette auf molekularen Sauerstoff übertragen werden. Man kann berechnen, dass der Elektronentransport über die Atmungskette etwa -624 kcal/Mol oxidierter Glucose einbringt. Vergleicht man dies mit der Abnahme der Freien Energie, die bei einer vollständigen Verbrennung von Glucose, nämlich -686 kcal/Mol, verbunden ist, so wird deutlich, dass bei der biologischen Glucoseoxidation fast die ganze Energiemenge durch den enzymatischen Elektronentransport auf dem Wege vom ersten Elektronenakzeptor (NAD) über die Atmungskette bis zum Sauerstoff freigesetzt wird.
Klinik
Der physiologische Ablauf der Atmungskette ist z.B. bei Mitochondriopathien gestört, die durch Deletionen oder Mutationen in der mitochondrialen oder chromosomalen DNA verursacht werden.
Darüber hinaus hemmen verschiedene Substanzen die mitochondriale Atmungskette. Dazu gehören z.B.: