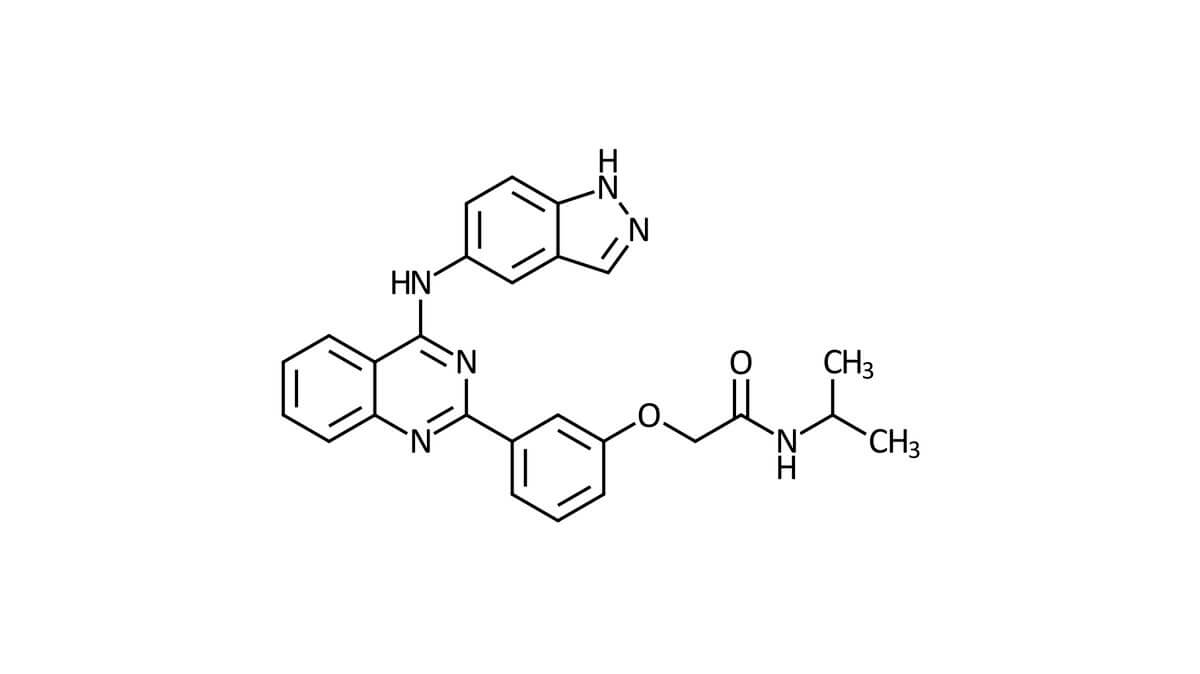
Belumosudil
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsname: Rezurock®
Englisch: belumosudil
Definition
Belumosudil ist ein Arzneistoff aus der Klasse der Serin/Threonin-Kinase-Hemmer und selektiver Inhibitor der Rho-assoziierten Proteinkinase 2 (ROCK2). Er wird zur Therapie der chronischen Graft-versus-Host-Reaktion (cGvHD) eingesetzt.
Chemie
Die Summenformel lautet C26H24N6O2, die molare Masse beträgt 452,52 g/mol.
Wirkmechanismus
Belumosudil hemmt selektiv ROCK2, eine Serin/Threonin-Kinase, die im Rahmen der chronischen GvHD zentrale proinflammatorische und profibrotische Signalwege reguliert. Durch die ROCK2-Hemmung wird die STAT3-Phosphorylierung supprimiert, was zu einer Reduktion proinflammatorischer Th17- und follikulärer T-Helferzellen führt. Gleichzeitig wird über einen STAT5-abhängigen Mechanismus die Differenzierung regulatorischer T-Zellen gefördert. Darüber hinaus hemmt Belumosudil fibrotische Signalwege, u.a. die TGF-β-induzierte Differenzierung von Fibroblasten zu Myofibroblasten, und kann so zur Reduktion von Fibrose in verschiedenen Organen beitragen.
Pharmakokinetik
Belumosudil wird nach oraler Gabe gut resorbiert. Die Einnahme zu einer Mahlzeit erhöht die systemische Exposition. Die maximale Plasmakonzentration wird in der Regel innerhalb von 1 bis 2 Stunden erreicht.
Der Wirkstoff wird überwiegend hepatisch metabolisiert, hauptsächlich über CYP3A4. Belumosudil ist zudem Substrat von Transportproteinen wie P-Glykoprotein (P-gp).
Die Eliminationshalbwertszeit beträgt etwa 19 Stunden. Die Ausscheidung erfolgt überwiegend über die Fäzes, zu einem geringeren Anteil renal. Protonenpumpeninhibitoren können die Bioverfügbarkeit verringern, vermutlich durch pH-abhängige Veränderungen der Resorption.
Indikation
Belumosudil ist indiziert zur:
- Therapie der chronischen Graft-versus-Host-Reaktion (cGvHD) bei Erwachsenen und Kindern ab 12 Jahren mit einem Körpergewicht von mindestens 40 kg, wenn andere Behandlungsoptionen einen begrenzten klinischen Nutzen bieten, nicht geeignet sind oder ausgeschöpft wurden
Die Behandlung sollte von Ärzten mit Erfahrung in der Therapie der cGvHD eingeleitet werden. Vor Therapiebeginn sind ein großes Blutbild und Leberfunktionstests erforderlich. Während der Behandlung sollten Leberwerte mindestens monatlich kontrolliert werden.
Darreichungsform
- Filmtabletten à 200 mg
Dosierung
- 1 × 200 mg täglich, unzerkaut mit Wasser zu einer Mahlzeit
- bei gleichzeitiger Anwendung mit starken CYP3A4-Induktoren (z.B. Rifampicin, Carbamazepin, Phenytoin, Johanniskraut) oder Protonenpumpeninhibitoren: 2 × 200 mg täglich zu einer Mahlzeit
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Nebenwirkungen
Häufige Nebenwirkungen der Therapie sind:
- Fatigue
- Übelkeit, Erbrechen
- Diarrhö
- Kopfschmerzen
- Erhöhte Leberenzymwerte (ALT, AST, GGT)
- Dyspnoe
- Husten
- Ödeme
- Hypertonie
- Labor: Phosphat ↓, Lymphozyten ↓
Schwerwiegende Nebenwirkungen umfassen u.a. Pneumonie, Cellulitis, bakterielle Infektionen, Hypoxie, Lungenembolie sowie Multiorganversagen.
Wechselwirkungen
Belumosudil ist ein Inhibitor von CYP3A4, P-Glykoprotein (P-gp), OATP1B1, BCRP und UGT1A1 und kann die Plasmakonzentrationen entsprechender Substrate erhöhen:
- Tacrolimus, Sirolimus (CYP3A4- und P-gp-Substrate): Konzentrationsanstieg möglich; engmaschiges Therapeutisches Drug-Monitoring bis zum Steady State empfohlen
- Rosuvastatin (OATP1B1/BCRP-Substrat), Dabigatran (P-gp-Substrat): Dosisanpassung ggf. erforderlich
- Starke CYP3A4-Induktoren verringern die Belumosudil-Exposition deutlich → Dosiserhöhung auf 2 × 200 mg/Tag (s. Dosierung); nach Absetzen des Induktors Rückkehr zur Standarddosis innerhalb eines Tages
- Protonenpumpeninhibitoren (z.B. Omeprazol, Rabeprazol): reduzieren die Belumosudil-Exposition → Dosiserhöhung auf 2 × 200 mg/Tag
- H2-Rezeptorantagonisten und Antazida: Belumosudil 2 Stunden vor oder 12 Stunden nach Einnahme dieser Arzneimittel einnehmen; keine Dosisanpassung erforderlich
Kontraindikationen
- Überempfindlichkeit gegenüber dem Wirkstoff oder einem der sonstigen Bestandteile
- Schwangerschaft und Stillzeit
- Schwere Leberinsuffizienz (Child-Pugh C) ohne Leber-GvHD
Zulassung
Belumosudil wurde im Juli 2021 von der FDA zugelassen. Die Europäische Kommission erteilte im März 2026 eine bedingte Marktzulassung; in Deutschland ist Rezurock® seit dem 1. Mai 2026 im Handel. Als bedingt zugelassenes Arzneimittel unterliegt es einer zusätzlichen Überwachungspflicht; weitere Bestätigungsdaten werden erwartet.
Quellen
- Gelbe Liste: Neueinführung Rezurock: Therapieoption bei chronischer Graft-versus-Host-Erkrankung, zuletzt abgerufen am 05.05.2026
- EMA: Rezurock, zuletzt abgerufen am 05.05.2026