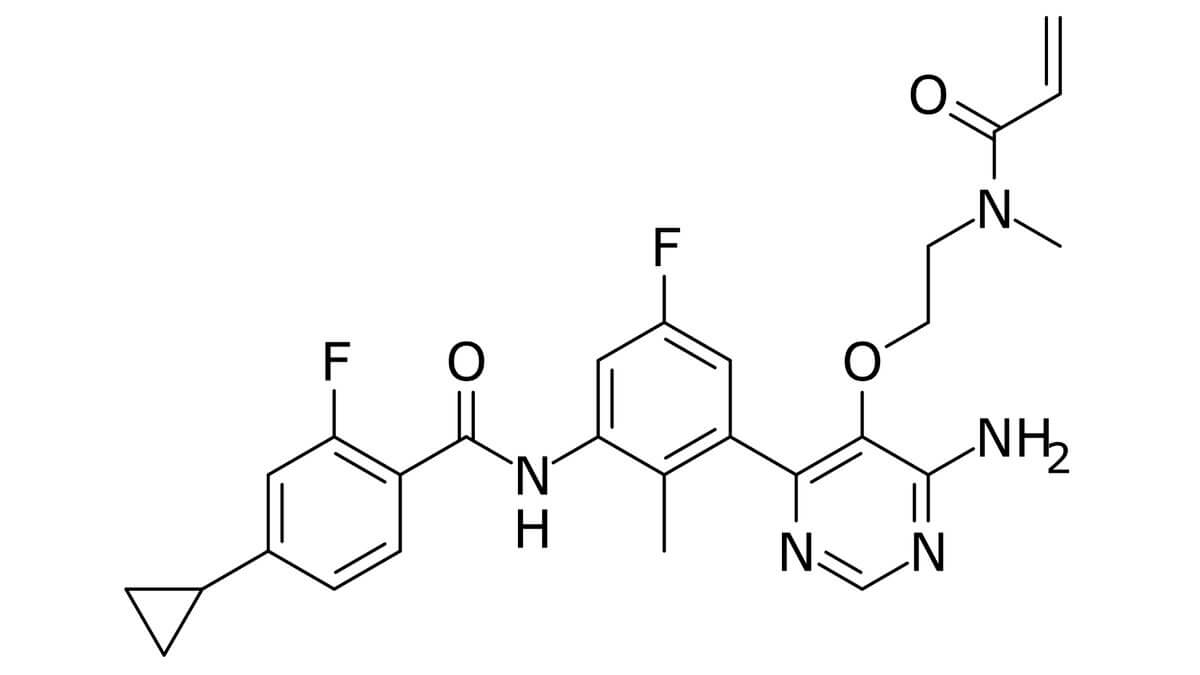
Remibrutinib
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenHandelsname: Rhapsido®
Synonym: LOU064
Englisch: remibrutinib
Definition
Remibrutinib ist ein oral verfügbarer Arzneistoff aus der Gruppe der Tyrosinkinasehemmer, der als hochselektiver, kovalenter BTK-Inhibitor die Bruton-Tyrosinkinase irreversibel hemmt. Der Wirkstoff ist zur Behandlung erwachsener Patientinnen und Patienten mit chronischer spontaner Urtikaria (csU) zugelassen, die trotz Therapie mit H1-Antihistaminika weiterhin symptomatisch sind.
Chemie
Wirkmechanismus
Remibrutinib hemmt kovalent und irreversibel die Bruton-Tyrosinkinase (BTK), ein wichtiges intrazelluläres Signalmolekül in Mastzellen, basophilen Granulozyten und B-Lymphozyten. BTK vermittelt die nachgeschalteten Signalkaskaden des hochaffinen IgE-Rezeptors (FcεRI), der sowohl in der autoallergischen (Typ-I-csU) als auch in der autoimmunen (Typ-IIb-csU) Pathogenese eine Schlüsselrolle spielt.[1]
Durch die Blockade der BTK-vermittelten Signaltransduktion werden zwei komplementäre Effekte erzielt:
- Hemmung der Degranulation von Mastzellen und basophilen Granulozyten, was die Freisetzung von Histamin und anderen proinflammatorischen Mediatoren reduziert
- Suppression der Expansion autoreaktiver B-Lymphozyten und damit Reduktion autoantikörperbasierter Mastzellenaktivierung
Pharmakokinetik
Remibrutinib ist ein oral einzunehmender, niedermolekularer Wirkstoff, der kovalent an Cystein 481 (Cys481) in der ATP-Bindungsdomäne der BTK bindet und diese irreversibel hemmt. Die mittlere inhibitorische Konzentration (IC50) im Blut liegt bei 0,023 μM. Pharmakodynamische Modellierungsstudien zeigten, dass die empfohlene Dosierung von 25 mg zweimal täglich über das gesamte Dosierungsintervall eine ausreichende Zielkinase-Besetzung aufrechterhält.[2]
Indikation
Remibrutinib ist zur Behandlung erwachsener Patienten mit chronischer spontaner Urtikaria (csU) zugelassen, die trotz Therapie mit H1-Antihistaminika weiterhin symptomatisch sind.
Darreichungsform
Remibrutinib steht als Filmtablette zur Verfügung.
Dosierung
Die empfohlene Dosis von Remibrutinib beträgt 25 mg oral zweimal täglich.
Hinweis: Diese Dosierungsangaben können Fehler enthalten. Ausschlaggebend ist die Dosierungsempfehlung in der Herstellerinformation.
Zulassung
Remibrutinib wurde am 30. September 2025 von der Food and Drug Administration (FDA) in den USA zugelassen. Die Zulassung gilt für erwachsene Patienten, die trotz Behandlung mit H1-Antihistaminika weiterhin symptomatisch sind.[3]
In Europa sprach der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur (EMA) im Februar 2026 eine positive Zulassungsempfehlung aus. Am 27. April 2026 erteilte die Europäische Kommission daraufhin die formale Marktzulassung für die EU.[4]
Quellen
- ↑ Perez et al. Treatments and Targets to Achieve Disease Control in Chronic Spontaneous Urticaria: Current and Emerging Therapeutic Options. J Inflamm Res. 2025. doi:10.2147/JIR.S546316
- ↑ Izawa et al. Remibrutinib showed a favorable safety profile and sustained efficacy in Japanese patients with chronic spontaneous urticaria over 52 weeks. Dermatol Ther (Heidelb). 2026. doi:10.1007/s13555-026-01666-5
- ↑ Novartis Pharma AG. Novartis receives FDA approval for Rhapsido® (remibrutinib), the only oral, targeted BTKi treatment for chronic spontaneous urticaria (CSU). Press Release. 2025
- ↑ Novartis Pharma AG. Novartis Rhapsido receives European Commission approval as first oral targeted treatment for chronic spontaneous urticaria. Press Release. 2026