β-Faltblatt
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: beta-Faltblatt
Englisch: beta sheet
Definition
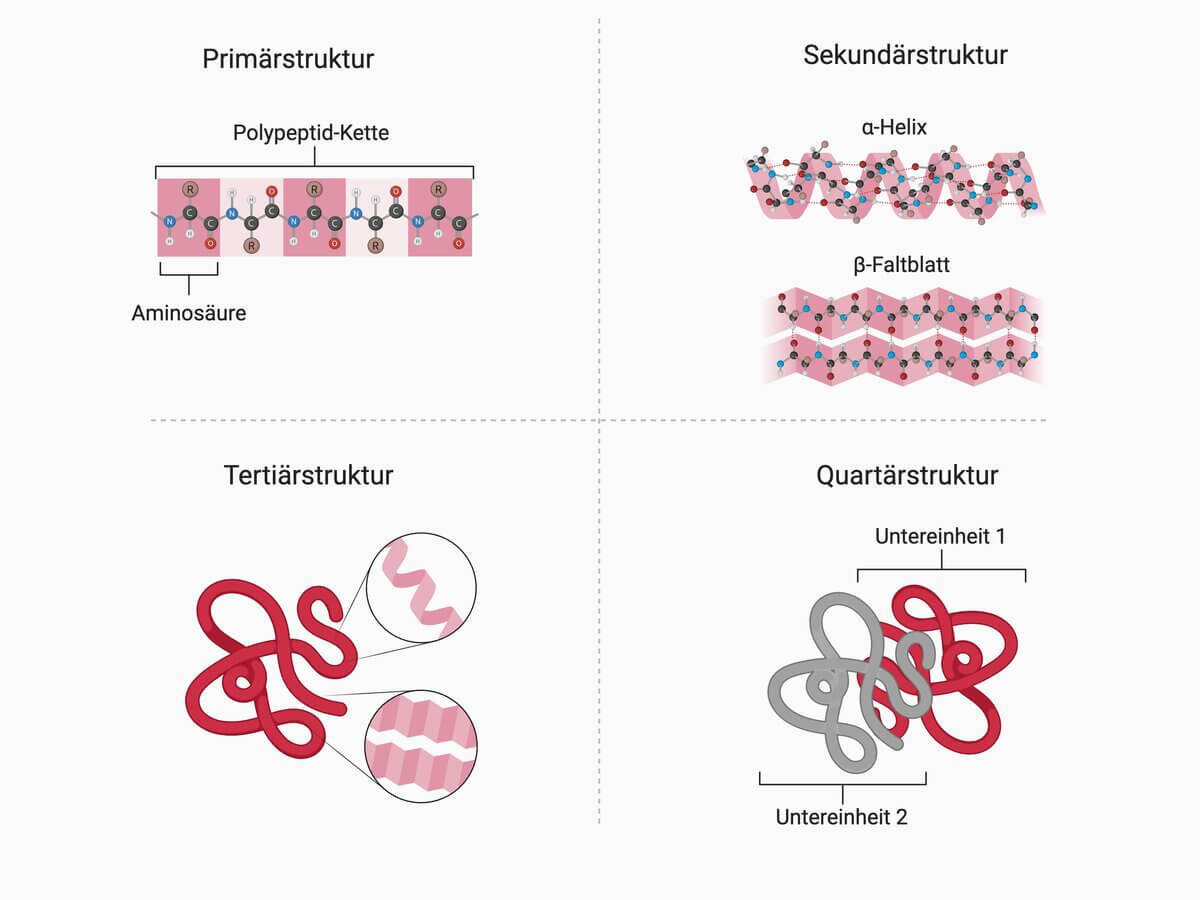
Das β-Faltblatt ist eine Sekundärstruktur von Proteinen, bei der Polypeptidketten flächenhaft in einer ziehharmonika-ähnlichen Anordnung vorliegen.
Abgrenzung
Im Gegensatz zur Alpha-Helix ist die Struktur nicht spindelförmig, sondern gestreckt.
Aufbau
Ein β-Faltblatt besteht aus zwei oder mehr sogenannten β-Strängen, die parallel oder antiparallel zueinander angeordnet sind. Die Stabilisierung erfolgt durch Wasserstoffbrückenbindungen zwischen den Peptidgruppen der benachbarten Stränge.
Der Abstand zwischen zwei Aminosäuren beträgt etwa 0,35 nm (im Vergleich zur Alpha-Helix: ca. 0,15 nm). Die Seitenketten der Aminosäuren ragen dabei alternierend ober- und unterhalb der Ebene des Faltblatts hervor.
Formen
Je nach Orientierung der Polypeptidketten unterscheidet man:
- Antiparalleles β-Faltblatt: Bei dieser Form verlaufen die Peptidketten in entgegengesetzter Richtung. Hier bilden sich Wasserstoffbrücken zwischen der CO-Gruppe einer Aminosäure und der NH-Gruppe einer zweiten Aminosäure, sowie zwischen NH-Gruppe der ersten Aminosäure und der CO-Gruppe der zweiten Aminosäure aus.
- Paralleles β-Faltblatt: Hier verlaufen die Peptidketten in gleicher Richtung. Dies hat zur Folge, dass sich nicht wie beim antiparallelen Faltblatt zwei Wasserstoffbrücken zwischen zwei gegenüberliegenden Aminosäuren ausbilden können. Stattdessen bilden sich die Wasserstoffbrücken versetzt zwischen den Aminosäuren aus.
- Gemischtes β-Faltblatt: Die meisten Faltblätter bestehen aus mehr als nur zwei Polypeptidketten. Infolgedessen können auch parallele und antiparallele Ketten vorkommen.