Hämostase
von altgriechisch: αἷμα ("haíma") - Blut; στάσις ("stasis") - Stillung
Synonyme: Blutstillung, Blutgerinnung
Englisch: h(a)emostasis, blood clotting
Definition
Als Hämostase bezeichnet man die Summe der physiologischen Prozesse, die den Stillstand einer Blutung herbeiführen.
Im erweiterten Sinn wird auch die ärztliche Blutstillung durch Gefäßnähte, Kompressionsverbände oder Hämostyptika als "Hämostase" bezeichnet.
Überblick
Die Hämostase ist eine lebenswichtige Funktion. Durch sie ist der Körper in der Lage, Schäden in Gefäßen abzudichten und somit einen Blutverlust zu reduzieren bzw. zu verhindern. Nach Verletzung kleinerer Gefäße wie Kapillaren kommt eine Blutung in der Regel bereits nach kurzer Zeit zum Stillstand. Die Hämostase kommt durch das Ineinandergreifen von drei Schritten zustande:
- Der erste ist eine Vasokonstriktion des verletzten Gefäßes, u.a. hervorgerufen durch freigesetztes Serotonin und Thromboxan mit einer nachfolgend verringerten Blutzirkulation.
- Die verlangsamte Strömungsgeschwindigkeit im verletzten Gefäß unterstützt den zweiten Schritt: die Adhäsion und Aktivierung der Thrombozyten.
- Als letzter Schritt verschließt, als Endprodukt der plasmatischen Gerinnungskaskade, ein Aggregat aus Fibrinpolymeren und Thrombozyten, den verletzten Gefäßabschnitt.
Einteilung
Man kann die drei Schritte der Hämostase in zwei Phasen einteilen, die primäre und die sekundäre Hämostase. Die verschiedenen Phasen der Hämostase laufen nicht – wie in der idealisierten Modellvorstellung – streng sequentiell ab, sondern gehen in vivo fließend ineinander über.
Primäre Hämostase
Die primäre Hämostase sorgt für eine Stillung der Blutung nach 1 bis 3 Minuten und lässt sich im klinischen Alltag durch die Bestimmung der Blutungszeit überprüfen.
Vasokonstriktion
Der erste Schritt der primären Hämostase ist eine Vasokonstriktion der verletzten Gefäße, sie wird durch bestimmte Stoffe wie z.B. Endothelin-1 ausgelöst. Sie führt zu einer Verengung der Gefäßabschnitte vor der Läsion und damit zu einer Verlangsamung des Blutstroms im Verletzungsgebiet, welche die hämodynamische Grundlage der weiteren Abläufe ist.
Thrombozytenadhäsion
Im weiteren Verlauf kommt es zu einer Thrombozytenadhäsion an bestimmte Komponenten des verletzten Gefäßendothels, z.B. Kollagen und Fibronektin. Sie wird über Glykoprotein Ib (GPIb) bzw. Glykoprotein Ic/IIa (GPIc/IIa) vermittelt. GPIb ist der wichtigste Adhäsionsrezeptor für den von-Willebrand-Faktor (vWF), der das Bindeglied zwischen den Thrombozyten und dem subendothelialen Kollagen ist. Die Adhäsion der Thrombozyten sorgt für eine erste, dünne Bedeckung der Wunde.
Thrombozytenaggregation
Glykoprotein IIb/IIIa wird erst nach Aktivierung der Thrombozyten exprimiert. Es bindet vWF, Fibronektin sowie Fibrinogen und fördert somit die Thrombozytenaggregation. Nach überschwelliger Aktivierung durch eine Fremdoberfläche oder bestimmte Agonisten, wie Kollagen, Thrombin, ADP, Adrenalin u.v.a. verändern die Plättchen ihre Form. Sie gehen von einer "passiven" Scheibenform in eine "aktive", sphärische Form mit unterschiedlich langen Pseudopodien über.
Die stimulierte Plättchen-Phospholipoprotein-Oberfläche katalysiert die weitere Anlagerung von Thrombozyten und die Aktivierung von Faktor X. Thrombin, Thromboxan und ADP führen synergistisch zu einem weiteren Formwandel sowie weiteren Freisetzungsreaktionen und Aggregation an der Verletzungsstelle. Diese Aggregation der Thrombozyten ist zunächst reversibel, wird jedoch nach Erreichen einer bestimmten Konzentration der Freisetzungsprodukte irreversibel. Es folgt eine visköse Metamorphose der Thrombozyten mit Verlust der Phospholipidmembran. Parallel dazu werden die Thrombozyten durch Fibrinogen vernetzt und zu einem Abscheidungsthrombus zusammenfügt.
Sekundäre Hämostase
Die sekundäre Hämostase ist die eigentliche Blutgerinnung. Sie nimmt etwa 6 bis 10 Minuten in Anspruch und führt zur Ausbildung eines festen Fasernetzes aus Fibrin, in das Thrombozyten und Erythrozyten eingebettet sind. Es stellt sich makroskopisch als Thrombus dar. Man unterscheidet nach Morawitz drei Phasen:
- Aktivierungsphase
- Koagulationsphase
- Retraktionsphase
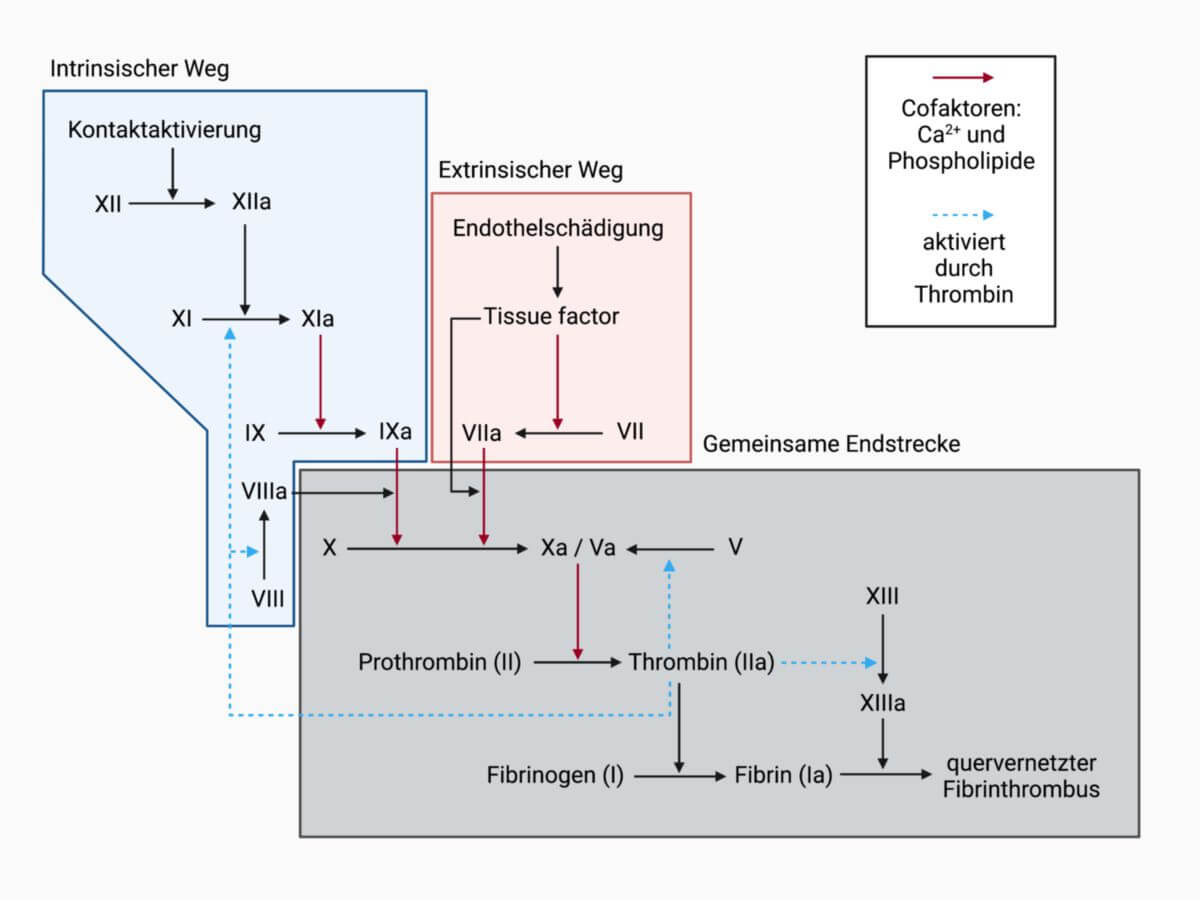
Nach dem klassischen Modell kann man zwei Systeme differenzieren, die intrinsische und die extrinsische Gerinnungskaskade. Bei beiden Systemen kommen die Gerinnungsfaktoren zum Tragen, die in einem treppenartigen Ablauf jeweils die Aktivierung eines oder mehrerer nächster Faktoren induzieren.
Der Endschritt der extrinsischen wie der intrinsischen plasmatischen Gerinnungskaskade ist die Fibrinpolymerisation. Beide Systeme münden über die Bildung von Faktor X letztendlich in die Thrombinbildung (Faktor II), was wiederum die Entstehung von Fibrinogen und dessen Polymerisation anregt.
Aus didaktischen Gründen wird die plasmatische Gerinnung weiterhin in eine extrinsische und eine intrinsische Gerinnungskaskade unterteilt. Es zeigen sich aber zunehmend mehr Wechselwirkungen der beiden Systeme.
Intrinsisches System
Das intrinsische System stellt überwiegend die Reaktionen an der Oberfläche aktivierter Thrombozyten dar und unterhält die weitergehende Fibrinbildung. Der intrinsische Weg spielt im klinischen Alltag eine große Rolle, da er eine Gerinnung ohne Freilegung der subendothelial gelegenen Strukturen, beispielsweise durch liegenden zentralen Venenkatheter oder künstlichen Herzklappen, triggert.
Der intrinsische Weg der Blutgerinnung startet über den Hageman-Faktor (Faktor XII). Seine Aktivierung wird über eine Bindung an negativ geladenen Oberflächen initiiert. Des Weiteren unterstützt er über aktives Kallikrein seine eigene Aktivierung. Faktor XI wird durch den aktivierten Hageman-Faktor und über positive Rückkopplung durch Thrombin aktiviert. In der Folge wird Faktor IX durch den aktivierten Faktor XIa aktiviert. Dieser bildet nun mit Faktor VIIIa einen Enzymkomplex, der intrinsischer Tenasekomplex oder Xase-Komplex genannt wird. Er aktiviert in der Folge Faktor X und mündet damit in die gemeinsame Endstrecke der Gerinnungswege.
Faktor VIII ist ein multimeres Glykoprotein, das in Endothelzellen und Megakaryozyten synthetisiert wird und sich im Plasma und in Thrombozyten nachweisen lässt. Er dient der intrinsischen Gerinnungskaskade als Katalysator bei der Aktivierung von Faktor X um bis zu drei Zehnerpotenzen und mehr. Um diese Funktion ausüben zu können, muss Faktor VIII mithilfe von Thrombin aus seinem Kofaktor und Trägerprotein, dem von-Willebrand-Faktor, herausgelöst werden.
Der von-Willebrand-Faktor führt den Faktor VIII an den Ort der Blutung und stellt eine Verbindung zwischen den Glykoproteinrezeptoren GPIIa und GPIIb/IIIa der Thrombozyten und dem Endothel her.
Extrinsisches System
Das auslösende Ereignis ist meist geschädigtes Endothel. Das extrinsische System reagiert durch Kontakt mit extravaskulärem Gewebsthromboplastin (Tissue Factor) mit einer Aktivierung des Faktor VII zu Faktor VIIa, der zusammen mit Kalzium den Faktor X zu Faktor Xa aktiviert. Hier mündet die extrinsische Gerinnungskaskade, zusammen mit der intrinsischen Gerinnungskaskade, in den gemeinsamen Endweg der plasmatischen Gerinnungskaskade
Gemeinsame Endstrecke der plasmatischen Gerinnung
Ab der Bildung von Faktor Xa verlaufen beide Schenkel der Gerinnungskaskade gemeinsam über die Verbindung von Faktor Xa und Faktor Va, der als Prothrombinase-Komplex bezeichnet wird. Dieser spaltet in Anwesenheit von Kalzium Prothrombin zu Thrombin (Faktor IIa), das sich von der Thrombozytenoberfläche löst und nun Fibrinogen zu Fibrinmonomeren spaltet. Die gleichzeitige Aktivierung von Faktor XIII durch Thrombin sorgt für die Quervernetzung der Fibrinmonomere zu Polymeren.
Des Weiteren stößt Thrombin durch die Aktivierung des Faktors XI die intrinsische Gerinnungskaskade an und fördert durch Aktivierung von Faktor V die Entstehung von mehr Prothrombinase-Komplexen.
Anschlussreaktionen
Wenige Minuten nach Bildung des fertigen Thrombus ziehen sich die Wundränder im Rahmen der Retraktion zusammen. Aus dem Blutkuchen wird dabei Serum herausgepresst, das mit dem Blutstrom abtransportiert wird. Der Abbau des Fibringerüsts erfolgt durch die Fibrinolyse.
Klinik
Störungen der Hämostase können sich sowohl als Neigung zur übermäßigen als auch in einer unzureichenden Hämostase äußern. Als Ursachen kommen Defekte auf der Ebene der Thrombozyten, der plasmatischen Gerinnung oder der Fibrinolyse infrage.
Erkrankungen mit einer erhöhten Blutungsneigung werden unter dem Begriff "Hämorrhagische Diathese" subsumiert. Krankheiten mit einer überschießenden Gerinnung werden unter dem Begriff "Thrombophilie" zusammengefasst.
Die Überprüfung der Blutgerinnung beim Patienten erfolgt im klinischen Alltag durch eine Reihe verschiedener Labortests, welche die Konzentration einzelner Gerinnungsfaktoren oder das intrinsische und/oder extrinsische System überprüfen, z.B.:
- Prothrombinzeit (Quick-Wert)
- Partielle Thromboplastinzeit (PTT)
- Thrombinzeit (TZ)
- Plasmafibrinogen
- International Normalized Ratio
- Thrombelastometrie
Podcast

Quiz
Skripte
Bildquelle
- Bildquelle Podcast: © Midjourney
- Bildquelle Quiz: © Testalize.me / Unsplash