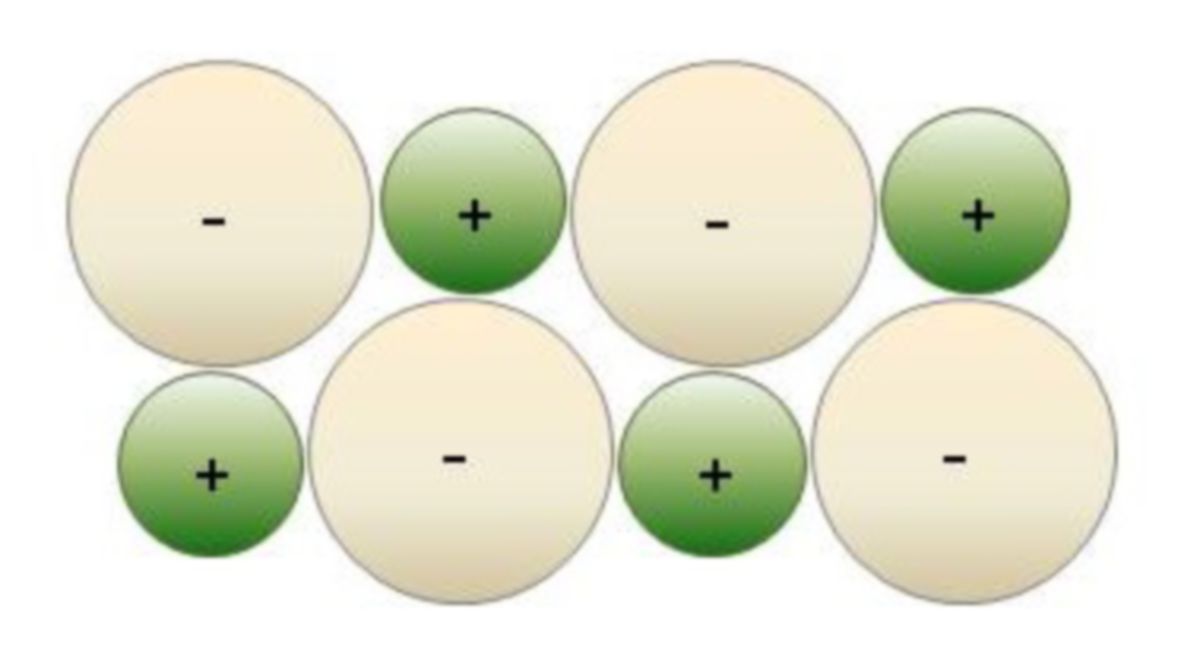
Ionengitter
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: Ionenkristall
Englisch: ionic crystal
Definition
Unter einem Ionengitter versteht man in der Physik und Chemie die regelmäßige räumliche Anordnung von Kationen und Anionen in einem homogenen Feststoff. Der Zusammenhang innerhalb des Gitterverbandes wird durch ungerichtete Ionenbindungen gewährleistet.
siehe auch: Ionenbindung
Hintergrund
Durch elektrostatische Anziehung werden positiv und negativ geladene Ionen zusammengehalten. Da es sich um starke Anziehungskräfte handelt, weisen Ionenkristalle hohe Schmelzpunkte auf. Zudem sind sie hart und spröde. Verschiebt man eine Ebene von Ionen gegen eine andere (darunterliegende), geraten Ionen mit gleicher Ladung nebeneinander, weshalb augenblicklich ein Abstoßungsvorgang eintritt - der Kristall zerbricht.
Leitfähigkeit
Ionenverbindungen sind gute elektrische Leiter, solange sie sich in einem geschmolzenen oder gelösten Zustand befinden. Befindet sich eine solche Verbindung im kristallinen Zustand, nimmt die Leitfähigkeit merkbar ab.
Literatur
- "Chemie" - Charles E. Mortimer, Ulrich Müller, Thieme-Verlag, 10. Auflage
- "Chemie für Mediziner" - A. Zeeck et. al., Urban & Fischer-Verlag, 7. Auflage