Nichtkompetitive Hemmung
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenSynonym: nicht-kompetitive Hemmung
Englisch: non-competitive inhibition
Definition
Die nichtkompetitive Hemmung ist eine Form der Enzymhemmung, bei der die Bindung des Inhibitors die Substratbindung nicht beeinträchtigt. Der Inhibitor bindet an eine vom aktiven Zentrum räumlich getrennte Bindungsstelle. Dadurch wird die katalytische Aktivität des Enzyms herabgesetzt, ohne die Affinität des Enzyms zum Substrat zu verändern.
siehe auch: kompetitive Hemmung
Hintergrund
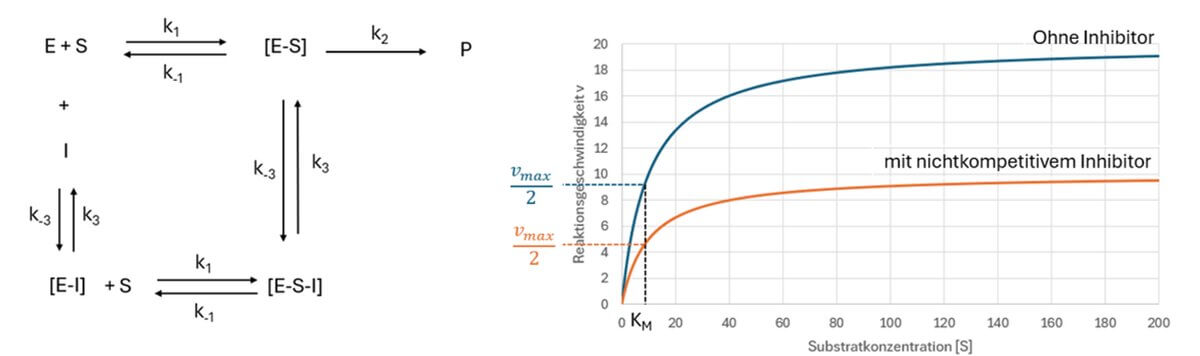
Bei der nichtkompetitiven Hemmung kann der Inhibitor sowohl an das freie Enzym (E) als auch an den Enzym-Substrat-Komplex [E-S] binden. Es können somit folgende Komplexe entstehen:
- Enzym-Substrat-Komplex [E-S]
- Enzym-Inhibitor-Komplex [E-I]
- Enzym-Substrat-Inhibitor-Komplex [E-S-I]
Das Produkt kann jedoch nur ausgehend vom Enzym-Substrat-Komplex gebildet werden.
Kinetik
Bei der reinen nichtkompetitiven Hemmung ist die Maximalgeschwindigkeit (Vmax) der Enzymreaktion herabgesetzt, während die Michaelis-Menten-Konstante (Km) unverändert bleibt. Dies beruht darauf, dass aus dem Enzym-Inhibitor-Komplex kein Produkt gebildet werden kann. Der Inhibitor verringert somit die Konzentration des katalytisch aktiven Enzyms, wodurch die Reaktionsgeschwindigkeit bei gegebener Substratkonzentration sinkt. Eine Erhöhung der Substratkonzentration kann die Hemmung nicht aufheben, da funktionsfähige Enzyme durch den Inhibitor blockiert sind.
Mathematisch lässt sich die Reaktionsgeschwindigkeit eines Enzyms in Gegenwart eines nichtkompetitiven Inhibitors mit der Michaelis-Menten-Gleichung beschreiben. Dabei wird lediglich Vmax durch die geänderte ("apparente") Maximalgeschwindigkeit Vmaxapp ersetzt, wobei Ki die Inhibitorkonstante ist:
Gemischte Hemmung
Die nichtkompetitive Hemmung ist ein Sonderfall der gemischten Hemmung.
- Bei der nichtkompetitiven Hemmung bindet der Inhibitor mit gleicher Affinität an das Enzym und den Enzym-Substrat-Komplex
- Bei der gemischten Hemmung unterscheidet sich diese Affinität → Km kann sich verändern und es wird entweder mehr Enzym-Inhibitor-Komplex oder mehr Enzym-Substrat-Inhibitor-Komplex gebildet
Allosterische Hemmung
Die allosterische Hemmung ist ein Spezialfall der nichtkompetitiven Hemmung. Hier führt die Bindung des Inhibitors an eine regulatorische Stelle des Enzyms zu einer Konformationsänderung. Das Substrat kann somit nur erschwert oder gar nicht an das aktive Zentrum binden.
Beispiele
- Schwermetalle: z.B. Quecksilber, Silber, Blei, Cadmium, Zinn binden i.d.R. an negative Stellen der Aminosäureketten von Proteinen
- Cyanid hemmt die Cytochrom-c-Oxidase nichtkompetitiv
- Fluorid bindet u.a. die Enolase
Literatur
- Berg et al., Stryer Biochemie, 7. Auflage, Springer, 2013






![{\displaystyle v_{max}app={\frac {v_{max}}{1+{\frac {[I]}{K_{I}}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5d2e07b02cdf76baffda6762f8b688f9fbfce831)