Unkompetitive Hemmung
Trainier deine Lernmuskeln!
Mit Flash Cards, Quiz und mehr
LoslegenDefinition
Als unkompetitive Hemmung bezeichnet man in der Biochemie eine Form der reversiblen Hemmung, bei der ein Inhibitor ausschließlich an den Enzym-Substrat-Komplex und nicht an das freie Enzym bindet. Der Inhibitor stabilisiert den Enzym-Substrat-Komplex und verhindert dadurch die Produktbildung.
Abgrenzung
Unkompetitive Hemmung unterscheidet sich von kompetitiver und nichtkompetitiver Hemmung dadurch, dass der Inhibitor keine Affinität zum freien Enzym besitzt und seine Wirkung nur im Beisein des Substrats entfalten kann.
Kinetik
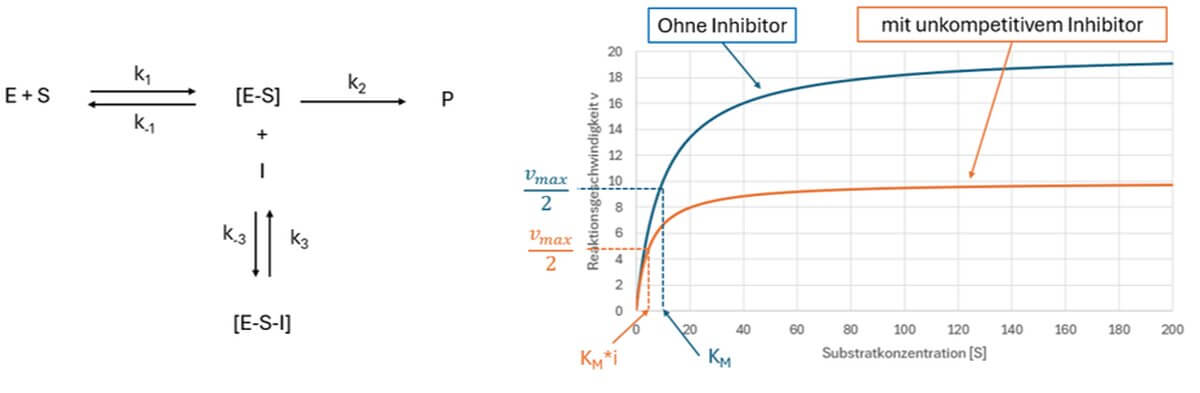
Bei der unkompetitiven Hemmung werden die maximale Reaktionsgeschwindigkeit (Vmax) und die Michaelis-Menten-Konstante (Km) proportional reduziert, da die Bildung des Produktes aus dem ES-Komplex gehemmt wird. Die Maximalgeschwindigkeit wird – analog zur nichtkompetitiven Hemmung – reduziert, da weniger freies Enzym vorliegt, das eine Reaktion katalysieren kann.
Der Km-Wert wird aufgrund der veränderten Lage des chemischen Gleichgewichtes verringert. Der Inhibitor entzieht dem Gleichgewicht den reinen Enzym-Substrat-Komplex, weshalb wegen des Prinzips des kleinsten Zwanges mehr Enzym-Substrat-Komplex nachgebildet wird. Die Verringerung des Km-Werts spielt eine erhöhte Affinität des Enzyms gegenüber dem Substrat vor. Charakteristisch ist, dass die Hemmwirkung mit steigender Substratkonzentration zunimmt, da mehr ES-Komplexe gebildet werden, an die der Inhibitor binden kann.
Aus mathematischer Sicht kann die Kinetik in Gegenwart eines unkompetitiven Inhibitors beschrieben werden, indem in der Michaelis-Menten-Gleichung eine Konstante eingeführt wird:
vmax = Maximalgeschwindigkeit, [S]0 = Substratkonzentration zu Beginn, KM = Michaelis-Menten-Konstante und k3 und k-3 = Reaktionsgeschwindigkeitskonstanten zwischen [E-S]+I und [E-S-I] (siehe Abbildung).
Literatur
- Berg et al., Stryer Biochemie, 7. Auflage, Springer, 2013






![{\displaystyle v_{max}=v_{max}{\frac {[S]_{0}}{K_{M}+i*S_{0}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1342a9832f8236ec138b0047d1eb262eb9ec4210)
