V-ATPase
Synonym: Vakuoläre H+-ATPase
Englisch: Vacuolar-type H+-ATPase, V-ATPase
Definition
V-ATPasen sind Transportproteine, die H+-Ionen durch Hydrolyse von ATP in membranumschlossene Organellen eukaryotischer Zellen schleusen. Hierdurch können diese ein saures Milieu gegenüber dem Rest der Zelle aufrechterhalten.
Vorkommen
V-ATPasen können in verschiedenen Kompartimenten eukaryotischer Zellen gefunden werden, u.a. in:
Struktur
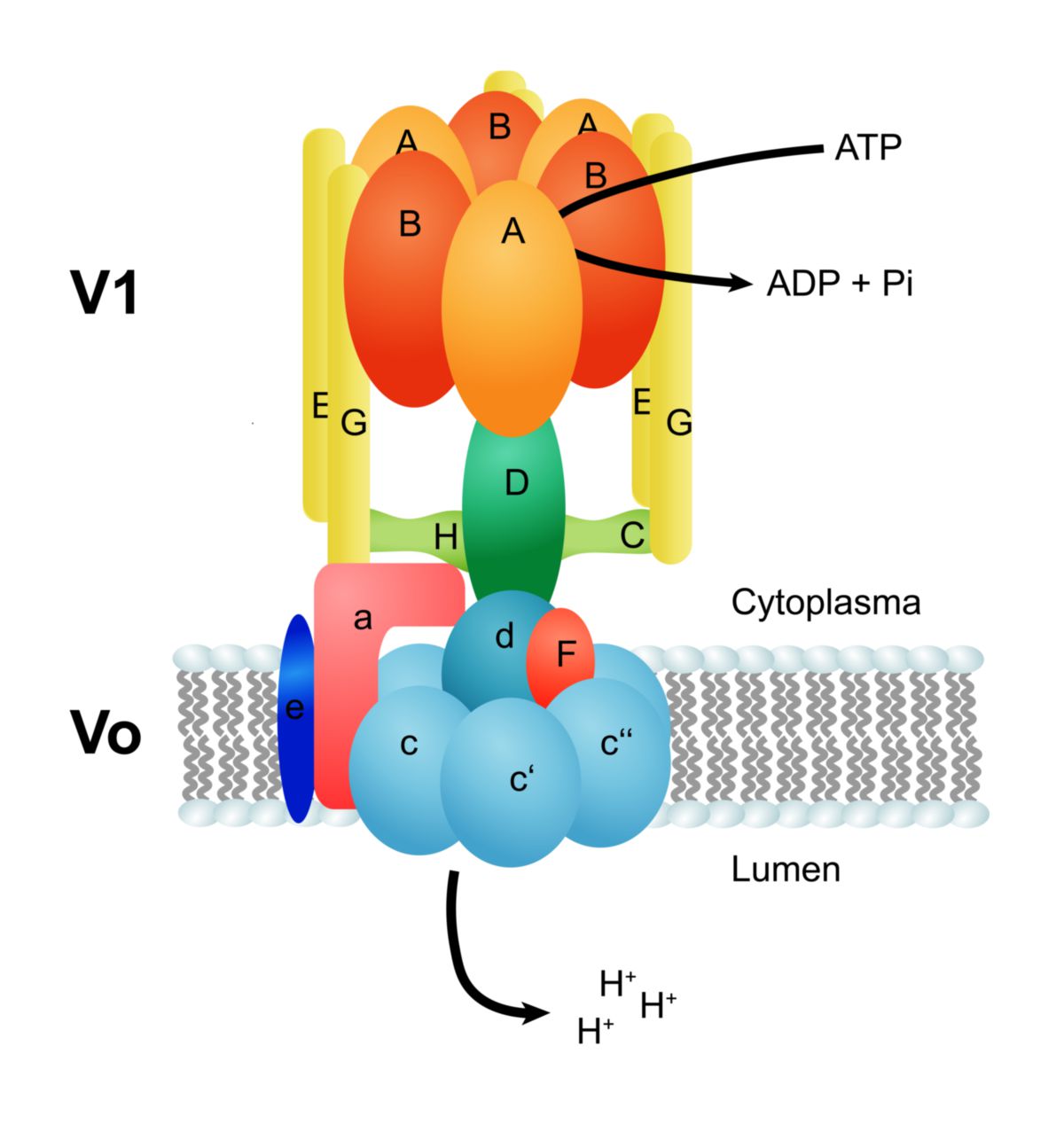
V-ATPasen haben eine sehr ähnliche Struktur wie die F-ATPasen. Sie bestehen aus mehreren enzymatischen Untereinheiten, die sich in zwei Bereiche gliedern lassen: Einen Membran-durchspannenden Bereich (Vo) und einen zytoplasmatischen katalytischen Bereich (V1). Die Untereinheiten wurden nach absteigender molekularer Masse A-H benannt. Die genaue Zusammensetzung variiert aber zwischen den Organismen.[1]
| Bereich | Untereinheit | Molekulare Masse (kD) | Funktion |
|---|---|---|---|
| V1 | A, A, A | 70 | Bindung |
| B, B, B | 60 | ATP-Hydrolyse | |
| E, E, E | 33 | Ständer Untereinheit | |
| G, G, G | 13 | Ständer Untereinheit | |
| C | 40 | Regulatorische Untereinheit | |
| H | 50 | Regulatorische Untereinheit | |
| D | 34 | Rotorachse | |
| F | 14 | Rotorachse | |
| Vo | a | 100 | Protonentransport |
| d | 38 | Kopplung der ATP-Hydrolyse mit Protonentransport | |
| e | 9 | Unbekannt | |
| c | 17 | Protonentransport | |
| c‘ | 17 | Protonentransport | |
| c‘‘ | 21 | Protonentransport |
Biochemie
Kern der Reaktion ist die Kopplung der Energie aus der ATP-Hydrolyse mit dem Transport von Protonen durch die Membran. Pro hydrolysiertem ATP-Molekül werden 3-4 Protonen transportiert. Diese Reaktion wird auch als Umkehrung des ATP-Synthase-Mechanismus charakterisiert, bei dem ein Protonengradient die Synthese von ATP antreibt.
Bindet ein ATP-Molekül an die A- und B-Untereinheit, führt dies zu einer Rotation der der Rotorachse (bestehend aus D, F und d) sowie der anhängenden Proteolipide c, c‘ und c‘‘. Diese Bewegung führt dazu, dass Protonen durch Kanäle der Untereinheit a, mit den Proteolipiden interagieren können. Die Protonen werden dadurch nacheinander in das Lumen des Kompartiments gepumpt.
Funktion
Je nach Lokalisation der V-ATPase kann der Protonentransport unterschiedliche Funktionen haben, jedoch führt er meist zu einer Ansäuerung des Milieus im Kompartiment.
- In Endosomen lösen sich durch den niedrigeren pH-Wert internalisierte Rezeptoren von ihren Liganden, wodurch der Rezeptor recycelt werden kann. Der pH-Wert reguliert auch den Übergang der frühen Endosomen zu den späten Endosomen.
- Innerhalb der Lysosomen aktiviert das saure Milieu hydrolysierende Enzyme des Proteinabbaus.
- Die pflanzliche Vakuole kann extrem niedrige pH-Werte erreichen. Sie kann hier als Speicher- oder Abfallorganell dienen.[2]
- In synaptischen Vesikeln erzeugen V-ATPasen den für den Import von Monoaminen benötigten Protonengradienten. Dieser wird durch Vesikuläre Monoamintransporter unterstützt.
Quellen
- ↑ Toei, M., Saum, R. & Forgac, M. Regulation and isoform function of the V-ATPases. Biochemistry 49, 4715-4723, doi:10.1021/bi100397s (2010).
- ↑ Finbow, M. E. & Harrison, M. A. The vacuolar H+-ATPase: a universal proton pump of eukaryotes. Biochem J 324 ( Pt 3), 697-712 (1997).